1.本发明涉及感光性树脂、包含该感光性树脂的负型感光性树脂组合物、使用该负型感光性树脂组合物的经图案化的固化膜的制造方法、和可成为该感光性树脂的中间体的含有羧基的树脂。
背景技术:
2.就适用于薄膜晶体管型液晶显示装置(tft-lcd)、有机发光元件(oled)、触摸屏面板(tsp)等的显示器用感光性树脂组合物而言,根据经uv(紫外线)照射而发生固化反应、光分解反应并形成图案的方法,分为正型感光材料和负型感光材料。就正型感光材料而言,经uv照射的区域发生光分解反应,溶解于显影液,由此形成图案。就负型感光材料而言,经uv照射的区域发生光固化反应而不溶于显影液,未进行uv照射的区域溶解于显影液,由此形成图案。
3.对于感光性树脂组合物而言,确保对工序中应用的热处理的耐性、对化学蚀刻及气体蚀刻工序的耐性非常重要,尤其是近来,为了使显示器的光效率增加,高透过度及高折射的特性受到重视。为了确保感光性树脂组合物的高耐热性、耐化学性(耐蚀刻性)、高透过性及高折射的特性,首先,在构成感光材料的组合物中,粘结剂的结构及特性非常重要。基于这样的原因,针对向作为感光性树脂组合物的代表性粘结剂树脂而使用的丙烯酸系感光性树脂、以及novolac树脂系、聚酰亚胺等粘结剂树脂赋予感光性的研究正积极进行。但是,以往使用的利用丙烯酸系感光性树脂及novolac树脂等的感光性树脂组合物在300℃以上的高温热处理工序中,耐热性差,因此会因释气(outgassing)而产生杂质,显示器的污染严重。需要说明的是,存在下述问题:因高温热处理而导致透过度降低,使得显示器的光效率特性劣化。
4.例如,专利文献1中公开了使用丙烯酸系化合物与丙烯酸酯化合物的共聚物作为粘结剂树脂、并使用丙烯酸酯系化合物作为多官能性单体而制造的感光性树脂组合物。但是,存在下述问题:由于曝光部与非曝光部之间的溶解度差不充分,因此显影特性不佳,显影过程中本应残留的粘结剂树脂的一部分溶解于显影溶液,从而难以得到10μm以下的微细图案。
5.另外,专利文献2及专利文献3中公开了含有作为聚酰亚胺前体的聚酰胺酸和作为溶解抑制剂的萘醌二叠氮化合物而使热稳定性提高的感光性光刻胶组合物,但是存在下述问题:在形成高分辨率的图案时,曝光部与非曝光部间的溶解速度之差不充分。
6.此外,就感光性树脂组合物而言,需要与下部层及上部层的密合性良好、并具有在与使用目的相应的各种工序条件下均能够形成高分辨率的微细图案的宽工序裕度,并且作为感光材料要求高灵敏度特性,因此,用于提高这样的特性的研究也在积极进行。
7.作为用于解决上述问题的技术,专利文献4中公开了将耐热性优异、具有高透过、高折射特性的特定结构的聚合物作为粘结剂树脂使用的负型感光性树脂组合物、正型感光
性树脂组合物。
8.现有技术文献
9.专利文献
10.专利文献1:美国专利第4139391号
11.专利文献2:日本特开昭52-13315号公报
12.专利文献3:日本特开昭62-135824号公报
13.专利文献4:日本特表2018-531311号公报
技术实现要素:
14.发明所要解决的课题
15.然而,使用专利文献4中记载的负型感光性树脂组合物形成了固化膜(固化物)的情况下,难以同时实现高折射率和高透明性。因此,使用专利文献4中记载的负型感光性树脂组合物形成的固化物存在难以在例如搭载于图像传感器上的微透镜、光波导等光学构件等要求高折射率及高透明性的用途中使用这样的问题。
16.本发明是鉴于上述课题而作出的,其目的在于提供可在能够形成具有高折射率及高透明性的固化膜的负型感光性树脂组合物中使用的感光性树脂、包含该感光性树脂的负型感光性树脂组合物、使用该负型感光性树脂组合物的经图案化的固化膜的制造方法、和可成为该感光性树脂的中间体的含有羧基的树脂。
17.用于解决课题的手段
18.为了达成上述目的,本技术的发明人反复进行深入研究,结果发现,利用在具有下述式(a1)所示的结构单元的含有羧基的树脂中、在含有羧基的树脂所具有的羧基的至少一部分上加成或缩合有具有羧酸反应性基团的(甲基)丙烯酸酯化合物的感光性树脂,能够解决上述课题,从而完成了本发明。具体而言,本发明提供如下所述的方式。
19.本发明的第1方式为感光性树脂,其中,在具有下述式(a1)所示的结构单元的含有羧基的树脂中,在前述含有羧基的树脂所具有的羧基的至少一部分上加成或缩合有具有羧酸反应性基团的(甲基)丙烯酸酯化合物。
20.[化学式1]
[0021][0022]
(式(a1)中,r
1a
及r
2a
各自独立地表示-r
4a
sr
5a
、-r
6a
c(=o)r
7a
、碳原子数为1以上20以下且可包含杂原子的烷基、或碳原子数为6以上20以下且可包含杂原子的芳基,
[0023]r4a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上15以下的亚芳基,
[0024]r5a
表示碳原子数1以上10以下的烷基、或碳原子数6以上15以下的芳基,
[0025]r6a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上10以下的亚芳基,
[0026]r7a
表示碳原子数1以上10以下的烷基、碳原子数1以上10以下的链烯基、或碳原子数6以上15以下的芳基,
[0027]r3a
表示包含芳香族烃基的4价有机基团,
[0028]
键合于r
3a
的4个羰基均与作为r
3a
的前述有机基团中的芳香族烃环键合,
[0029]
a表示下述式(a2)所示的2价基团,
[0030]
j1及j2各自独立地表示1以上6以下的整数。)
[0031]
[化学式2]
[0032][0033]
(式(a2)中,
[0034]
环z1及环z2各自独立地表示芳香族烃环,
[0035]r8a
及r
9a
各自独立地表示氢原子、羟基、巯基、氨基、硝基、卤素原子、氰基或烷基,
[0036]r10a
及r
11a
各自独立地表示氢原子、烷基或芳基,
[0037]
k1及k2各自独立地表示0以上4以下的整数,
[0038]
m1及m2各自独立地表示0以上3以下的整数。)
[0039]
本发明的第2方式为负型感光性树脂组合物,其包含第1方式涉及的感光性树脂、和光聚合引发剂。
[0040]
本发明的第3方式为经图案化的固化膜的制造方法,其包括下述工序:
[0041]
将第2方式涉及的负型感光性树脂组合物涂布于基板上从而形成涂布膜的工序;
[0042]
以位置选择性方式对前述涂布膜进行曝光的工序;以及
[0043]
对曝光后的前述涂布膜进行显影的工序。
[0044]
本发明的第4方式为含有羧基的树脂,其具有下述式(a1-1)所示的结构单元。
[0045]
[化学式3]
[0046][0047]
(式(a1-1)中,r
1a
及r
2a
各自独立地表示-r
4a
sr
5a
、-r
6a
c(=o)r
7a
、碳原子数为1以上20以下且可包含杂原子的烷基、或碳原子数为6以上20以下且可包含杂原子的芳基,
[0048]r4a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上15以下的亚芳基,
[0049]r5a
表示碳原子数1以上10以下的烷基、或碳原子数6以上15以下的芳基,
[0050]r6a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上10以下的亚芳基,
[0051]r7a
表示碳原子数1以上10以下的烷基、碳原子数1以上10以下的链烯基、或碳原子数6以上15以下的芳基,
[0052]r31a
表示下述式(a1a)所示的4价基团,
[0053]
>ar
1a-x
1-ar
2a
<
···
(a1a)
[0054]
ar
1a
及ar
2a
各自独立地表示可被供电子性基团取代的芳香族烃基,
[0055]
x1表示不与ar
1a
及ar
2a
一起形成π共轭体系的2价连接基团,
[0056]
a表示下述式(a2)所示的2价基团,
[0057]
j1及j2各自独立地表示1以上6以下的整数。)
[0058]
[化学式4]
[0059][0060]
(式(a2)中,
[0061]
环z1及环z2各自独立地表示芳香族烃环,
[0062]r8a
及r
9a
各自独立地表示氢原子、羟基、巯基、氨基、硝基、卤素原子、氰基或烷基,
[0063]r10a
及r
11a
各自独立地表示氢原子、烷基或芳基,
[0064]
k1及k2各自独立地表示0以上4以下的整数,
[0065]
m1及m2各自独立地表示0以上3以下的整数。)
[0066]
发明效果
[0067]
根据本发明,可以提供可在能够形成具有高折射率及高透明性的固化膜的负型感光性树脂组合物中使用的感光性树脂、包含该感光性树脂的负型感光性树脂组合物、使用该负型感光性树脂组合物的经图案化的固化膜的制造方法、和可成为该感光性树脂的中间体的含有羧基的树脂。
具体实施方式
[0068]
以下,详细地说明本发明。
[0069]
《感光性树脂》
[0070]
本发明的感光性树脂(以下也记载为“感光性树脂(a)”)为:在具有下述式(a1)所示的结构单元的含有羧基的树脂中、在含有羧基的树脂所具有的羧基的至少一部分上加成或缩合有具有羧酸反应性基团的(甲基)丙烯酸酯化合物的树脂。
[0071]
[化学式5]
[0072][0073]
(式(a1)中,r
1a
及r
2a
各自独立地表示-r
4a
sr
5a
、-r
6a
c(=o)r
7a
、碳原子数为1以上20以下且可包含杂原子的烷基、或碳原子数为6以上20以下且可包含杂原子的芳基,
[0074]r4a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上15以下的亚芳基,
[0075]r5a
表示碳原子数1以上10以下的烷基、或碳原子数6以上15以下的芳基,
[0076]r6a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上10以下的亚芳基,
[0077]r7a
表示碳原子数1以上10以下的烷基、碳原子数1以上10以下的链烯基、或碳原子数6以上15以下的芳基,
[0078]r3a
表示包含芳香族烃基的4价有机基团,
[0079]
键合于r
3a
的4个羰基均与作为r
3a
的前述有机基团中的芳香族烃环键合,
[0080]
a表示下述式(a2)所示的2价基团,
[0081]
j1及j2各自独立地表示1以上6以下的整数。)
[0082]
[化学式6]
[0083][0084]
(式(a2)中,
[0085]
环z1及环z2各自独立地表示芳香族烃环,
[0086]r8a
及r
9a
各自独立地表示氢原子、羟基、巯基、氨基、硝基、卤素原子、氰基或烷基,
[0087]r10a
及r
11a
各自独立地表示氢原子、烷基或芳基,
[0088]
k1及k2各自独立地表示0以上4以下的整数,
[0089]
m1及m2各自独立地表示0以上3以下的整数。)
[0090]
首先,对具有式(a1)所示的结构单元的含有羧基的树脂(以下也称为“含有羧基的树脂”)进行说明。
[0091]
如可以由上述式(a1)的结构确认的那样,具有式(a1)所示的结构单元的含有羧基的树脂在其结构单元中具有羧基。
[0092]
另外,如可以由上述式(a2)的结构确认的那样,具有式(a1)所示的结构单元的含有羧基的树脂在其结构单元中具有联苯芴结构作为基本结构。
[0093]
式(a1)中,杂原子是指除碳原子和氢原子以外的元素。作为杂原子,例如,可举出氧原子、氮原子、硫原子、卤素原子、硅原子。这些杂原子可以被包含有多个。杂原子优选为
硫原子,在该情况下,具有耐热性、耐化学性、高透过性、高折射及光学特性特别优异的效果。
[0094]
式(a1)中,作为r
1a
及r
2a
的可包含杂原子的烷基的碳原子数为1以上20以下,优选为2以上15以下,更优选为2以上10以下。作为可包含杂原子的烷基的具体例,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、2-乙基己基、正壬基、正癸基等。
[0095]
作为r
1a
及r
2a
的可包含杂原子的芳基的碳原子数为6以上20以下,优选为6以上15以下,更优选为6以上10以下。作为可包含杂原子的芳基的具体例,可举出苯基、萘基、呋喃基、噻吩基等。
[0096]
关于作为r
4a
的碳原子数1以上10以下的亚烷基的具体例,可举出亚甲基、亚乙基、亚正丙基、亚异丙基等。
[0097]
关于作为r
4a
的碳原子数6以上15以下的亚芳基的具体例,可举出亚苯基、亚萘基等。
[0098]
关于作为r
5a
的碳原子数1以上10以下的烷基的具体例,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、2-乙基己基、正壬基、正癸基等。
[0099]
关于作为r
5a
的碳原子数6以上15以下的芳基的具体例,可举出苯基、萘基等。
[0100]
若r
1a
及r
2a
为-r
4a
sr
5a
,则具有耐热性、高透过及高折射的特性特别优异的效果。
[0101]
关于作为r
6a
的碳原子数1以上10以下的亚烷基的具体例,可举出与针对r
4a
示例的亚烷基同样的基团。
[0102]
关于作为r
6a
的碳原子数6以上10以下的亚芳基的具体例,可举出与针对r
4a
示例的亚芳基同样的基团。
[0103]
关于作为r
7a
的碳原子数1以上10以下的烷基的具体例,可举出与针对r
5a
示例的烷基同样的基团。
[0104]
关于作为r
7a
的碳原子数6以上15以下的芳基的具体例,可举出与针对r
5a
示例的芳基同样的基团。
[0105]
关于作为r
7a
的碳原子数1以上10以下的链烯基的具体例,可举出乙烯基及烯丙基等。
[0106]r3a
表示包含芳香族烃基的4价有机基团,键合于r
3a
的4个羰基均与作为r
3a
的4价有机基团中的芳香族烃环键合。
[0107]
作为r
3a
中包含的芳香族烃基,可举出由1个苯环形成的基团、多个苯环介由单键进行键合而形成的基团、多个苯环介由羰基键合而形成的基团、多个苯环进行稠合而形成的基团。
[0108]
另外,r
3a
中包含的芳香族烃基可以为1个,也可以为多个。
[0109]
关于作为r
3a
的包含芳香族烃基的4价有机基团,可举出仅由芳香族烃基形成的基团、及多个芳香族烃基通过-o-、-s-、亚烷基等连接基团进行连接而成的基团,但优选为下述式(a1a)所示的4价有机基团。
[0110]
>ar
1a-x
1-ar
2a
<
···
(a1a)
[0111]
(式(a1a)中,
[0112]
ar
1a
及ar
2a
各自独立地表示可被供电子性基团取代的芳香族烃基,x1表示不与ar
1a
及ar
2a
一起形成π共轭体系的2价连接基团。)
[0113]
式(a1a)中,作为ar
1a
及ar
2a
的芳香族烃基没有特别限定,只要不损害所期望的效果即可。作为ar
1a
及ar
2a
的芳香族烃基与r
3a
中的芳香族烃基同样。
[0114]
作为供电子性基团,只要是化学领域中的技术人员通常识别为供电子性基团的基团即可,没有特别限定。作为供电子性基团,可举出烷氧基、氨基、烷基等。
[0115]
式(a1a)中,关于作为x1的、不与ar
1a
及ar
2a
一起形成π共轭体系的2价连接基团,可举出-o-、-s-、亚烷基、及选自它们中的2种以上的组合等。另外,只要不形成包含ar
1a
及ar
2a
的π共轭体系,则x1也可以包含苯环、及萘环等芳香族烃环。需要说明的是,羰基(-c(=o)-)、亚乙烯基(-ch=ch-)等由于与ar
1a
及ar
2a
一起形成π共轭体系,因此不属于x1。x1为单键的情况下,也由于与ar
1a
及ar
2a
一起形成π共轭体系而不属于式(a1a)。
[0116]
作为式(a1a)所示的基团,可举出下述式(a1b)所示的基团。
[0117]
>ar
3a-(x
2-ar
5a
)
n-x
3-ar
4a
<
···
(a1b)
[0118]
((a1b)中,
[0119]
ar
3a
、ar
4a
及ar
5a
各自独立地表示可被供电子性基团取代的芳香族烃基,
[0120]
x2及x3各自独立地表示氧原子、硫原子、或碳原子数1以上10以下的亚烷基,
[0121]
n表示0以上2以下的整数。)
[0122]
式(a1b)中,ar
3a
、ar
4a
及ar
5a
中的芳香族烃基及供电子性基团与ar
1a
及ar
2a
中的芳香族烃基及供电子性基团同样。关于作为ar
3a
及ar
4a
的芳香族烃基,优选为苯-1,2,4-三基。关于作为ar
5a
的芳香族烃基,优选为对亚苯基及间亚苯基,更优选为对亚苯基。
[0123]
作为r
3a
的具体例,可举出下述的4价基团、下述4价基团中苯环的氢原子被甲基、乙基、甲氧基、或乙氧基等的1个以上的供电子性基团取代而得到的基团。
[0124]
[化学式7]
[0125][0126]
j1及j2各自独立地为1以上6以下的整数,优选为1以上3以下的整数,更优选为1以上2以下的整数。
[0127]
式(a2)中,环z1及环z2各自独立地为芳香族烃环。
[0128]
作为芳香族烃环,可举出萘环、苯环等,萘环从高折射率化的方面考虑是优选的。
[0129]
式(a2)中,r
8a
及r
9a
各自独立地为氢原子、羟基(-oh)、巯基(-sh)、氨基(-nh2)、硝基
(-no2)、卤素原子、氰基或烷基。
[0130]
关于作为r
8a
及r
9a
的卤素原子的具体例,可举出氯原子、氟原子、溴原子、及碘原子。
[0131]
作为r
8a
及r
9a
的烷基例如为碳原子数1以上10以下的烷基。作为其具体例,可举出与针对r
5a
示例的烷基同样的基团。
[0132]r8a
及r
9a
优选为氢原子。
[0133]
作为r
10a
及r
11a
的烷基例如为碳原子数1以上10以下的烷基。作为其具体例,可举出与针对r
5a
示例的烷基同样的基团。
[0134]
作为r
10a
及r
11a
的芳基例如为碳原子数6以上15以下的芳基。作为其具体例,可举出与针对r
5a
示例的芳基同样的基团。
[0135]
k1及k2各自独立地为0以上4以下的整数,优选为0以上2以下的整数。
[0136]
m1及m2各自独立地为0以上3以下的整数,优选为1以上2以下的整数。
[0137]
作为式(a2)所示的2价基团,可举出下述式(a2-1)所示的2价基团。
[0138]
[化学式8]
[0139][0140]
(式(a2-1)中,
[0141]r8a
及r
9a
各自独立地表示氢原子、羟基、巯基、氨基、硝基、卤素原子、氰基或烷基,
[0142]r10a
及r
11a
各自独立地表示氢原子、烷基或芳基,
[0143]
k1及k2各自独立地表示0以上4以下的整数,
[0144]
m1及m2各自独立地表示0以上3以下的整数。)
[0145]
式(a2-1)中的r
8a
~r
11a
、k1、k2、m1及m2与式(a2)中的r
8a
~r
11a
、k1、k2、m1及m2同样。
[0146]
需要说明的是,具有式(a1)所示的结构单元的含有羧基的树脂中,r
3a
为式(a1a)所示的4价有机基团的树脂为新型树脂。即,具有下述式(a1-1)所示的结构单元的含有羧基的树脂为新型树脂。
[0147]
另外,具有下述式(a1-1)所示的结构单元的含有羧基的树脂具有高折射率及高透过率。
[0148]
[化学式9]
[0149][0150]
(式(a1-1)中,r
1a
及r
2a
各自独立地表示-r
4a
sr
5a
、-r
6a
c(=o)r
7a
、碳原子数为1以上20以下且可包含杂原子的烷基、或碳原子数为6以上20以下且可包含杂原子的芳基,
[0151]r4a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上15以下的亚芳基,
[0152]r5a
表示碳原子数1以上10以下的烷基、或碳原子数6以上15以下的芳基,
[0153]r6a
表示单键、碳原子数1以上10以下的亚烷基、或碳原子数6以上10以下的亚芳基,
[0154]r7a
表示碳原子数1以上10以下的烷基、碳原子数1以上10以下的链烯基、或碳原子数6以上15以下的芳基,
[0155]r31a
表示下述式(a1a)所示的4价基团,
[0156]
>ar
1a-x
1-ar
2a
<
···
(a1a)
[0157]
ar
1a
及ar
2a
各自独立地表示可被供电子性基团取代的芳香族烃基,
[0158]
x1表示不与ar
1a
及ar
2a
一起形成π共轭体系的2价连接基团,
[0159]
a表示下述式(a2)所示的2价基团,
[0160]
j1及j2各自独立地表示1以上6以下的整数。)
[0161]
[化学式10]
[0162][0163]
(式(a2)中,
[0164]
环z1及环z2各自独立地表示芳香族烃环,
[0165]r8a
及r
9a
各自独立地表示氢原子、羟基、巯基、氨基、硝基、卤素原子、氰基或烷基,
[0166]r10a
及r
11a
各自独立地表示氢原子、烷基或芳基,
[0167]
k1及k2各自独立地表示0以上4以下的整数,
[0168]
m1及m2各自独立地表示0以上3以下的整数。)
[0169]
具有式(a1)所示的结构单元的含有羧基的树脂所具有的式(a1)所示的结构单元的数目没有特别限定。具有式(a1)所示的结构单元的含有羧基的树脂所具有的式(a1)所示的结构单元数例如为1以上30以下的整数,优选为1以上10以下的整数。在该范围内时,具有耐热性、高透过及高折射的特性特别优异的效果。
[0170]
具有式(a1)所示的结构单元的含有羧基的树脂的质均分子量例如可以优选为1,
000g/mol以上100,000g/mol以下,更优选为1,500g/mol以上50,000g/mol以下,进一步优选为2,000g/mol以上10,000g/mol以下。
[0171]
另外,具有式(a1)所示的结构单元的含有羧基的树脂的分散度(质均分子量mw/数均分子量mn)例如可以为1.0以上5.0以下的范围,优选为1.5以上4.0以下的范围。
[0172]
需要说明的是,本说明书中的质均分子量、数均分子量、分散度可利用凝胶渗透色谱(gpc)法测定。
[0173]
具有式(a1)所示的结构单元的含有羧基的树脂例如可利用专利文献4中记载的方法制造。
[0174]
具体而言,具有式(a1)所示的结构单元的含有羧基的树脂可通过下述方式合成:从下述式(1)所示的化合物合成下述式(2)所示的包含羟基的化合物(单体),然后与下述式(3)所示的四羧酸二酐进行聚合反应。
[0175]
[化学式11]
[0176][0177]
(式(1)中,环z1及环z2、r
8a
~r
11a
、k1、k2、m1及m2分别与式(a2)中的环z1及环z2、r
8a
~r
11a
、k1、k2、m1及m2同样,r
12a
及r
13a
各自独立地表示羟基、硫醇基、氨基、硝基、氰基、包含杂原子的碳原子数1以上20以下的脂肪族烷基或脂环族烷基、或者包含杂原子的碳原子数6以上20以下的芳基。)
[0178]
[化学式12]
[0179][0180]
(式(2)中,环z1及环z2、r
8a
~r
11a
、k1、k2、m1及m2分别与式(a2)中的环z1及环z2、r
8a
~r
11a
、k1、k2、m1及m2同样,r
1a
、r
2a
、j1及j2分别与式(a1)中的r
1a
、r
2a
、j1及j2同样。)
[0181]
[化学式13]
[0182][0183]
(式(3)中,r
3a
与式(a1)中的r
3a
同样。)
[0184]
式(1)中,杂原子是指除碳原子和氢原子以外的元素。作为杂原子,例如,可举出氧原子、氮原子、硫原子、卤素原子、硅原子。这些杂原子可以被包含有多个。例如,r
12a
及r
13a
可以以羟基、硫醇基、氨基、硝基、氰基的形态包含杂原子。
[0185]
作为r
12a
及r
13a
的包含杂原子的脂肪族烷基或脂环族烷基的碳原子数为1以上20以下,优选为1以上10以下,更优选为3以上8以下,特别优选为3以上5以下。作为包含杂原子的脂肪族烷基或脂环族烷基的具体例,可举出碳原子数1以上5以下的、羟基烷基或硫代烷基。
[0186]
作为r
12a
及r
13a
的包含杂原子的芳基的碳原子数为6以上20以下,优选为6以上15以下,更优选为6以上10以下,特别优选为7以上10以下。
[0187]r12a
及r
13a
优选为羟基。
[0188]
聚合反应例如可以在2小时~24小时、或4小时~12小时之间于100~130℃、或110~120℃实施。
[0189]
以上述式(2)所示的包含羟基的化合物100质量份为基准,式(3)所示的四羧酸二酐例如可以以5质量份以上40质量份以下、10质量份以上30质量份以下、或10质量份以上20质量份以下的量使用。
[0190]
在具有式(a1)所示的结构单元的含有羧基的树脂的制造中,例如,可以在上述的聚合反应开始后加入封端剂进行反应。通过封端剂,具有式(a1)所示的结构单元的含有羧基的树脂的质均分子量的控制变得容易。但是,由于存在折射率因封端剂而降低的倾向,因此优选不使用封端剂。
[0191]
该封端剂的反应(封端反应)例如可以在30分钟~4小时、或1小时~3小时之间于100~130℃、或110~120℃实施。
[0192]
以上述式(2)所示的包含羟基的化合物100质量份为基准,前述封端剂例如可以以2质量份以上10质量份以下、2质量份以上5质量份以下、或3质量份以上5质量份以下的量投入。
[0193]
作为封端剂,可举出有机酸、有机酸酐、酰胺酸。
[0194]
作为封端剂,优选为芳香族羧酸酐,作为具体例,可举出邻苯二甲酸酐。
[0195]
使用了封端剂的情况下,具有式(a1)所示的结构单元的含有羧基的树脂的末端结构可成为来自封端剂的结构。
[0196]
另外,具有式(a1)所示的结构单元的含有羧基的树脂的末端结构可成为来自上述式(2)所示的包含羟基的化合物、四羧酸二酐等原料中过量加入的原料的结构。
[0197]
更具体而言,具有式(a1)所示的结构单元的含有羧基的树脂的末端结构例如可以为以下的结构1~结构3,可以适当地控制具有式(a1)所示的结构单元的含有羧基的树脂的质均分子量。构成具有式(a1)所示的结构单元的含有羧基的树脂的树脂的分子链中的多个末端的结构可以彼此不同。关于结构3的下述ox为结构2中的羟基、与上述的封端剂反应而生成的基团。
[0198]
结构1:在式(a1)所示的结构中的左端的羰基氧基上键合有氢原子的结构
[0199]
结构2:-chr
2a-(ch2)
j2-o-a-o-(ch2)
j1-ch(oh)-r
1a
所示的结构
[0200]
结构3:-chr
2a-(ch2)
j2-o-a-o-(ch2)
j1-ch(ox)-r
1a
所示的结构
[0201]
感光性树脂(a)为在这样的具有式(a1)所示的结构单元的含有羧基的树脂所具有的羧基的至少一部分上加成或缩合有具有羧酸反应性基团的(甲基)丙烯酸酯化合物的树
脂。
[0202]
即,感光性树脂(a)为使具有羧酸反应性基团的(甲基)丙烯酸酯化合物加成或缩合于具有式(a1)所示的结构单元的含有羧基的树脂所具有的羧基的至少一部分上而得到的树脂。
[0203]
如可以由上述式(a2)的结构确认的那样,感光性树脂(a)在其结构单元中具有联苯芴结构作为基本结构。
[0204]
另外,感光性树脂(a)在其结构单元中具有来自具有羧酸反应性基团的(甲基)丙烯酸酯化合物的、(甲基)丙烯酰基氧基。
[0205]
需要说明的是,本说明书中,所谓“(甲基)丙烯酸酯”,是指“丙烯酸酯”及“甲基丙烯酸酯”这两者,所谓“(甲基)丙烯
‑”
,是指“丙烯
‑”
及“甲基丙烯
‑”
这两者,所谓“(甲基)丙烯酰基氧基”,是指“丙烯酰基氧基”及“甲基丙烯酰基氧基”这两者。
[0206]
所谓羧酸反应性基团,是与羧酸、或卤代羰基这样的由羧基衍生的基团反应的官能团。即,具有羧酸反应性基团的(甲基)丙烯酸酯化合物的羧酸反应性基团与具有式(a1)所示的结构单元的含有羧基的树脂的羧基、由羧基衍生的基团进行加成或缩合反应。
[0207]
作为羧酸反应性基团,可举出具有环氧基的基团、氨基、羟基、异氰酸酯基等。作为具有环氧基的基团,例如可举出缩水甘油基、环氧环戊基、环氧环己基、环氧环戊基甲基、环氧环己基甲基、环氧环戊基乙基、及环氧环己基甲基等。
[0208]
作为具有羧酸反应性基团的(甲基)丙烯酸酯化合物的具体例,可举出丙烯酸缩水甘油酯、甲基丙烯酸缩水甘油酯、丙烯酸羟基乙酯、甲基丙烯酸羟基乙酯、丙烯酸羟基丙酯、甲基丙烯酸羟基丙酯等。
[0209]
通过包含这样的感光性树脂(a)、以及详情后述的光聚合引发剂(c)的负型感光性树脂组合物,如后述的实施例所示,能够形成具有高折射率及高透明性的固化膜。因此,由包含感光性树脂(a)和光聚合引发剂(c)的负型感光性树脂组合物形成的固化膜可以用作要求高折射率及高透明性的构件、例如搭载于图像传感器上的微透镜、光波导等光学构件。
[0210]
另外,该负型感光性树脂组合物可以通过曝光及显影而形成经图案化的固化膜。
[0211]
另外,该负型感光性树脂组合物还能够形成具有高耐溶剂性的固化膜。
[0212]
感光性树脂(a)中,r
3a
为式(a1a)所示的4价有机基团时,能够以特别高的水平同时实现固化物的折射率及透明性。r
3a
为式(a1a)所示的4价有机基团时能够以特别高的水平同时实现折射率及透明性的理由不明确。
[0213]
但是,式(a1a)所示的4价有机基团是两末端分别为芳香族烃基、在该两末端的芳香族烃基之间π共轭体系被中断的结构。因此,推测该结构是能够以特别高的水平同时实现折射率及透明性的一个原因。
[0214]
需要说明的是,感光性树脂(a)的末端结构与具有上述式(a1)所示的结构单元的含有羧基的树脂的末端结构同样。
[0215]
感光性树脂(a)的质均分子量例如可以优选为1,100g/mol以上100,500g/mol以下,更优选为1,600g/mol以上50,500g/mol以下,进一步优选为2,100g/mol以上10,500g/mol以下。
[0216]
另外,感光性树脂(a)的分散度(质均分子量mw/数均分子量mn)例如可以为1.0以上5.0以下的范围,优选为1.5以上4.0以下的范围。
[0217]
感光性树脂(a)可以通过具有式(a1)所示的结构单元的含有羧基的树脂与具有羧酸反应性基团的(甲基)丙烯酸酯化合物的加成反应或缩合反应来制造。通过该反应,使具有羧酸反应性基团的(甲基)丙烯酸酯化合物加成或缩合于具有式(a1)所示的结构单元的含有羧基的树脂所具有的羧基的至少一部分上。
[0218]
反应例如可以在30分钟~5小时、优选1小时~3小时之间于80~120℃、优选90~110℃实施。
[0219]
也可以使具有羧酸反应性基团的(甲基)丙烯酸酯化合物加成或缩合于具有式(a1)所示的结构单元的含有羧基的树脂所具有的全部羧基上,但从含有感光性树脂(a)的负型感光性树脂组合物的显影性的观点考虑,优选的是,使具有羧酸反应性基团的(甲基)丙烯酸酯化合物加成或缩合于具有式(a1)所示的结构单元的含有羧基的树脂所具有的羧基的一部分上,在感光性树脂(a)中残存有羧基。
[0220]
例如,具有羧酸反应性基团的(甲基)丙烯酸酯化合物相对于具有式(a1)所示的结构单元的含有羧基的树脂的摩尔比(具有羧酸反应性基团的(甲基)丙烯酸酯化合物/具有式(a1)所示的结构单元的含有羧基的树脂)优选为0.05以上0.50以下,更优选为0.10以上0.40以下,进一步优选为0.15以上0.30以下。
[0221]
《负型感光性树脂组合物》
[0222]
负型感光性树脂组合物包含上述的感光性树脂(a)、和光聚合引发剂(c)。
[0223]
负型感光性树脂组合物可以根据需要而包含光聚合性化合物(b)、密合增强剂(d)、溶剂(s)、其他成分。
[0224]
如后述的实施例所示,包含上述的感光性树脂(a)、和光聚合引发剂(c)的负型感光性树脂组合物能够形成具有高折射率及高透明性的固化膜。因此,由负型感光性树脂组合物形成的固化膜可以用作要求高折射率及高透明性的构件、例如搭载于图像传感器上的微透镜、光波导等光学构件。
[0225]
另外,负型感光性树脂组合物可以通过曝光及显影而形成经图案化的固化膜。
[0226]
另外,还能够利用负型感光性树脂组合物形成具有高耐溶剂性的固化膜。
[0227]
以下,对负型感光性树脂组合物所包含的、除感光性树脂(a)以外的必需或任选的成分、和负型感光性树脂组合物的制造方法进行说明。
[0228]
<光聚合性化合物(b)>
[0229]
负型感光性树脂组合物可以包含或不包含光聚合性化合物(b)。
[0230]
光聚合性化合物(b)没有特别限定,例如,可举出具有烯键式不饱和键的交联性化合物。
[0231]
具有烯键式不饱和键的交联性化合物通常为具有至少2个以上的烯键式双键的交联性单体,例如,可举出:乙二醇二丙烯酸酯、乙二醇二甲基丙烯酸酯、二乙二醇二丙烯酸酯、三乙二醇二丙烯酸酯、三乙二醇二甲基丙烯酸酯、四乙二醇二丙烯酸酯、四乙二醇二甲基丙烯酸酯、丁二醇二甲基丙烯酸酯、丙二醇二丙烯酸酯、丙二醇二甲基丙烯酸酯、三羟甲基丙烷三丙烯酸酯、三羟甲基丙烷三甲基丙烯酸酯、四羟甲基丙烷四丙烯酸酯、四羟甲基丙烷四甲基丙烯酸酯、季戊四醇三丙烯酸酯、季戊四醇三甲基丙烯酸酯、季戊四醇四丙烯酸酯、季戊四醇四甲基丙烯酸酯、二季戊四醇五丙烯酸酯、二季戊四醇五甲基丙烯酸酯、二季戊四醇六丙烯酸酯、二季戊四醇六甲基丙烯酸酯、1,6-己二醇二丙烯酸酯、1,6-己二醇二甲
基丙烯酸酯、cardo环氧基二丙烯酸酯及它们的聚(poly-)合物(聚乙二醇二丙烯酸酯)等多作用性(甲基)丙烯酸系单体及低聚物类;
[0232]
使多元醇类与一元酸或多元酸缩合得到的聚酯预聚物、与(甲基)丙烯酸反应而得到的聚酯(甲基)丙烯酸酯,使多元醇与具有2个异氰酸酯基的化合物反应后、与(甲基)丙烯酸反应而得到的聚氨酯(甲基)丙烯酸酯;
[0233]
双酚a型环氧树脂、双酚f型环氧树脂、双酚s型环氧树脂、苯酚或甲酚novolac型环氧树脂、resol型环氧树脂、三酚甲烷型环氧树脂、聚羧酸聚缩水甘油酯、多元醇聚缩水甘油酯、脂肪族或脂环式环氧树脂、胺环氧树脂、二羟基苯型环氧树脂等环氧树脂与(甲基)丙烯酸反应而得到的环氧(甲基)丙烯酸酯树脂。另外,考虑到曝光灵敏度等,优选使用多官能性(甲基)丙烯酸系单体作为光聚合性化合物(b)。
[0234]
包含光聚合性化合物(b)的情况下,光聚合性化合物(b)优选以相对于感光性树脂(a)100质量份而言为0.1质量份以上200质量份以下的量被包含,更优选以1质量份以上100质量份以下的量被包含,进一步优选以10质量份以上80质量份以下的量被包含。
[0235]
<光聚合引发剂(c)>
[0236]
作为光聚合引发剂(c),没有特别限定,可以使用以往已知的光聚合引发剂。
[0237]
作为光聚合引发剂(c),可举出肟酯化合物。
[0238]
作为肟酯化合物,优选为具有下述式(c1)所示的部分结构的化合物。
[0239]
[化学式14]
[0240][0241]
(式(c1)中,
[0242]
n1为0或1,
[0243]rc2
为一价有机基团,
[0244]rc3
为氢原子、可具有取代基的碳原子数1以上20以下的脂肪族烃基、或可具有取代基的芳基,
[0245]
*为化学键。)
[0246]
具有式(c1)所示的部分结构的化合物优选具有咔唑骨架、芴骨架、二苯基醚骨架、苯硫醚骨架。
[0247]
具有式(c1)所示的部分结构的化合物优选具有1个或2个式(c1)所示的部分结构。
[0248]
作为具有式(c1)所示的部分结构的化合物,可举出下述式(c2)所示的化合物。
[0249]
[化学式15]
[0250][0251]
(式(c2)中,r
c1
为下述式(c3)、(c4)、或(c5)所示的基团,
[0252]
n1为0或1,
[0253]rc2
为一价有机基团,
[0254]rc3
为氢原子、可具有取代基的碳原子数1以上20以下的脂肪族烃基、或可具有取代基的芳基。)
[0255]
[化学式16]
[0256][0257]
(式(c3)中,r
c4
及r
c5
各自独立地为1价有机基团,
[0258]
n2为0以上3以下的整数,
[0259]
n2为2或3的情况下,多个r
c5
可以相同也可以不同,多个r
c5
可以相互键合而形成环。
[0260]
*为化学键。)
[0261]
[化学式17]
[0262][0263]
(式(c4)中,r
c6
及r
c7
各自独立地为可具有取代基的链状烷基、可具有取代基的链状烷氧基、可具有取代基的环状有机基团、或氢原子,
[0264]rc6
与r
c7
可以相互键合而形成环,
[0265]rc7
与芴骨架中的苯环可以相互键合而形成环,
[0266]rc8
为硝基或1价有机基团,
[0267]
n3为0以上4以下的整数,
[0268]
*为化学键。)
[0269]
[化学式18]
[0270][0271]
(式(c5)中,r
c9
为1价有机基团、卤素原子、硝基、或氰基,
[0272]
a为s或o,
[0273]
n4为0以上4以下的整数,
[0274]
*为化学键。)
[0275]
式(c3)中,r
c4
为1价有机基团。r
c4
可以在不妨碍本发明的目的的范围内从各种有机基团中选择。作为有机基团,优选为含有碳原子的基团,更优选为包含1个以上的碳原子、以及选自由h、o、s、se、n、b、p、si及卤素原子组成的组中的1个以上的原子的基团。含有碳原子的基团的碳原子数没有特别限定,优选为1以上50以下,更优选为1以上20以下。
[0276]
作为r
c4
的优选例,可举出碳原子数1以上20以下的可具有取代基的烷基、碳原子数3以上20以下的可具有取代基的环烷基、碳原子数2以上20以下的可具有取代基的饱和脂肪族酰基、碳原子数2以上20以下的可具有取代基的烷氧基羰基、可具有取代基的苯基、可具有取代基的苯甲酰基、可具有取代基的苯氧基羰基、可具有取代基的碳原子数7以上20以下的苯基烷基、可具有取代基的萘基、可具有取代基的萘甲酰基、可具有取代基的萘氧基羰基、可具有取代基的碳原子数11以上20以下的萘基烷基、可具有取代基的杂环基、及可具有取代基的杂环基羰基等。
[0277]rc4
中,优选为碳原子数1以上20以下的烷基。该烷基可以为直链状,也可以为支链状。从式(c3)所示的化合物在感光性树脂组合物中的溶解性良好的方面考虑,作为r
c4
的烷基的碳原子数优选为2以上,更优选为5以上,特别优选为7以上。另外,从感光性树脂组合物中的、式(c3)所示的化合物与其他成分的相容性良好的方面考虑,作为r
c4
的烷基的碳原子数优选为15以下,更优选为10以下。
[0278]rc4
具有取代基的情况下,作为该取代基的优选例,可举出羟基、碳原子数1以上20以下的烷基、碳原子数1以上20以下的烷氧基、碳原子数2以上20以下的脂肪族酰基、碳原子数2以上20以下的脂肪族酰基氧基、苯氧基、苯甲酰基、苯甲酰基氧基、-po(or)2所示的基团(r为碳原子数1以上6以下的烷基)、卤素原子、氰基、杂环基等。
[0279]rc4
为杂环基的情况下,该杂环基可以为脂肪族杂环基,也可以为芳香族杂环基。r
c4
为杂环基的情况下,杂环基为包含1个以上的n、s、o的5元或6元的单环,或者为所述单环彼此、或所述单环与苯环稠合而成的杂环基。杂环基为稠合环的情况下,使其环数为3以下。作为构成所述杂环基的杂环,可举出呋喃、噻吩、吡咯、噁唑、异噁唑、噻唑、噻二唑、异噻唑、咪唑、吡唑、三唑、吡啶、吡嗪、嘧啶、哒嗪、苯并呋喃、苯并噻吩、吲哚、异吲哚、吲哚嗪、苯并咪唑、苯并三唑、苯并噁唑、苯并噻唑、咔唑、嘌呤、喹啉、异喹啉、喹唑啉、酞嗪、噌啉、喹喔啉、哌啶、哌嗪、吗啉、哌啶、四氢吡喃、及四氢呋喃等。
[0280]rc4
为杂环基的情况下,作为该杂环基可具有的取代基,可举出羟基、碳原子数1以上6以下的烷氧基、卤素原子、氰基、硝基等。
[0281]
作为以上说明的r
c4
的优选的具体例,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、新戊基、戊烷-3-基、仲戊基、叔戊基、正己基、正庚
基、正辛基、及2-乙基己基。
[0282]
另外,从式(c3)所示的化合物在感光性树脂组合物中的溶解性良好的方面考虑,优选为正辛基、及2-乙基己基,更优选为2-乙基己基。
[0283]
式(c3)中,r
c5
为1价有机基团。r
c5
可以在不妨碍本发明的目的的范围内从各种有机基团中选择。作为有机基团,优选为含有碳原子的基团,更优选为包含1个以上的碳原子、以及选自由h、o、s、se、n、b、p、si及卤素原子组成的组中的1个以上的原子的基团。含有碳原子的基团的碳原子数没有特别限定,优选为1以上50以下,更优选为1以上20以下。
[0284]
关于作为r
c5
而优选的1价有机基团的例子,可举出烷基、烷氧基、环烷基、环烷氧基、饱和脂肪族酰基、烷氧基羰基、饱和脂肪族酰基氧基、可具有取代基的苯基、可具有取代基的苯氧基、可具有取代基的苯甲酰基、可具有取代基的苯氧基羰基、可具有取代基的苯甲酰基氧基、可具有取代基的苯基烷基、可具有取代基的萘基、可具有取代基的萘氧基、可具有取代基的萘甲酰基、可具有取代基的萘氧基羰基、可具有取代基的萘甲酰基氧基、可具有取代基的萘基烷基、可具有取代基的杂环基、可具有取代基的杂环基羰基、被1个或2个有机基团取代的氨基、吗啉-1-基、哌嗪-1-基、卤素、硝基、氰基、包含hx2c-或h2xc-所示的基团的取代基(其中,x各自独立地为卤素原子)等。
[0285]rc5
为烷基的情况下,烷基的碳原子数优选为1以上20以下,更优选为1以上6以下。另外,r
c5
为烷基的情况下,可以为直链,也可以为支链。作为r
c5
为烷基的情况下的具体例,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、仲戊基、叔戊基、正己基、正庚基、正辛基、异辛基、仲辛基、叔辛基、正壬基、异壬基、正癸基、及异癸基等。另外,r
c5
为烷基的情况下,烷基可以在碳链中包含醚键(-o-)。作为在碳链中具有醚键的烷基的例子,可举出甲氧基乙基、乙氧基乙基、甲氧基乙氧基乙基、乙氧基乙氧基乙基、丙基氧基乙氧基乙基、及甲氧基丙基等。
[0286]rc5
为烷氧基的情况下,烷氧基的碳原子数优选为1以上20以下,更优选为1以上6以下。另外,r
c5
为烷氧基的情况下,可以为直链,也可以为支链。作为r
c5
为烷氧基的情况下的具体例,可举出甲氧基、乙氧基、正丙基氧基、异丙基氧基、正丁基氧基、异丁基氧基、仲丁基氧基、叔丁基氧基、正戊基氧基、异戊基氧基、仲戊基氧基、叔戊基氧基、正己基氧基、正庚基氧基、正辛基氧基、异辛基氧基、仲辛基氧基、叔辛基氧基、正壬基氧基、异壬基氧基、正癸基氧基、及异癸基氧基等。另外,r
c5
为烷氧基的情况下,烷氧基可以在碳链中包含醚键(-o-)。作为在碳链中具有醚键的烷氧基的例子,可举出甲氧基乙氧基、乙氧基乙氧基、甲氧基乙氧基乙氧基、乙氧基乙氧基乙氧基、丙基氧基乙氧基乙氧基、及甲氧基丙基氧基等。
[0287]rc5
为环烷基或环烷氧基的情况下,环烷基或环烷氧基的碳原子数优选为3以上10以下,更优选为3以上6以下。作为r
c5
为环烷基的情况下的具体例,可举出环丙基、环丁基、环戊基、环己基、环庚基、及环辛基等。作为r
c5
为环烷氧基的情况下的具体例,可举出环丙基氧基、环丁基氧基、环戊基氧基、环己基氧基、环庚基氧基、及环辛基氧基等。
[0288]rc5
为饱和脂肪族酰基或饱和脂肪族酰基氧基的情况下,饱和脂肪族酰基或饱和脂肪族酰基氧基的碳原子数优选为2以上21以下,更优选为2以上7以下。作为r
c5
为饱和脂肪族酰基的情况下的具体例,可举出乙酰基、丙酰基、正丁酰基、2-甲基丙酰基、正戊酰基、2,2-二甲基丙酰基、正己酰基、正庚酰基、正辛酰基、正壬酰基、正癸酰基、正十一烷酰基、正十二烷酰基、正十三烷酰基、正十四烷酰基、正十五烷酰基、及正十六烷酰基等。作为r
c5
为饱和脂
肪族酰基氧基的情况下的具体例,可举出乙酰基氧基、丙酰基氧基、正丁酰基氧基、2-甲基丙酰基氧基、正戊酰基氧基、2,2-二甲基丙酰基氧基、正己酰基氧基、正庚酰基氧基、正辛酰基氧基、正壬酰基氧基、正癸酰基氧基、正十一烷酰基氧基、正十二烷酰基氧基、正十三烷酰基氧基、正十四烷酰基氧基、正十五烷酰基氧基、及正十六烷酰基氧基等。
[0289]rc5
为烷氧基羰基的情况下,烷氧基羰基的碳原子数优选为2以上20以下,更优选为2以上7以下。作为r
c5
为烷氧基羰基的情况下的具体例,可举出甲氧基羰基、乙氧基羰基、正丙基氧基羰基、异丙基氧基羰基、正丁基氧基羰基、异丁基氧基羰基、仲丁基氧基羰基、叔丁基氧基羰基、正戊基氧基羰基、异戊基氧基羰基、仲戊基氧基羰基、叔戊基氧基羰基、正己基氧基羰基、正庚基氧基羰基、正辛基氧基羰基、异辛基氧基羰基、仲辛基氧基羰基、叔辛基氧基羰基、正壬基氧基羰基、异壬基氧基羰基、正癸基氧基羰基、及异癸基氧基羰基等。
[0290]rc5
为苯基烷基的情况下,苯基烷基的碳原子数优选为7以上20以下,更优选为7以上10以下。另外,r
c5
为萘基烷基的情况下,萘基烷基的碳原子数优选为11以上20以下,更优选为11以上14以下。作为r
c5
为苯基烷基的情况下的具体例,可举出苄基、2-苯基乙基、3-苯基丙基、及4-苯基丁基。作为r
c5
为萘基烷基的情况下的具体例,可举出α-萘基甲基、β-萘基甲基、2-(α-萘基)乙基、及2-(β-萘基)乙基。r
c5
为苯基烷基或萘基烷基的情况下,r
c5
可在苯基或萘基上进一步具有取代基。
[0291]rc5
为杂环基的情况下,杂环基与式(c3)中的r
c4
为杂环基的情况同样,杂环基可进一步具有取代基。
[0292]rc5
为杂环基羰基的情况下,杂环基羰基中包含的杂环基与r
c5
为杂环基的情况同样。
[0293]rc5
为被1个或2个有机基团取代的氨基的情况下,有机基团的优选例可举出碳原子数1以上20以下的烷基、碳原子数3以上10以下的环烷基、碳原子数2以上21以下的饱和脂肪族酰基、可具有取代基的苯基、可具有取代基的苯甲酰基、可具有取代基的碳原子数7以上20以下的苯基烷基、可具有取代基的萘基、可具有取代基的萘甲酰基、可具有取代基的碳原子数11以上20以下的萘基烷基、及杂环基等。这些优选的有机基团的具体例与r
c5
同样。作为被1个或2个有机基团取代的氨基的具体例,可举出甲基氨基、乙基氨基、二乙基氨基、正丙基氨基、二正丙基氨基、异丙基氨基、正丁基氨基、二正丁基氨基、正戊基氨基、正己基氨基、正庚基氨基、正辛基氨基、正壬基氨基、正癸基氨基、苯基氨基、萘基氨基、乙酰基氨基、丙酰基氨基、正丁酰基氨基、正戊酰基氨基、正己酰基氨基、正庚酰基氨基、正辛酰基氨基、正癸酰基氨基、苯甲酰基氨基、α-萘甲酰基氨基、及β-萘甲酰基氨基等。
[0294]
作为r
c5
中包含的苯基、萘基、及杂环基进一步具有取代基的情况下的取代基,可举出包含hx2c-或h2xc-所示的基团的取代基(例如,包含hx2c-或h2xc-所示的基团的卤代烷氧基、包含hx2c-或h2xc-所示的基团的卤代烷基)、碳原子数1以上6以下的烷基、碳原子数1以上6以下的烷氧基、碳原子数2以上7以下的饱和脂肪族酰基、碳原子数2以上7以下的烷氧基羰基、碳原子数2以上7以下的饱和脂肪族酰基氧基、具有碳原子数1以上6以下的烷基的单烷基氨基、具有碳原子数1以上6以下的烷基的二烷基氨基、吗啉-1-基、哌嗪-1-基、苯甲酰基、卤素、硝基、及氰基等。r
c5
中包含的苯基、萘基、及杂环基进一步具有取代基的情况下,该取代基的数目在不妨碍本发明的目的的范围内没有限定,优选为1以上4以下。r
c5
中包含的苯基、萘基、及杂环基具有多个取代基的情况下,多个取代基可以相同也可以不同。
[0295]
作为r
c5
中包含的苯甲酰基进一步具有取代基的情况下的取代基,可举出碳原子数1以上6以下的烷基、吗啉-1-基、哌嗪-1-基、2-噻吩甲酰基(噻吩-2-基羰基)、呋喃-3-基羰基及苯基等。
[0296]
作为x所示的卤素原子,可举出氟原子、氯原子、溴原子等,优选为氟原子。
[0297]
作为包含hx2c-或h2xc-所示的基团的取代基,可举出包含hx2c-或h2xc-所示的基团的卤代烷氧基、具有包含hx2c-或h2xc-所示的基团的卤代烷氧基的基团、包含hx2c-或h2xc-所示的基团的卤代烷基、具有包含hx2c-或h2xc-所示的基团的卤代烷基的基团等,更优选为包含hx2c-或h2xc-所示的基团的卤代烷氧基、或具有包含hx2c-或h2xc-所示的基团的卤代烷氧基的基团。
[0298]
作为具有包含hx2c-或h2xc-所示的基团的卤代烷基的基团,可举出被包含hx2c-或h2xc-所示的基团的卤代烷基取代的芳香族基团(例如,苯基、萘基等)、被包含hx2c-或h2xc-所示的基团的卤代烷基取代的环烷基(例如,环戊基、环己基等)等,优选为被包含hx2c-或h2xc-所示的基团的卤代烷基取代的芳香族基团。
[0299]
作为具有包含hx2c-或h2xc-所示的基团的卤代烷氧基的基团,可举出被包含hx2c-或h2xc-所示的基团的卤代烷氧基取代的芳香族基团(例如,苯基、萘基等)、被包含hx2c-或h2xc-所示的基团的卤代烷氧基取代的烷基(例如,甲基、乙基、正丙基、异丙基等)、被包含hx2c-或h2xc-所示的基团的卤代烷氧基取代的环烷基(例如,环戊基、环己基等)等,优选为被包含hx2c-或h2xc-所示的基团的卤代烷氧基取代的芳香族基团。
[0300]
另外,作为r
c5
,环烷基烷基、可在芳香环上具有取代基的苯氧基烷基、可在芳香环上具有取代基的苯基硫基烷基也是优选的。苯氧基烷基、及苯基硫基烷基可具有的取代基与r
c5
中包含的苯基可具有的取代基同样。
[0301]
1价有机基团中,作为r
c5
,优选为烷基、环烷基、可具有取代基的苯基、或环烷基烷基、可在芳香环上具有取代基的苯基硫基烷基。作为烷基,优选为碳原子数1以上20以下的烷基,更优选为碳原子数1以上8以下的烷基,特别优选为碳原子数1以上4以下的烷基,最优选为甲基。可具有取代基的苯基中,优选为甲基苯基,更优选为2-甲基苯基。环烷基烷基中包含的环烷基的碳原子数优选为5以上10以下,更优选为5以上8以下,特别优选为5或6。环烷基烷基中包含的亚烷基的碳原子数优选为1以上8以下,更优选为1以上4以下,特别优选为2。环烷基烷基中,优选为环戊基乙基。可在芳香环上具有取代基的苯基硫基烷基中包含的亚烷基的碳原子数优选为1以上8以下,更优选为1以上4以下,特别优选为2。可在芳香环上具有取代基的苯基硫基烷基中,优选为2-(4-氯苯基硫基)乙基。
[0302]
式(c3)所示的基团中,r
c5
存在有多个,多个r
c5
相互键合而形成环的情况下,作为所形成的环,可举出烃环、杂环等。作为杂环中包含的杂原子,例如,可举出n、o、s。作为多个r
c5
相互键合而形成的环,特别优选为芳香族环。所述芳香族环可以为芳香族烃环,也可以为芳香族杂环。作为所述芳香族环,优选为芳香族烃环。以下示出式(c3)中多个r
c5
相互键合而形成了苯环的情况下的具体例。
[0303]
[化学式19]
[0304][0305]
式(c4)所示的基团中,r
c8
为硝基或1价有机基团。r
c8
在式(c4)中的稠合环上键合于与-(co)
n1-所示的基团所键合的芳香环不同的6元芳香环上。式(c4)中,r
c8
的键合位置没有特别限定。式(c4)所示的基团具有1个以上的r
c8
的情况下,从式(c4)所示的化合物的合成容易进行等方面考虑,优选1个以上的r
c8
中的1个键合于芴骨架的7位的位置上。即,式(c4)所示的基团具有1个以上的r
c8
的情况下,式(c4)所示的基团优选由下述式(c6)表示。r
c8
为多个的情况下,多个r
c8
可以相同也可以不同。
[0306]
[化学式20]
[0307][0308]
(式(c6)中,r
c6
、r
c7
、r
c8
、n3分别与式(c4)中的r
c6
、r
c7
、r
c8
、n3同样。)
[0309]rc8
为1价有机基团的情况下,r
c8
在不妨碍本发明的目的的范围内没有特别限定。作为有机基团,优选为含有碳原子的基团,更优选为包含1个以上的碳原子、以及选自由h、o、s、se、n、b、p、si及卤素原子组成的组中的1个以上的原子的基团。含有碳原子的基团的碳原子数没有特别限定,优选为1以上50以下,更优选为1以上20以下。
[0310]
作为r
c8
为1价有机基团的情况下的优选例,可举出与作为式(c3)中的r
c5
的1价有机基团的优选例同样的基团。
[0311]
式(c4)中,r
c6
及r
c7
各自为可具有取代基的链状烷基、可具有取代基的链状烷氧基、可具有取代基的环状有机基团、或氢原子。r
c6
与r
c7
可以相互键合而形成环。这些基团中,作为r
c6
及r
c7
,优选为可具有取代基的链状烷基。r
c6
及r
c7
为可具有取代基的链状烷基的情况下,链状烷基可以为直链烷基,也可以为支链烷基。
[0312]rc6
及r
c7
为不具有取代基的链状烷基的情况下,链状烷基的碳原子数优选为1以上20以下,更优选为1以上10以下,特别优选为1以上6以下。作为r
c6
及r
c7
为链状烷基的情况下的具体例,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、仲戊基、叔戊基、正己基、正庚基、正辛基、异辛基、仲辛基、叔辛基、正壬基、异壬基、正癸基、及异癸基等。另外,r
c6
及r
c7
为烷基的情况下,烷基可以在碳链中包含醚键(-o-)。作为在碳链中具有醚键的烷基的例子,可举出甲氧基乙基、乙氧基乙基、甲氧基乙氧基乙基、乙氧基乙氧基乙基、丙基氧基乙氧基乙基、及甲氧基丙基等。
[0313]rc6
及r
c7
为具有取代基的链状烷基的情况下,链状烷基的碳原子数优选为1以上20以下,更优选为1以上10以下,特别优选为1以上6以下。在该情况下,链状烷基的碳原子数中不包括取代基的碳原子数。具有取代基的链状烷基优选为直链状。
[0314]
烷基可具有的取代基在不妨碍本发明的目的的范围内没有特别限定。作为取代基的优选例,可举出烷氧基、氰基、卤素原子、卤代烷基、环状有机基团、及烷氧基羰基。作为卤素原子,可举出氟原子、氯原子、溴原子、碘原子。它们之中,优选为氟原子、氯原子、溴原子。作为环状有机基团,可举出环烷基、芳香族烃基、杂环基。作为环烷基的具体例,与r
c8
为环烷基的情况下的优选例同样。作为芳香族烃基的具体例,可举出苯基、萘基、联苯基、蒽基、及菲基等。作为杂环基的具体例,与r
c8
为杂环基的情况下的优选例同样。r
c8
为烷氧基羰基的情况下,烷氧基羰基中包含的烷氧基可以为直链状,也可以为支链状,优选为直链状。烷氧基羰基中包含的烷氧基的碳原子数优选为1以上10以下,更优选为1以上6以下。
[0315]
链状烷基具有取代基的情况下,取代基的数目没有特别限定。优选的取代基的数目根据链状烷基的碳原子数而变化。典型地,取代基的数目为1以上20以下,优选为1以上10以下,更优选为1以上6以下。
[0316]rc6
及r
c7
为不具有取代基的链状烷氧基的情况下,链状烷氧基的碳原子数优选为1以上20以下,更优选为1以上10以下,特别优选为1以上6以下。作为r
c6
及r
c7
为链状烷氧基的情况下的具体例,可举出甲氧基、乙氧基、正丙基氧基、异丙基氧基、正丁基氧基、异丁基氧基、仲丁基氧基、叔丁基氧基、正戊基氧基、异戊基氧基、仲戊基氧基、叔戊基氧基、正己基氧基、正庚基氧基、正辛基氧基、异辛基氧基、仲辛基氧基、叔辛基氧基、正壬基氧基、异壬基氧基、正癸基氧基、及异癸基氧基等。另外,r
c6
及r
c7
为烷氧基的情况下,烷氧基可以在碳链中包含醚键(-o-)。作为在碳链中具有醚键的烷氧基的例子,可举出甲氧基乙氧基、乙氧基乙氧基、甲氧基乙氧基乙氧基、乙氧基乙氧基乙氧基、丙基氧基乙氧基乙氧基、及甲氧基丙基氧基等。
[0317]rc6
及r
c7
为具有取代基的链状烷氧基的情况下,烷氧基可具有的取代基与r
c6
及r
c7
为链状烷基的情况同样。
[0318]rc6
及r
c7
为环状有机基团的情况下,环状有机基团可以为脂环式基团,也可以为芳香族基团。作为环状有机基团,可举出脂肪族环状烃基、芳香族烃基、杂环基。r
c6
及r
c7
为环状有机基团的情况下,环状有机基团可具有的取代基与r
c6
及r
c7
为链状烷基的情况同样。
[0319]rc6
及r
c7
为芳香族烃基的情况下,优选地,芳香族烃基为苯基,或者为多个苯环介由碳-碳键进行键合而形成的基团,或者为多个苯环稠合而形成的基团。芳香族烃基为苯基、或者为多个苯环进行键合或稠合而形成的基团的情况下,芳香族烃基中包含的苯环的环数没有特别限定,优选为3以下,更优选为2以下,特别优选为1。作为芳香族烃基的优选的具体例,可举出苯基、萘基、联苯基、蒽基、及菲基等。
[0320]rc6
及r
c7
为脂肪族环状烃基的情况下,脂肪族环状烃基可以为单环式,也可以为多环式。脂肪族环状烃基的碳原子数没有特别限定,但优选为3以上20以下,更优选为3以上10以下。作为单环式的环状烃基的例子,可举出环丙基、环丁基、环戊基、环己基、环庚基、环辛基、降冰片基、异冰片基、三环壬基、三环癸基、四环十二烷基(tetracyclododecyl)、及金刚烷基等。
[0321]rc6
及r
c7
为杂环基的情况下,可举出与作为式(c3)中的r
c5
的杂环基同样的基团。
[0322]rc6
与r
c7
可以相互键合而形成环。包含r
c6
与r
c7
所形成的环的基团优选为环烷叉基(cycloalkylidene group)。r
c6
与r
c7
键合而形成环烷叉基的情况下,构成环烷叉基的环优选为5元环~6元环,更优选为5元环。
[0323]rc7
与芴骨架的苯环形成环的情况下,该环可以为芳香族环,也可以为脂肪族环。
[0324]rc6
与r
c7
键合而形成的基团为环烷叉基的情况下,环烷叉基可以与1个以上的其他环稠合。作为可与环烷叉基稠合的环的例子,可举出苯环、萘环、环丁烷环、环戊烷环、环己烷环、环庚烷环、环辛烷环、呋喃环、噻吩环、吡咯环、吡啶环、吡嗪环、及嘧啶环等。
[0325]
以上说明的r
c6
及r
c7
中,作为优选的基团的例子,可举出式-a1-a2所示的基团。式中,a1为直链亚烷基,a2为烷氧基、氰基、卤素原子、卤代烷基、环状有机基团、或烷氧基羰基。
[0326]
a1的直链亚烷基的碳原子数优选为1以上10以下,更优选为1以上6以下。a2为烷氧基的情况下,烷氧基可以为直链状,也可以为支链状,优选为直链状。烷氧基的碳原子数优选为1以上10以下,更优选为1以上6以下。a2为卤素原子的情况下,优选为氟原子、氯原子、溴原子、碘原子,更优选为氟原子、氯原子、溴原子。a2为卤代烷基的情况下,卤代烷基中包含的卤素原子优选为氟原子、氯原子、溴原子、碘原子,更优选为氟原子、氯原子、溴原子。卤代烷基可以为直链状,也可以为支链状,优选为直链状。a2为环状有机基团的情况下,环状有机基团的例子与r
c6
及r
c7
作为取代基而具有的环状有机基团同样。a2为烷氧基羰基的情况下,烷氧基羰基的例子与r
c6
及r
c7
作为取代基而具有的烷氧基羰基同样。
[0327]
作为r
c6
及r
c7
的优选的具体例,可举出乙基、正丙基、正丁基、正己基、正庚基、及正辛基等烷基;2-甲氧基乙基、3-甲氧基正丙基、4-甲氧基正丁基、5-甲氧基正戊基、6-甲氧基正己基、7-甲氧基正庚基、8-甲氧基正辛基、2-乙氧基乙基、3-乙氧基正丙基、4-乙氧基正丁基、5-乙氧基正戊基、6-乙氧基正己基、7-乙氧基正庚基、及8-乙氧基正辛基等烷氧基烷基;2-氰基乙基、3-氰基正丙基、4-氰基正丁基、5-氰基正戊基、6-氰基正己基、7-氰基正庚基、及8-氰基正辛基等氰基烷基;2-苯基乙基、3-苯基正丙基、4-苯基正丁基、5-苯基正戊基、6-苯基正己基、7-苯基正庚基、及8-苯基正辛基等苯基烷基;2-环己基乙基、3-环己基正丙基、4-环己基正丁基、5-环己基正戊基、6-环己基正己基、7-环己基正庚基、8-环己基正辛基、2-环戊基乙基、3-环戊基正丙基、4-环戊基正丁基、5-环戊基正戊基、6-环戊基正己基、7-环戊基正庚基、及8-环戊基正辛基等环烷基烷基;2-甲氧基羰基乙基、3-甲氧基羰基正丙基、4-甲氧基羰基正丁基、5-甲氧基羰基正戊基、6-甲氧基羰基正己基、7-甲氧基羰基正庚基、8-甲氧基羰基正辛基、2-乙氧基羰基乙基、3-乙氧基羰基正丙基、4-乙氧基羰基正丁基、5-乙氧基羰基正戊基、6-乙氧基羰基正己基、7-乙氧基羰基正庚基、及8-乙氧基羰基正辛基等烷氧基羰基烷基;2-氯乙基、3-氯正丙基、4-氯正丁基、5-氯正戊基、6-氯正己基、7-氯正庚基、8-氯正辛基、2-溴乙基、3-溴正丙基、4-溴正丁基、5-溴正戊基、6-溴正己基、7-溴正庚基、8-溴正辛基、3,3,3-三氟丙基、及3,3,4,4,5,5,5-七氟正戊基等卤代烷基。
[0328]
作为r
c6
及r
c7
,上述中优选的基团为乙基、正丙基、正丁基、正戊基、2-甲氧基乙基、2-氰基乙基、2-苯基乙基、2-环己基乙基、2-甲氧基羰基乙基、2-氯乙基、2-溴乙基、3,3,3-三氟丙基、及3,3,4,4,5,5,5-七氟正戊基。
[0329]
式(c5)中,从容易得到灵敏度优异的光聚合引发剂的方面考虑,a特别优选为s。
[0330]
式(c5)中,r
c9
为1价有机基团、卤素原子、硝基、或氰基。
[0331]
式(c5)中的r
c9
为1价有机基团的情况下,可以在不妨碍本发明的目的的范围内从各种有机基团中选择。作为有机基团,优选为含有碳原子的基团,更优选为包含1个以上的碳原子、以及选自由h、o、s、se、n、b、p、si及卤素原子组成的组中的1个以上的原子的基团。
含有碳原子的基团的碳原子数没有特别限定,优选为1以上50以下,更优选为1以上20以下。
[0332]
作为式(c5)中r
c9
为有机基团的情况下的优选例,可举出与作为式(c3)中的r
c5
的1价有机基团同样的基团。
[0333]rc9
中,优选为苯甲酰基;萘甲酰基;被选自由碳原子数1以上6以下的烷基、吗啉-1-基、哌嗪-1-基、及苯基组成的组中的基团取代的苯甲酰基;硝基;可具有取代基的苯并呋喃基羰基,更优选为苯甲酰基;萘甲酰基;2-甲基苯基羰基;4-(哌嗪-1-基)苯基羰基;4-(苯基)苯基羰基。
[0334]
另外,式(c5)中,n4优选为0以上3以下的整数,更优选为0以上2以下的整数,特别优选为0或1。n4为1的情况下,r
c9
的键合位置优选相对于r
c9
所键合的苯基与氧原子或硫原子进行键合的化学键而言为对位。
[0335]
式(c1)及(c2)中,作为r
c2
的1价有机基团在不妨碍本发明的目的的范围内没有特别限定。作为有机基团,优选为含有碳原子的基团,更优选为包含1个以上的碳原子、以及选自由h、o、s、se、n、b、p、si及卤素原子组成的组中的1个以上的原子的基团。含有碳原子的基团的碳原子数没有特别限定,优选为1以上50以下,更优选为1以上20以下。
[0336]
关于作为r
c2
的1价有机基团的优选例,可举出与作为式(c3)中的r
c5
的1价有机基团同样的基团。这些基团的具体例与针对式(c3)中的r
c5
而说明的基团同样。
[0337]
另外,作为r
c2
,环烷基烷基、可在芳香环上具有取代基的苯氧基烷基、可在芳香环上具有取代基的苯基硫基烷基也是优选的。苯氧基烷基、及苯基硫基烷基可具有的取代基与式(c3)中的r
c5
中包含的苯基、萘基、及杂环基进一步具有取代基的情况下的取代基同样。
[0338]
有机基团中,作为r
c2
,优选为上述包含hx2c-或h2xc-所示的基团的取代基、烷基、环烷基、可具有取代基的苯基、或环烷基烷基、可在芳香环上具有取代基的苯基硫基烷基。关于烷基、可具有取代基的苯基、环烷基烷基中包含的环烷基的碳原子数、环烷基烷基中包含的亚烷基的碳原子数、环烷基烷基、可在芳香环上具有取代基的苯基硫基烷基中包含的亚烷基的碳原子数、或可在芳香环上具有取代基的苯基硫基烷基,与式(c3)的r
c5
同样。
[0339]
另外,作为r
c2
,-a3-co-o-a4所示的基团也是优选的。a3为2价有机基团,优选为2价烃基,优选为亚烷基。a4为1价有机基团,优选为1价烃基。
[0340]
a3为亚烷基的情况下,亚烷基可以为直链状,也可以为支链状,优选为直链状。a3为亚烷基的情况下,亚烷基的碳原子数优选为1以上10以下,更优选为1以上6以下,特别优选为1以上4以下。
[0341]
作为a4的优选例,可举出碳原子数1以上10以下的烷基、碳原子数7以上20以下的芳烷基、及碳原子数6以上20以下的芳香族烃基。作为a4的优选的具体例,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、苯基、萘基、苄基、苯乙基、α-萘基甲基、及β-萘基甲基等。
[0342]
作为-a3-co-o-a4所示的基团的优选的具体例,可举出2-甲氧基羰基乙基、2-乙氧基羰基乙基、2-正丙基氧基羰基乙基、2-正丁基氧基羰基乙基、2-正戊基氧基羰基乙基、2-正己基氧基羰基乙基、2-苄基氧基羰基乙基、2-苯氧基羰基乙基、3-甲氧基羰基正丙基、3-乙氧基羰基正丙基、3-正丙基氧基羰基正丙基、3-正丁基氧基羰基正丙基、3-正戊基氧基羰基正丙基、3-正己基氧基羰基正丙基、3-苄基氧基羰基正丙基、及3-苯氧基羰基正丙基等。
[0343]
另外,作为r
c2
,下述式(c7)或(c8)所示的基团也是优选的。
[0344]
[化学式21]
[0345][0346]
(式(c7)及(c8)中,r
c10
及r
c11
各自独立地为1价有机基团,
[0347]
n5为0以上4以下的整数,
[0348]rc10
及r
c11
存在于苯环上的相邻位置的情况下,r
c10
与r
c11
可以相互键合而形成环,
[0349]rc12
为1价有机基团,
[0350]
n6为1以下8以下的整数,
[0351]
n7为1以上5以下的整数,
[0352]
n8为0以上且(n7 3)以下的整数。)
[0353]
作为式(c7)中的r
c10
及r
c11
的有机基团与式(c4)中的r
c8
同样。作为r
c10
,优选为包含hx2c-或h2xc-所示的基团的卤代烷氧基、包含hx2c-或h2xc-所示的基团的卤代烷基、烷基或苯基。r
c10
与r
c11
键合而形成环的情况下,该环可以为芳香族环,也可以为脂肪族环。关于作为式(c7)所示的基团的、r
c10
与r
c11
形成了环的基团的优选例,可举出萘-1-基、1,2,3,4-四氢萘-5-基等。
[0354]
上述式(c7)中,n7为0以上4以下的整数,优选为0或1,更优选为0。
[0355]
上述式(c8)中,r
c12
为有机基团。作为有机基团,可举出与针对式(c4)中的r
c8
而说明的有机基团同样的基团。有机基团中,优选为烷基。烷基可以为直链状,也可以为支链状。烷基的碳原子数优选为1以上10以下,更优选为1以上5以下,特别优选为1以上3以下。作为r
c12
,可优选例示甲基、乙基、丙基、异丙基、丁基等,它们之中,更优选为甲基。
[0356]
上述式(c8)中,n7为1以上5以下的整数,优选为1以上3以下的整数,更优选为1或2。上述式(c8)中,n8为0以上且(n7 3)以下,优选为0以上3以下的整数,更优选为0以上2以下的整数,特别优选为0。
[0357]
上述式(c8)中,n8为1以上8以下的整数,优选为1以上5以下的整数,更优选为1以上3以下的整数,特别优选为1或2。
[0358]
式(c2)中,r
c3
为氢原子、可具有取代基的碳原子数1以上20以下的脂肪族烃基、或可具有取代基的芳基。作为r
c3
为脂肪族烃基时可具有的取代基,可优选例示苯基、萘基等。
[0359]
式(c1)及(c2)中,作为r
c3
,可优选例示氢原子、甲基、乙基、正丙基、异丙基、正丁基、2-环戊基乙基、2-环丁基乙基、环己基甲基、苯基、苄基、甲基苯基、萘基等,它们之中,更优选为甲基或苯基。
[0360]
作为由式(c2)表示、并且具有式(c3)所示的基团作为r
c1
的化合物的优选的具体例,可举出以下的化合物。
[0361]
[化学式22]
[0362][0363]
[化学式23]
[0364][0365]
[化学式24]
[0366][0367]
[化学式25]
[0368][0369]
作为由式(c2)表示、并且具有式(c4)所示的基团作为r
c1
的化合物的优选的具体例,可举出以下的化合物。
[0370]
[化学式26]
[0371][0372]
[化学式27]
[0373][0374]
[化学式28]
[0375][0376]
[化学式29]
[0377][0378]
[化学式30]
[0379]
[0380]
作为由式(c2)表示、并且具有式(c5)所示的基团作为r
c1
的化合物的优选的具体例,可举出以下的化合物。
[0381]
[化学式31]
[0382][0383]
作为肟酯化合物以外的光聚合引发剂(c),可例示2-苄基-2-二甲基氨基-1-(4-吗啉代苯基)丁烷-1-酮、2-甲基-1-[4-(甲基硫基)苯基]-2-吗啉代丙烷-1-酮、2-苄基-2-二甲基氨基-1-(4-二甲基氨基苯基)丁烷-1-酮、2-(4-甲基苄基)-2-二乙基氨基-1-(4-吗啉代苯基)丁烷-1-酮、2-甲基-1-苯基-2-吗啉代丙烷-1-酮、2-甲基-1-[4-(己基)苯基]-2-吗啉代丙烷-1-酮、2-乙基-2-二甲基氨基-1-(4-吗啉代苯基)丁烷-1-酮等α-氨基酮系化合物;1-苯基-2-羟基-2-甲基丙烷-1-酮、1-(4-异丙基苯基)-2-羟基-2-甲基丙烷-1-酮、4-(2-羟基乙氧基)苯基-(2-羟基-2-丙基)酮、1-羟基环己基苯基酮等α-羟基酮系光聚合引发剂;苯偶姻、苯偶姻甲基醚、苯偶姻乙基醚、苯偶姻丙基醚、联苯酰缩二甲醇(benzil methyl ketal)等苯偶姻系光聚合引发剂;二苯甲酮、苯甲酰基苯甲酸、苯甲酰基苯甲酸甲酯、4-苯基二苯甲酮、羟基二苯甲酮、丙烯酸化二苯甲酮、4-苯甲酰4
’‑
甲基二苯基硫醚(4-benzoyl 4
’‑
methyldiphenyl sulfide)、4,4
’‑
双二乙基氨基二苯甲酮等二苯甲酮系光聚合引发剂;噻吨酮、2-氯噻吨酮、2-甲基噻吨酮、异丙基噻吨酮、2,4-二异丙基噻吨酮等噻吨酮系光聚合引发剂;2,4,6-三氯均三嗪、2-苯基-4,6-双(三氯甲基)均三嗪、2-(对甲氧基苯基)-4,6-双(三氯甲基)均三嗪、2-(对甲苯基)-4,6-双(三氯甲基)均三嗪、2-胡椒基-4,6-双(三氯甲基)均三嗪、2,4-双(三氯甲基)-6-苯乙烯基均三嗪、2-(萘-1-基)-4,6-双(三氯甲基)均三嗪、2-(4-甲氧基-萘-1-基)-4,6-双(三氯甲基)均三嗪、2,4-三氯甲基-(胡椒基)-6-三嗪、2,4-三氯甲基-(4
’‑
甲氧基苯乙烯基)-6-三嗪、2-[4-(4-甲氧基苯乙烯基)苯基]-4,6-双(三氯甲基)-1,3,5-三嗪等三嗪系光聚合引发剂;咔唑系光聚合引发剂;2,2
’‑
双(2-氯苯基)-4,4’,5,5
’‑
四(4-乙氧基羰基苯基)-1,2
’‑
联咪唑、2,2
’‑
双(2-溴苯基)-4,4’,5,5
’‑
四(4-乙氧基羰基苯基)-1,2
’‑
联咪唑、2,2
’‑
双(2-氯苯基)-4,4’,5,5
’‑
四苯基-1,2
’‑
联咪
唑、2,2
’‑
双(2,4-二氯苯基)-4,4’,5,5
’‑
四苯基-1,2
’‑
联咪唑、2,2
’‑
双(2,4,6-三氯苯基)-4,4’,5,5
’‑
四苯基-1,2
’‑
联咪唑、2,2
’‑
双(2-溴苯基)-4,4,5,5
’‑
四苯基-1,2
’‑
联咪唑、2,2
’‑
双(2,4-二溴苯基)-4,4’,5,5
’‑
四苯基-1,2
’‑
联咪唑、2,2
’‑
双(2,4,6-三溴苯基)-4,4’,5,5
’‑
四苯基-1,2
’‑
联咪唑等联咪唑系光聚合引发剂;下式所示的这样的苯并咪唑啉系光聚合引发剂等。
[0384]
[化学式32]
[0385][0386]
光聚合引发剂可以单独使用或者组合2种以上而使用。通过组合2种以上而使用,从而容易有效地利用曝光用光中包含的宽范围的波长的光线,另外,容易将负型感光性树脂组合物的灵敏度调整至合适的范围。
[0387]
负型感光性树脂组合物的全部固态成分中的、光聚合引发剂(c)的含量优选为0.5质量%以上15质量%以下,更优选为1质量%以上10质量%以下。
[0388]
并用肟酯化合物以外的其他光聚合引发剂的情况下,肟酯化合物的质量相对于光聚合引发剂(c)的质量而言的比率优选为50质量%以上,更优选为50质量%以上99质量%以下,特别优选为70质量%以上97质量%以下,最优选为80质量%以上95质量%以下。
[0389]
相对于负型感光性树脂组合物的固态成分的合计100质量份而言,光聚合引发剂(c)的含量优选为0.001质量份以上30质量份以下,更优选为0.1质量份以上20质量份以下,进一步优选为0.5质量份以上10质量份以下。需要说明的是,所谓固态成分,是除溶剂(s)以外的成分。
[0390]
另外,相对于感光性树脂(a)与光聚合引发剂(c)的总和而言,光聚合引发剂(c)的含量优选为0.1质量%以上50质量%以下,更优选为0.5质量%以上30质量%以下,进一步优选为0.5质量%以上10质量%以下。
[0391]
<密合增强剂(d)>
[0392]
负型感光性树脂组合物可以包含或不包含密合增强剂(d)。
[0393]
密合增强剂(d)为具有提高与基板的粘接力的作用的成分,例如,优选为具有羧基、(甲基)丙烯酰基、乙烯基、异氰酸酯基、环氧基、巯基等反应性官能团的硅烷偶联剂。具体而言,例如,为选自三甲氧基甲硅烷基苯甲酸、3-((甲基)丙烯酰基氧基)丙基三甲氧基硅烷、乙烯基三乙酰氧基硅烷、乙烯基三甲氧基硅烷、(3-异氰酸酯基丙基)三乙氧基硅烷、3-环氧丙氧基丙基三甲氧基硅烷、3-环氧丙氧基丙基甲基二甲氧基硅烷及2-(3,4-环氧环己基)乙基三甲氧基硅烷中的一种或两种以上。
[0394]
作为密合增强剂(d),尽管与上述硅烷偶联剂一部分重复,可举出异氰酸酯系化合物、环氧系化合物、(甲基)丙烯酸酯系化合物、乙烯基化合物、巯基系化合物,更优选为环氧系化合物。作为环氧系化合物,例如,可举出具有环氧基的有机硅烷化合物,作为更具体的例子,可举出具有环氧基的碳原子数1以上5以下的烷氧基硅烷。
[0395]
相对于感光性树脂(a)与光聚合性化合物(b)的总和而言,密合增强剂(d)的含量优选为0.1质量%以上50质量%以下,更优选为0.5质量%以上30质量%以下,进一步优选
为0.5质量%以上10质量%以下。在该范围内时,具有与基板的粘接力优异的效果。
[0396]
<溶剂(s)>
[0397]
负型感光性树脂组合物可以包含或不包含溶剂(s)。
[0398]
作为溶剂(s),可举出有机溶剂、水。作为有机溶剂,只要是可溶解感光性树脂(a)的、通常的负型感光性树脂组合物中使用的乙酸酯系、醚系、二醇系、酮系、醇系及碳酸酯系等的有机溶剂即可,没有特别限定。作为有机溶剂,例如,可举出丙二醇单甲基醚乙酸酯(pegmea)、乙基溶纤剂、丁基溶纤剂、乙基卡必醇、丁基卡必醇、乙基卡必醇乙酸酯、丁基卡必醇乙酸酯、乙二醇、环己酮、环戊酮、3-乙氧基丙酸、n,n-二甲基乙酰胺、n-甲基吡咯烷酮(nmp)、n-甲基己内酰胺等。
[0399]
相对于负型感光性树脂组合物100质量份而言,溶剂(s)的含量例如优选为20质量份以上95质量份以下,更优选为30质量份以上90质量份以下,进一步优选为50质量份以上80质量份以下。在该范围内时,使用现有的涂覆方法也容易形成薄膜,涂覆后能够容易地得到所期望厚度的薄膜。
[0400]
<其他成分>
[0401]
负型感光性树脂组合物可以根据需要而包含添加剂。作为这样的添加剂的例子,有稳定剂、热交联剂、光固化促进剂、表面活性剂、碱淬灭剂、抗氧化剂、粘接助剂、消泡剂等,可以根据需要而单独使用或者混合使用。
[0402]
表面活性剂为具有提高对基板的涂覆性和涂布性、均匀性及污垢除去性的作用的成分。作为表面活性剂,例如,可举出氟系表面活性剂、硅系表面活性剂、非离子系表面活性剂,优选为硅系表面活性剂。作为硅系表面活性剂,例如,可举出聚醚改性聚硅氧烷,作为更具体的例子,可举出聚醚改性聚二甲基硅氧烷。
[0403]
以感光性树脂(a)100质量份为基准,表面活性剂的含量的优选范围为0.01质量份以上5质量份以下、0.02质量份以上1质量份以下、或0.05质量份以上0.1质量份以下。
[0404]
作为稳定剂,例如,可举出热稳定剂、光稳定剂。
[0405]
热稳定剂可以使用通常负型感光性树脂组合物中能够使用的热稳定剂,没有特别限定,例如,可举出能够对所形成的固化物(有机膜)在后热处理工序中透过度的降低进行抑制、提高残留有机膜的透过度的热稳定剂。作为热稳定剂,可举出酚系热稳定剂、亚磷酸酯系热稳定剂、内酯系热稳定剂。作为优选的热稳定剂,例如,可举出下述式(4)~(6)所示的化合物。
[0406]
[化学式33]
[0407][0408]
[化学式34]
[0409][0410]
[化学式35]
[0411][0412]
光稳定剂可以使用通常负型感光性树脂组合物中能够使用的光稳定剂,例如,可举出能够使所形成的固化物(例如有机绝缘膜)的耐光性最大化的光稳定剂。作为光稳定剂,可举出苯并三唑系光稳定剂、三嗪系光稳定剂、二苯甲酮系光稳定剂、受阻氨基醚系光稳定剂、受阻胺系光稳定剂。
[0413]
《负型感光性树脂组合物的制造方法》
[0414]
上述负型感光性树脂组合物可以利用通常的方法来制造,例如,可以通过将上述的各成分混合、并根据需要使用过滤器进行过滤从而制造。
[0415]
《固化膜的制造方法》
[0416]
使用上述负型感光性树脂组合物,能够制造可在tft-lcd、oled、触摸屏面板等显示器、搭载于图像传感器上的微透镜、光波导等光学构件等中使用的固化膜(固化物)。所制造的固化膜可以根据需要图案化。
[0417]
以下,对使用上述负型感光性树脂组合物来制造经图案化的固化膜的方法进行说明。
[0418]
首先,将上述负型感光性树脂组合物涂布于基板上从而形成涂布膜。
[0419]
形成涂布膜的基板没有特别限定,可以使用以往已知的基板,例如,可举出硅基板、玻璃基板、具有金属表面的基板。作为构成金属表面的金属种类,优选为铜、金、铝,更优选为铜。
[0420]
上述负型感光性树脂组合物的涂布方法没有特别限定,可以使用已知的方法。例如,可举出旋涂、浸涂、辊涂、丝网涂覆、喷涂、流涂、丝网印刷、喷墨、液滴涂布(drop-casting)等涂覆方法。
[0421]
所形成的涂布膜的膜厚根据涂布方法、负型感光性树脂组合物的固态成分的浓度、粘度等而变化,没有特别限定,通常可以以干燥后膜厚为0.5μm以上100μm以下的方式进行涂布。
[0422]
可以根据需要使涂布膜干燥。干燥方法没有特别限定,可举出通过真空、红外线照射、加热而使溶剂挥发的方法。
[0423]
接下来,以位置选择性方式对涂布膜进行曝光。位置选择性的曝光例如隔着负型的掩模进行。通过进行位置选择性的曝光,能够形成经图案化的固化膜。
[0424]
曝光中,将准分子激光、远紫外线、紫外线、可见光、电子射线、x射线或g线(波长
436nm)、i线(波长365nm)、h线(波长405nm)或它们的混合光线等能量射线以位置选择性方式照射至涂布膜。曝光中,可以使用接触式、接近式、投影式等的曝光法等。
[0425]
照射的能量射线量也根据负型感光性树脂组合物的组成而不同,例如为140mj/cm2以下,优选为5mj/cm2以上100mj/cm2以下,更优选为10mj/cm2以上60mj/cm2以下。
[0426]
通过对涂布膜进行曝光,从而发生固化反应。
[0427]
接下来,利用显影液对曝光后的涂布膜进行显影,由此能够得到被图案化为所期望的形状的固化膜。
[0428]
显影方法没有特别限定,例如,可以使用浸渍法、喷雾法等。
[0429]
显影液根据负型感光性树脂组合物的组成而适当地选择。作为显影液,可以使用碱性水溶液,其较有机溶剂而言更环保且廉价。作为碱性显影液,可举出四甲基氢氧化铵(tmah)、四乙基氢氧化铵等氢氧化季铵的水溶液、氨、乙胺、丙胺、二乙胺、三乙胺等胺系水溶液。
[0430]
可以对曝光后的涂布膜进行加热(曝光后烘烤(peb)或后烘烤)。加热温度没有特别限定,例如为80℃以上250℃以下,优选为80℃以上200℃以下,更优选为80℃以上150℃以下,进一步优选为85℃以上110℃以下。
[0431]
优选进行曝光后烘烤(peb),其为在对涂布膜进行曝光的工序之后、且在进行显影的工序之前实施的加热。
[0432]
利用上述制造方法制造的固化膜(固化物)由于是使用上述负型感光性树脂组合物形成的,因此具有高折射率和高透明性。因此,使用上述负型感光性树脂组合物形成的固化膜可以用作要求高折射率及高透明性的构件。
[0433]
另外,上述负型感光性树脂组合物具有高耐溶剂性,因此,对丙二醇单甲基醚乙酸酯(pegmea)等有机溶剂具有高耐性。因此,适合用于下述用途:使用在溶剂中溶解树脂等成分而得到的组合物,在上述固化膜上形成其他层从而制造层叠材料的用途;对上述固化膜应用包含溶剂的粘接剂的用途。
[0434]
这样的经图案化的固化膜能够应用于例如半导体元件、lcd用元件、oled用元件、太阳能电池用元件、柔性显示器用元件、触摸屏制造用元件或纳米压印光刻用元件等元件的制作、涂覆材料、搭载于图像传感器上的微透镜、光波导等光学构件等各种用途。
[0435]
实施例
[0436]
以下,利用实施例来更详细地说明本发明,但本发明不限于这些实施例。
[0437]
<化合物a(3,3
’‑
(((9h-芴-9,9-二基)双(4,1-萘基))双(氧基))双(1-(苯基硫基)丙-2-醇)的合成>
[0438]
[化学式36]
[0439][0440]
在三颈瓶上设置回流冷凝器和温度计后,装入2,2
’‑
((((9h-芴-9,9-二基)双(4,1-萘基))双(氧基))双(亚甲基))双(环氧乙烷)(1000g)、苯硫酚524g、乙醇617g并搅拌。向反应溶液中缓缓滴加三乙胺328g。利用高效液相色谱(hplc)法确认了起始物质消失后,结束反应。反应完成后,将乙醇减压蒸馏而除去。将有机物溶解于二氯甲烷,然后用水洗涤,然后通过减压蒸馏将二氯甲烷除去。经浓缩的有机物在乙酸乙酯中进行重结晶,以淡黄色固体的形态得到化合物a 945g(收率64%),其结构通过1hnmr进行了确认。
[0441]
cdcl3中的1h nmr:6.98~7.84(30h),4.19(4h),4.00(2h),2.92(4h),2.21(2h)。
[0442]
<含有羧基的树脂的制造>
[0443]
[合成例1]含有羧基的树脂a-1(具有r
3a
为下述4价基团的、式(a1)所示的结构单元的含有羧基的树脂)的制造
[0444]
[化学式37]
[0445][0446]
在三颈瓶上设置回流管和温度计后,装入10g化合物a、2.79g均苯四甲酸酐、30g丙二醇甲基醚乙酸酯,于115℃进行10小时加热搅拌,结束反应。将其冷却,由此得到质均分子量为5,200g/mol的含有羧基的树脂a-1的溶液。
[0447]
[合成例2]含有羧基的树脂a-2(具有r
3a
为下述4价基团的、式(a1)所示的结构单元的含有羧基的树脂)的制造
[0448]
[化学式38]
[0449][0450]
在三颈瓶上设置回流管和温度计后,装入10g化合物a、3.76g的4,4
’‑
二邻苯二甲酸酐(4,4
’‑
biphthalic anhydride)、30g丙二醇甲基醚乙酸酯,于115℃进行10小时加热搅拌,结束反应。将其冷却,由此得到质均分子量为3,500g/mol的含有羧基的树脂a-2的溶液。
[0451]
[合成例3]含有羧基的树脂a-3(具有r
3a
为下述4价基团的、式(a1)所示的结构单元的含有羧基的树脂)的制造
[0452]
[化学式39]
[0453][0454]
在三颈瓶上设置回流管和温度计后,装入10g化合物a、4.12g的3,3’,4,4
’‑
二苯甲酮四甲酸二酐、30g丙二醇甲基醚乙酸酯,于115℃进行10小时加热搅拌,结束反应。将其冷却,由此得到质均分子量为4,800g/mol的含有羧基的树脂a-3的溶液。
[0455]
[合成例4]含有羧基的树脂a-4(具有r
3a
为下述4价基团的、式(a1)所示的结构单元的含有羧基的树脂)的制造
[0456]
[化学式40]
[0457][0458]
在三颈瓶上设置回流管和温度计后,装入10g化合物a、4.91g的1,4-双(3,4-二羧基苯氧基)苯二酐、30g丙二醇甲基醚乙酸酯,于115℃进行10小时加热搅拌,结束反应。将其冷却,由此得到质均分子量为2,200g/mol的含有羧基的树脂a-4的溶液。
[0459]
[合成例5]含有羧基的树脂a-5(具有r
3a
为下述4价基团的、式(a1)所示的结构单元的含有羧基的树脂)的制造
[0460]
[化学式41]
[0461][0462]
在三颈瓶上设置回流管和温度计后,装入10g化合物a、3.96g的4,4
’‑
氧二邻苯二甲酸酐、30g丙二醇甲基醚乙酸酯,于115℃进行10小时加热搅拌,结束反应。将其冷却,由此得到质均分子量为2,800g/mol的含有羧基的树脂a-5的溶液。
[0463]
[比较合成例1]
[0464]
按照专利文献4(日本特表2018-531311号公报)中记载的制造例1,得到含有羧基的树脂a-6(其为具有r
3a
为下述4价基团的、式(a1)所示的结构单元的含有羧基的树脂,并且,式(a2)中的z1及z2为苯环,k1、k2、m1及m2为0)的溶液。
[0465]
[化学式42]
[0466][0467]
<感光性树脂的制造>
[0468]
[合成例6]感光性树脂a-1的制造
[0469]
于室温向合成例1中得到的含有羧基的树脂a-1的溶液中加入甲基丙烯酸缩水甘油酯0.45g,于95℃进行2小时搅拌。需要说明的是,相对于合成例1中使用的化合物a1摩尔而言,添加0.25摩尔甲基丙烯酸缩水甘油酯。接着冷却至室温,以固态成分(不挥发成分)浓度成为30质量%的方式加入丙二醇单甲基醚乙酸酯,得到质均分子量为5,600g/mol的感光性树脂a-1的溶液。通过测定固态成分酸值而确认了加成有甲基丙烯酸缩水甘油酯。
[0470]
[合成例7]感光性树脂a-2的制造
[0471]
于室温向合成例2中得到的含有羧基的树脂a-2的溶液中加入甲基丙烯酸缩水甘油酯0.45g,于95℃进行2小时搅拌。需要说明的是,相对于合成例2中使用的化合物a1摩尔而言,添加0.25摩尔甲基丙烯酸缩水甘油酯。接着冷却至室温,以固态成分(不挥发成分)浓度成为30质量%的方式加入丙二醇单甲基醚乙酸酯,得到质均分子量为3,700g/mol的感光性树脂a-2的溶液。通过测定固态成分酸值而确认了加成有甲基丙烯酸缩水甘油酯。
[0472]
[合成例8]感光性树脂a-3的制造
[0473]
于室温向合成例3中得到的含有羧基的树脂a-3的溶液中加入甲基丙烯酸缩水甘油酯0.45g,于95℃进行2小时搅拌。需要说明的是,相对于合成例3中使用的化合物a1摩尔而言,添加0.25摩尔甲基丙烯酸缩水甘油酯。接着冷却至室温,以固态成分(不挥发成分)浓度成为30质量%的方式加入丙二醇单甲基醚乙酸酯,得到质均分子量为5100g/mol的感光性树脂a-3的溶液。通过测定固态成分酸值而确认了加成有甲基丙烯酸缩水甘油酯。
[0474]
[合成例9]感光性树脂a-4的制造
[0475]
于室温向合成例4中得到的含有羧基的树脂a-4的溶液中加入甲基丙烯酸缩水甘油酯0.45g,于95℃进行2小时搅拌。需要说明的是,相对于合成例4中使用的化合物a1摩尔而言,添加0.25摩尔甲基丙烯酸缩水甘油酯。接着冷却至室温,以固态成分(不挥发成分)浓度成为30质量%的方式加入丙二醇单甲基醚乙酸酯,得到质均分子量为2400g/mol的感光性树脂a-4的溶液。通过测定固态成分酸值而确认了加成有甲基丙烯酸缩水甘油酯。
[0476]
[合成例10]感光性树脂a-5的制造
[0477]
于室温向合成例5中得到的含有羧基的树脂a-5的溶液中加入甲基丙烯酸缩水甘油酯0.45g,于95℃进行2小时搅拌。需要说明的是,相对于合成例5中使用的化合物a1摩尔而言,添加0.25摩尔甲基丙烯酸缩水甘油酯。接着冷却至室温,以固态成分(不挥发成分)浓度成为30质量%的方式加入丙二醇单甲基醚乙酸酯,得到质均分子量为3,100g/mol的感光性树脂a-5的溶液。通过测定固态成分酸值而确认了加成有甲基丙烯酸缩水甘油酯。
[0478]
<负型感光性树脂组合物及经图案化的固化膜的制作>
[0479]
[实施例1~5及比较例1]
[0480]
使作为感光性树脂的表1中记载的感光性树脂a-1~a-5或含有羧基的树脂a-6 60质量份、作为光聚合性化合物(b)的下述b-1 30质量份、作为光聚合引发剂(c)的下述化合物p-1 5质量份、和作为具有反应性官能团的硅烷偶联剂的3-丙烯酰氧基丙基三甲氧基硅烷5质量份以固态成分浓度成为30质量%的方式溶解于作为溶剂(s)的丙二醇单甲基醚乙酸酯中,制作实施例1~5及比较例1的负型感光性树脂组合物。
[0481]
[化学式43]
[0482][0483]
使用旋涂机将所得到的负型感光性树脂组合物涂布于玻璃基板,于100℃进行2分钟加热(干燥),形成膜厚为3μm的涂布膜。
[0484]
对于干燥后的涂布膜,使用形成有宽度为10μm的图案的负型掩模,使用高压汞灯作为光源,以累计曝光量成为50mj/cm2的方式进行曝光。
[0485]
于100℃对曝光后的涂布膜进行2分钟加热(peb)后,通过下述的方法进行折射率和透过率的测定。
[0486]
其后,利用25℃的2.38质量%四甲基氢氧化铵水溶液(水溶性碱性显影液)对涂布膜进行180秒钟显影,进行水洗,得到经图案化的固化膜。
[0487]
对于所得到的经图案化的固化膜,通过下述的方法进行耐溶剂性的评价。将结果示于表1。
[0488]
[折射率的测定]
[0489]
对于peb后的涂布膜(固化膜),使用metricon公司制棱镜耦合器,求出波长550nm处的折射率的值。
[0490]
[透过率的测定]
[0491]
对于peb后的涂布膜(固化膜),使用大塚电子公司制多通道分光器(mcpd-3000),求出波长400nm处的透过率的值。
[0492]
[耐溶剂性的测定]
[0493]
将所得到的经图案化的固化膜在丙二醇单甲基醚乙酸酯中浸渍1分钟,测定浸渍前后的膜厚,利用下式求出残膜率。
[0494]
残膜率(%)=(浸渍后的膜厚/浸渍前的膜厚)
×
100
[0495]
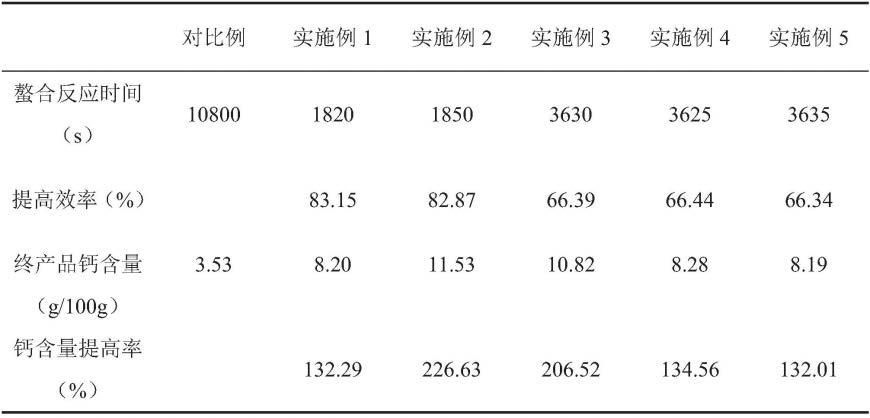
[表1]
[0496][0497]
如表1所示,可知利用包含在具有式(a1)所示的结构单元的含有羧基的树脂所具
有的羧基的至少一部分上加成或缩合有具有羧酸反应性基团的(甲基)丙烯酸酯化合物的感光性树脂和光聚合引发剂的实施例的负型感光性树脂组合物形成的固化膜具有高折射率及高透明性。另外可知,这些固化膜的残膜率高,耐溶剂性也优异。需要说明的是,实施例及比较例中,均形成了宽度为10μm的图案。
[0498]
另一方面,根据比较例1可知,负型感光性树脂组合物不包含在具有式(a1)所示的结构单元的含有羧基的树脂所具有的羧基的至少一部分上加成或缩合有具有羧酸反应性基团的(甲基)丙烯酸酯化合物的感光性树脂的情况下,不能同时实现高折射率及高透明性。另外可知,比较例1的固化膜的耐溶剂性较之实施例而言极差。
[0499]
<含有羧基的树脂的评价>
[0500]
[参考例1~6]
[0501]
向作为含有羧基的树脂的表2中记载的含有羧基的树脂a-1~a-5或含有羧基的树脂a-6的溶液中,以固态成分浓度(不挥发成分)成为30质量%的方式加入丙二醇单甲基醚乙酸酯,制作含有羧基的树脂的溶液。
[0502]
使用旋涂机将含有羧基的树脂的溶液涂布于玻璃基板,于100℃进行2分钟加热(干燥),形成厚度为3μm的涂布膜。
[0503]
对于所得到的涂布膜,进行下文中记载的折射率及透过率的测定。将结果记载于表2。
[0504]
[折射率的测定]
[0505]
对于所得到的涂布膜,使用metricon公司制棱镜耦合器,求出波长550nm处的折射率的值。
[0506]
[透过率的测定]
[0507]
对于所得到的涂布膜,使用大塚电子公司制多通道分光器(mcpd-3000),求出波长400nm处的透过率的值。
[0508]
[表2]
[0509][0510]
如表2所示,可知具有式(a1)所示的结构单元的含有羧基的树脂中,r
3a
为式(a1a)所示的4价有机基团的a-4或a-5、与r
3a
并非式(a1a)所示的4价有机基团的a-1~a-3及a-6相比,以高水平同时实现了折射率及透过率。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。