1.本发明涉及一种用于产前胎儿结构异常辅助诊断的羊水代谢物组合及检测试剂盒,属于检验医学及临床化学、生殖医学领域。
背景技术:
2.胎儿结构异常,是指在产前检查中发现的胎儿单器官缺陷或多器官发育异常,是引起新生儿死亡和危重症的主要病因。常见的胎儿结构异常主要包括心脏畸形、中枢神经系统发育异常和泌尿系统发育异常等。其中,胎儿心脏结构异常的发病率在6~19
‰
之间,居于胎儿先天性缺陷的首位,是引起新生儿死亡的最主要疾病原因。常见心脏缺陷主要有心内膜垫缺损、法洛氏四联症、左室流出道梗阻、复杂心脏畸形等。胎儿中枢神经系统发育异常也是常见的先天性畸形之一,中枢神经系统疾病复杂繁多,这其中神经管缺陷最为常见,据文献报道国内发病率为1
‰
~2
‰
。中枢神经系统异常的主要临床指征有前脑无裂畸形、无脑回畸形、胼胝体发育不全或缺失、dandy-walker畸形等。泌尿系统畸形在胎儿常见畸形中的发病率也较高,在1.5~4%
‰
之间,常见的合并染色体异常的胎儿泌尿系统异常的临床指征主要有肾积水或肾盂扩张、多囊性肾发育不良、肾囊肿、异位肾等。
3.目前,临床上筛查诊断胎儿结构异常的主要手段是超声波检查。同时,因胎儿结构异常与染色体非整倍体、拷贝数变异(cnvs)和发育基因中的致病序列变异等等遗传因素有关。因此,临床上对于超声波检查发现的胎儿结构异常病例或疑似病例,还利用羊水穿刺术等产前诊断手段采集羊水,再利用核型分析和染色体微阵列分析(cma)等遗传学检测来辅助诊断并明确病因。根据一项权威的医学研究报道,目前约32%结构异常胎儿具有临床相关的异常核型,另外6.5%的胎儿具有致病性cnvs,这也意味着有超过60%的结构异常胎儿没有检测到明确的遗传学缺陷(wapner rj, martin cl,levy b,et al.chromosomal microarray versus karyotyping forprenatal diagnosis.n engl j med 2012;367:2175-84.),换言之目前临床上有超过60%以上的结构异常胎儿没有表现出核型分析和cma检测结果异常。而根据另外一项最新研究报道,对于核型检测和cma检测均为阴性的胎儿结构异常病例,即使是使用价格高昂且实施周期长的全外显子测序(wes) 也只能在10%的结构异常病例中鉴定出与发育障碍相关的诊断性基因变异 (slav
é
petrovski,vimla aggarwal,jessica l giordano,et al.whole-exomesequencing in the evaluation of fetal structural anomalies:a prospective cohort study.lancet 2019;393(10173):758-767.)。另一方面,超声诊断筛查十分依赖于超声医师的经验与技能,同时还存在一定的漏诊与误诊风险。因此,开发与超声筛查、遗传学检测形成互补的新型诊断技术对于产前胎儿结构异常的辅助诊断,进而对于优生优育都具有重要临床价值。
4.羊水起源于母体、胎儿和胎盘组织,羊水中代谢物的浓度是孕期内伴随胎儿成熟而在母体与胎儿体内进行的代谢物合成与降解的最终结果,可以反映胎儿的健康状况,这一生化特性使其成为对胎儿健康诊断极有价值的材料。氨基酸作为蛋白质和核苷酸等大分子生物合成的重要前体,参与胎儿发育和生长。谷氨酰胺和谷氨酸是妊娠晚期胎儿体内最
丰富和使用最多的氨基酸之一。谷氨酸通过高亲和力兴奋性氨基酸转运蛋白转运穿过合体滋养层微绒毛膜和基底膜,并在胎盘中转化为谷氨酰胺,谷氨酸同时也是重要的生物合成氮源和神经递质前体。因此,胎盘-胎儿中的谷氨酸-谷氨酰胺循环和交换在胎儿生长发育中发挥着重要作用(moores rr,jr.,vaughnpr,battaglia fc,et al.glutamate metabolism in fetus and placenta oflate-gestation sheep.am j physiol.1994;267(1pt 2):r89-96.)。
技术实现要素:
5.本发明提供了一种基于两种羊水氨基酸定量检测的新的代谢物组合以及检测试剂盒,应用于产前胎儿结构异常的辅助诊断。所述发明的代谢物组合和检测试剂盒的特征如下:
6.本发明所述的代谢物组合包括两种小分子氨基酸代谢物,即:l-谷氨酰胺和l-谷氨酸。
7.本发明所述的检测试剂盒包括定量液、提取液、稀释液、内标液和微孔板。其中,定量液含有定量外标物l-谷氨酰胺、l-谷氨酸和内标物谷氨酰胺-d5、谷氨酸-d5,所述外标物分别用于受试者待检羊水中l-谷氨酰胺、 l-谷氨酸的浓度定量和/或定性鉴定,内标物分别用于l-谷氨酰胺、l-谷氨酸的定量。提取液是甲醇和/或乙腈溶液,用于受试者待检羊水样本的预处理。稀释液是甲醇和/或乙腈的水溶液(稀释液中添加适量的有机溶剂可以抑制微生物增殖,便于延长有效期),用于受试者待检羊水提取液的稀释。试剂盒含有3张微孔板,其中一号板是单孔容量750微升的深孔板,用于受试者待检羊水预处理;二号板是单孔容量450微升的浅孔板,用于稀释从一号板中转移出的受试者待检羊水的提取液;三号板同二号板,将二号板中的稀释液转移至三号板,供液相色谱质谱法上机检测。
8.本发明所述的检测试剂盒的工作流程是:(1)取10~100μl待检羊水样本逐份转移至一号板微孔中,分别加入5~50μl内标液和40~400μl提取液,1500rpm转速涡旋振荡3分钟,将一号板放入离心机,5000rpm转速离心20分钟,得羊水提取液;(2)每份待检样本吸取20~500μl羊水提取液转移至二号板微孔,使用20~500μl稀释液稀释羊水提取液,得羊水稀释液;(3)羊水稀释液5000rpm转速离心20分钟后,每份待检样本吸取30~900μl羊水稀释液转移至三号板微孔中,即可进行液相色谱质谱法上机检测;(4)将所述的定量液、处理后的受试者待检羊水稀释液分别经液相色谱质谱法检测,比较定量液(20~200ng/ml之间任一浓度点)中外标物 l-谷氨酰胺、l-谷氨酸与受试者待检羊水质谱扫描记录的色谱峰的保留时间,保留时间相差
±
0.05分钟以内,即判断该色谱峰为受试者待检羊水中检测到的两个代谢物的色谱峰,实现对受试者待检羊水中两个氨基酸代谢物的定性鉴定(谷氨酰胺与谷氨酸作为生命活动中发挥重要作用的关键氨基酸是一定在羊水中存在的,不存在检测不到的情况);比较任一浓度点定量液中内标物氘代谷氨酰胺-d5、氘代谷氨酸-d5与受试者待检羊水质谱扫描记录的色谱峰的保留时间,保留时间相差
±
0.05分钟以内,即判断该色谱峰为两个氨基酸分别对应的内标物的色谱峰,实现对受试者待检羊水中内标物的定性鉴定。分别记录定量液、受试者待检羊水中l-谷氨酰胺与内标物氘代谷氨酰胺-d5的峰面积值,l-谷氨酸与内标物氘代谷氨酸-d5的峰面积值,并分别计算两个氨基酸外标物与对应内标物的峰面积比值,再以定量液中外标物浓度值为x,以前述外/内标峰面积比值为y,分别
绘制l-谷氨酰胺、l-谷氨酸的定量工作曲线并建立定量工作方程。将受试者待检羊水样本记录计算的前述外/内标峰面积比值代入方程得到质量浓度,再经过样本预处理体积折算和摩尔量换算,即计算出受试者l-谷氨酰胺、l-谷氨酸的羊水浓度值,单位μmol/l,同时计算l-谷氨酰胺/l-谷氨酸浓度比。(5) 本发明确定基于所述两个氨基酸组合的浓度比用于胎儿结构异常诊断的最佳截断值是2.38,受试者羊水l-谷氨酰胺/l-谷氨酸摩尔浓度比高于2.38,诊断为结构异常阳性病例,反之为阴性。截断值的设定方法是首先依据诊断模型训练集中每一个受试者的l-谷氨酰胺/l-谷氨酸浓度比及其对应分类信息(胎儿结构异常组分类信息设定为1,正常对照组分类信息设定为0),采用graphpad软件或medcalc软件等功能相当的医学统计软件,或者r语言等开源程序包绘制roc曲线,所得roc曲线图中x轴表示诊断模型的 100%-特异性%,y轴表示诊断模型的灵敏度%。最佳截断值是roc曲线中灵敏度与特异性之和最大处对应的l-谷氨酰胺/l-谷氨酸浓度比。本发明涉及的羊水检测试剂盒使用单位可以根据新的训练集和现场的实验结果设定适合所在单位使用的新的最佳截断值。
9.本发明涉及的两种氨基酸在胎儿结构异常组与正常对照组间均有显著的浓度差异,且都对辅助结构异常诊断具有良好的效果。两种代谢物组合后,诊断的灵敏度和特异性提升至87.1%和86.1%,roc曲线的曲线下面积(auc)提升至0.913。据此,本发明两种羊水代谢物组合所呈现的良好诊断性能使其具备辅助胎儿结构异常的实用价值。本发明所述检测试剂盒具有诊断特异性与灵敏度高、标志物组合简单、质谱法测定准确、报告结果快、检测成本低等特点,有助于与超声筛查和遗传学检测形成互补,提高妇产科临床中针对胎儿结构异常病例的诊断准确性。
10.本发明还涉及用于胎儿结构异常辅助诊断的检测试剂盒,通过液相色谱质谱法检测受试者羊水中上述两种氨基酸的浓度值,计算l-谷氨酰胺/l-谷氨酸的浓度比,与诊断模型的最佳截断值相比较,从而诊断受试者是否为胎儿结构异常。所述两种代谢物组合的联合应用对于产前超声胎儿结构异常具有良好的辅助诊断效果。本发明所述检测试剂盒具有诊断特异性与灵敏度高、标志物组合简单、质谱法测定准确、报告结果快、检测成本低等特点,有助于与超声筛查和遗传学检测形成互补,提高妇产科临床上胎儿结构异常的诊断准确性。
附图说明
11.图1为实施例1说明附图:
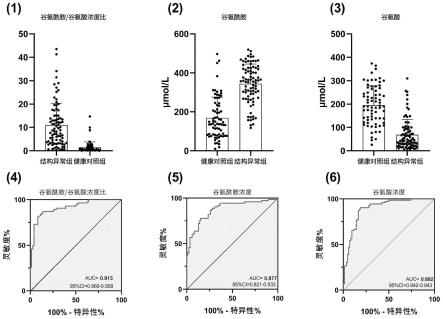
12.(1)实施例1受试样本l-谷氨酰胺/l-谷氨酸浓度比的柱图;
13.(2)l-谷氨酰胺羊水浓度值柱图;
14.(3)l-谷氨酸羊水浓度值柱图;
15.(4)组合使用l-谷氨酰胺/l-谷氨酸浓度比用于胎儿结构异常诊断的roc 曲线;
16.(5)单独使用l-谷氨酰胺浓度用于胎儿结构异常诊断的roc曲线;
17.(6)单独使用l-谷氨酸浓度用于胎儿结构异常诊断的roc曲线;
18.图2为实施例2说明附图
19.(1)实施例2受试样本l-谷氨酰胺/l-谷氨酸浓度比的柱图;
20.(2)l-谷氨酰胺羊水浓度值柱图;
21.(3)l-谷氨酸羊水浓度值柱图。
具体实施方式
22.实施例1
23.诊断阈值的确定
24.1.临床试验设计:研究项目经过医学伦理会批准,受试者纳入临床试验前签署知情同意书。包括72例正常对照组受试者(母亲年龄29.07
±
2.64岁,孕期146.36
±
4.68天)和85例胎儿结构异常组受试者(母亲年龄25.68
±
1.85 岁,孕期147.14
±
4.61天)。正常对照组受试者因符合羊水穿刺术的临床要求而接受了羊水穿刺,但分娩后证实胎儿无结构异常。结构异常受试者同样也因符合妇产科临床要求而接受了羊水穿刺,引产后证实胎儿结构异常。其中,心脏结构异常40例,中枢神经系统结构异常23例,泌尿系统结构异常22例。结构异常组受试者核型分析与染色体微阵列检测结果均正常,即临床遗传学检查没有发现基因缺陷。
25.2.受试者羊水采集:医院产前诊断科行羊膜穿刺术,采集受试者羊水20~25 ml,采集后4℃下1200rpm离心10min,分离羊水,存储在-80℃冰箱中待检。
26.3.受试者待检羊水预处理:受试者待检羊水样本室温下解冻,逐份分别转移50μl至一号微孔板的微孔中,使用电动分液器逐孔分别加入10μl内标液(谷氨酰胺-d5和谷氨酸-d5的浓度均为10μg/ml)和200μl提取液(体积比1:1的甲醇-乙腈混合液),1500rpm
×
3min涡旋振荡后,5300rpm
×
20 min离心去除蛋白沉淀,分别一一转移130μl羊水提取液至二号板的微孔中,逐孔加入130μl水稀释提取液,1500rpm
×
3min涡旋振荡后,5300rpm
ꢀ×
20min离心再次去除蛋白沉淀,分别一一转移130μl稀释液至三号板的微孔中备液相色谱串联质谱上机检测。
27.4.液相色谱串联质谱检测:氨基酸检测使用日本岛津公司shimadzulc-20adxr型液相色谱仪串联美国爱博才思公司sciex 5500 三重四极杆质谱仪,采用选择反应监测模式(srm)扫描,内标法定量。
28.4.1液相色谱方法:液相色谱使用acquity beh酰胺柱(acquity uplcbeh amide column)(填料粒径1.7μm,内径2.1mm,柱长100mm);二元洗脱流动相分别是a:10/90水/乙腈混合液(v/v),内含10mm甲酸铵和 0.1%甲酸(v/v),b:50/50水/乙腈混合液(v/v),内含10mm甲酸铵和 0.1%甲酸(v/v);流速是0.3ml/min;进样体积是2μl。色谱洗脱梯度设定为:起始体积比例0%b相,第0~12分钟线性递升至70%b,第12~13 分钟维持70%b,第13分钟下降至起始比例0%b,并维持到第19分钟,完成。
29.4.2质谱方法:turbo v电喷雾离子源,正离子电离电压5.5kv,离子源温度550℃,气帘气压强20磅力/平方英寸,喷雾气压强50磅力/平方英寸,辅助加热气压强50磅力/平方英寸。使用选择反应监测模式扫描,l-谷氨酰胺扫描离子对是母离子147.1
→
子离子130.1、去簇电压65v,碰撞电压15v,其内标物氘代谷氨酰胺-d5的扫描离子对是母离子152.1
→
子离子135.1、去簇电压与碰撞电压同谷氨酰胺;l-谷氨酸扫描离子对是母离子148.1
→
子离子84.1、去簇电压与碰撞电压分别为75v和25v,其对应内标物氘代谷氨酸-d5的扫描离子对是母离子153.1
→
子离子88.1,去簇电压与碰撞电压同谷氨酸。
30.5.定量工作曲线与氨基酸定量:定量液是含外标物(10个浓度点)以及相同浓度内
标物的10份甲醇-水溶液(甲醇体积浓度是50%),用于建立内标法定量工作曲线。外标物是l-谷氨酰胺、l-谷氨酸,10份定量工作曲线溶液中两种外标物分别的浓度从低到高依次为:10、20、50、100、200、500、 1000、2000、5000、10000ng/ml,依次简称为l1、l2、l3、l4、l5、l6、 l7、l8、l9、l10。内标物氘代谷氨酰胺-d5、氘代谷氨酸-d5的浓度均为 200ng/ml。将定量工作曲线溶液和处理后的受试者羊水样本分别进行液相色谱串联质谱检测,比较定量液(500ng/ml浓度点)中外标物l-谷氨酰胺、 l-谷氨酸与受试者待检羊水质谱扫描记录的色谱峰的保留时间,保留时间相差
±
0.05分钟以内,判断该色谱峰为受试者待检羊水中检测到的两个氨基酸,实现对受试者待检羊水中两个氨基酸的定性鉴定。比较任一浓度点定量液中内标物氘代谷氨酰胺-d5、氘代谷氨酸-d5与受试者待检羊水质谱扫描记录的色谱峰的保留时间,保留时间相差
±
0.05分钟以内,即判断该色谱峰为两个标志物分别对应的内标物的色谱峰,实现对受试者待检羊水中内标物的定性鉴定。
31.分别记录定量液和受试者待检羊水中l-谷氨酰胺与氘代谷氨酰胺-d5 的峰面积值、l-谷氨酸与内标物氘代谷氨酸-d5的峰面积值(表1),并计算两个氨基酸外/内标物的峰面积比值。以对应定量液中外标物浓度为x,以外/内标峰面积比值为y,分别绘制定量工作曲线并建立定量工作方程,如下。
32.l-谷氨酰胺的定量工作曲线方程:y=4.87439e-4x 0.02469
33.l-谷氨酸的定量工作曲线方程:y=7.66456e-4x 0.11324
34.分别将受试者待检羊水样本记录计算的前述峰面积比值代入方程,即可计算出受试者待检羊水l-谷氨酰胺、l-谷氨酸的质量浓度值(单位 ng/ml),先分别乘以样本预处理环节引入的体积折算系数10.4(来自《3.受试者待检羊水预处理》项下描述的数值,计算公式:[(c d e)
÷
c]
×
[(a b)
÷
a], c表示羊水使用体积,d表示内标液使用体积,e表示加入羊水中的提取液的使用体积,a表示稀释前转移至三号板的羊水提取液体积,b表示稀释液使用体积。再分别除以谷氨酰胺和谷氨酸的摩尔质量146.15g/mol、147.13 g/mol,得到两个氨基酸代谢物的浓度值,单位为μmol/l(表1)。使用spss 统计软件进行t检验,结果l-谷氨酰胺/l-谷氨酸浓度比在两组之间具有显著性差异(p《0.0001,图1-(1))。l-谷氨酰胺在正常对照组和胎儿结构异常组的羊水浓度分别为168.8
±
107.5μmol/ml和344.7
±
100.7μmol/l,l-谷氨酸的浓度分别为195.8
±
82.6μmol/ml和68.74
±
64.66μmol/l(图1-(2)和图1-(3)), l-谷氨酰胺和l-谷氨酸在两组之间均具有显著性差异(p《0.0001)。
[0035]
6.基于代谢物组合的诊断模型与诊断性能评价:分别以实施例1受试者l
‑ꢀ
谷氨酰胺浓度、l-谷氨酸浓度以及对应的受试者分类信息(胎儿结构异常组分类设定为1,正常对照组分类设定为0),使用graphpad prism软件绘制诊断模型的roc曲线(图1-(5)和图1-(6)),图中x轴是诊断模型的100%
‑ꢀ
特异性%,y轴是诊断模型的灵敏度。可知,单独使用l-谷氨酰胺和l-谷氨酸进行胎儿结构异常诊断的模型曲线下面积(auc)分别为0.877、0.892。再以受试者l-谷氨酰胺/l-谷氨酸浓度比和分类信息绘制用于胎儿结构异常诊断模型的roc曲线(图1-(4)),结果显示所述两个代谢物组合使用后auc 提高至0.913,诊断模型的灵敏度与特异性更为均衡,辅助结构异常诊断的性能更出色。
[0036]
根据实施例1确定诊断模型的最佳截断值是2.38。对实施例1涉及的病例与疑似病例进行诊断,结果72例健康受试者中有62例受试者的l-谷氨酰胺/l-谷氨酸浓度比低于截断值,判定结果为阴性,试剂盒的诊断准确性86.1%。85例结构异常受试者中有74例的判定
结果为阳性,试剂盒的诊断准确性87.1%(表2)。
[0037]
实施例2
[0038]
用于评估诊断效果的盲样测试
[0039]
1.临床试验设计:研究项目经过医学伦理会批准,受试者纳入临床试验前签署知情同意书。包括30例正常对照组受试者(母亲年龄27.77
±
1.74岁,孕期145.77
±
2.66天)和38例胎儿结构异常组受试者(母亲年龄27.53
±
1.59 岁,孕期146.84
±
2.64天)。正常对照组受试者因符合羊水穿刺术的临床要求而接受了羊水穿刺,但分娩后证实胎儿无结构异常。结构异常受试者同样也因符合妇产科临床要求而接受了羊水穿刺,引产后证实胎儿结构异常。包括心脏结构异常20例、中枢神经系统结构异常6例、泌尿系统结构异常 12例。结构异常组受试者核型分析与染色体微阵列检测均正常,即临床遗传学检查没有发现缺陷。质谱测试前将受试者样本做盲样化处理,质谱检验人员、数据分析人员与复核人员均不知道盲样的实际分类。测试后揭盲,比较试剂盒的诊断结果与实际临床结论,并计算诊断准确率。
[0040]
2.受试者羊水采集:同实施例1此相应过程和条件。
[0041]
3.受试者待检羊水预处理:同实施例1此相应过程和条件。
[0042]
4.液相色谱串联质谱检测:实施例2使用具备医疗器械注册证的临床质谱系统进行氨基酸检测,系统包括日本岛津公司shimadzu lc-40a型液相色谱仪和美国爱博才思公司ab sciex triple quad 4500md三重四极杆质谱仪,采用选择反应监测模式(srm)扫描,内标法定量。
[0043]
4.1液相色谱方法:同实施例1此相应过程和条件。
[0044]
4.2质谱方法:同实施例1此相应过程和条件。
[0045]
5.定量工作曲线与氨基酸定量:同实施例1此相应过程和条件。
[0046]
分别记录定量液和受试者待检羊水中l-谷氨酰胺与氘代谷氨酰胺-d5 的峰面积值、l-谷氨酸与内标物氘代谷氨酸-d5的峰面积值(表3),并计算两个氨基酸外/内标物的峰面积比值。以对应定量液中外标物浓度为x,以外/内标峰面积比值为y,分别绘制定量工作曲线并建立定量工作方程,如下。
[0047]
l-谷氨酰胺的定量工作曲线方程:y=-8.61399e-10x2 5.83699e-4x 0.00695
[0048]
l-谷氨酸的定量工作曲线方程:y=8.16227e-4x 0.09569
[0049]
分别将受试者待检羊水样本记录计算的前述峰面积比值代入方程,即可计算出受试者待检羊水l-谷氨酰胺、l-谷氨酸的质量浓度值(单位 ng/ml),按照实施例1中同样的体积折算系数和摩尔量换算,最终得到两个氨基酸代谢物的浓度值,单位为μmol/l(表3)。谷氨酰胺/谷氨酸浓度比在两组之间具有显著性差异(p《0.0001,图2-(1)),l-谷氨酰胺在正常对照组和胎儿结构异常组的羊水浓度分别为67.5
±
76.15μmol/ml和325.8
±
59.44 μmol/l,l-谷氨酸的浓度分别为285.9
±
68.13μmol/ml和94.29
±
38.40μmol/l (图2-(2)和图2-(3)),二者在两组之间均具有显著性差异(p《0.0001)。
[0050]
6.基于代谢物组合的诊断结果与揭盲结果:根据实施例1确定的诊断阈值, l-谷氨酰胺/l-谷氨酸浓度比高于2.38,则诊断样本为结构异常(阳性病例),反之,则为结构正常(阴性)。实施例2中,有31例盲样在经过所述试剂盒检测后被诊断为结构异常,37个被诊断为结构正常。揭盲后发现,在实际分组为结构异常的38例受试者中有31例诊断正确,7例
被诊断为结构正常,显示所述代谢物组合和质谱试剂盒对于病例的诊断准确率为81.6%,漏诊率(假阴性)为18.4%;在被诊断为结构正常的37例样本中,实际分组为结构正常的30例受试者均诊断正确,显示所述代谢物组合和质谱试剂盒对于正常对照的诊断准确率为100%(表4)。本发明所述代谢物组合和质谱检测试剂盒在盲样验证测试中展示了良好的辅助诊断效果,对结构异常阳性病例的诊断效果较为理想。
[0051]
表1
[0052]
[0053]
[0054]
[0055]
[0056][0057]
表2
[0058]
[0059]
[0060]
[0061][0062]
表3
[0063]
[0064][0065]
表4
[0066]
[0067]
[0068]
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。