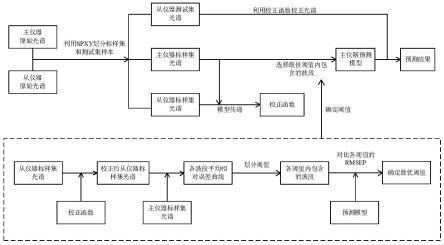
1.本发明涉及中药炮制的质量检测领域,特别涉及大戟属中草药的质量检测方法。
背景技术:
2.中药药用部位含有有效成分,但也常含有一些影响药效的成分,使药材在发挥治疗作用的同时,可能出现不良反应,尤其对于有毒中药。通过炮制技术,调整药性,增利除弊,可以更好发挥中药药效,满足临床治疗要求。
3.大戟属中草药中较多种类中草药为有毒药用植物,例如:甘遂作为中国药典收载的有毒中药之一,在临床使用时需要降低其毒性。目前普遍采用炮制的方法来降低其毒性,例如:甘遂传统的炮制方法包括:醋甘遂、豆腐制甘遂、甘草制甘遂等。《中国药典》2010版收载了醋甘遂;豆腐制甘遂在上海一些医院中使用较为多见,有其独特的临床应用特点;而甘遂与甘草是中药著名十八反之一,此种方法也是中药炮制中非常有特点的一种炮制方法。上述三种方法涵盖了炒、煮、蒸三种处理方法,并且涉及三种不同原料(米醋、豆腐和甘草浓煎汁),非常具有代表性。甘遂采用上述三种不同炮制方法和不同原料处理方法,目的均是降低甘遂的毒性,但无法统一评价各炮制方法的质量是否符合临床药用标准,因此需要建立检测方法来评判大戟属中草药及其炮制品的质量。
4.目前,围绕中药炮制前后的差异问题,相关研究人员已经采用色谱指纹图谱方法、蒸发光散射检测器(elsd)等技术手段进行了研究;更有采用质谱作为检测手段对炮制工艺进行优化。但迄今仍没有方法可以明确指出炮制对大戟属中草药(例如:甘遂)效应物质的影响。因此,急需一种能够明确指出炮制对大戟属中草药效应物质的影响的质量检测方法,以便于实现对各炮制品的质量控制。
技术实现要素:
5.基于此,有必要提供一种大戟属中草药的质量检测方法,该质量检测方法能够明确指出炮制对大戟属中草药效应物质的影响,以便于实现对各炮制品的质量控制。
6.一种大戟属中草药的质量检测方法,包括以下步骤:
7.获取大戟属中草药炮制前的生药和炮制后的炮制品,并分别配制成检测样品;
8.采用色谱-质谱联用方法分别检测所述生药和所述炮制品的检测样品,获得对应的检测数据;
9.采用化学计量学方法分析各所述检测数据,确定所述炮制品和所述生药的成分差异。
10.在其中一实施例中,所述炮制品包括至少两种不同方法炮制而成的炮制品,所述检测是指采用相同的方法进行检测。
11.在其中一实施例中,所述化学计量学方法分析方法包括以下步骤:
12.分析各所述炮制品和所述生品的检测数据的整体数据差异;
13.分析各所述炮制品和所述生品的检测数据的局部数据差异。
14.在其中一实施例中,分析所述整体数据差异和所述局部数据差异的步骤中,采用metalign软件结合simca-p软件。
15.在其中一实施例中,分析各所述炮制品和所述生品的检测数据的整体数据差异的步骤包括以下步骤:
16.将各炮制品的检测数据进行主成分分析,并绘制部分主成分的得分图,根据所述得分图中点的离散性,判断整体数据差异,若整体数据差异较小,进行后续步骤;
17.分别建立pls-da模型和opls-da模型,采用parn对各炮制品的检测数据进行数据变换,并判断何种模型可以最大程度的体现变量对分类的预测性,以确定应选用模型;
18.采用所述选用模型对各炮制品的检测数据进行处理,选择两个和/或三个主成分,绘制得分图,根据所述得分图判断各炮制品之间成分差异程度;
19.对各炮制品和生品的检测数据进行差异比较,以parn进行数据变换,以所述选用模型进行差异分析,并绘制s-plot图,计算变量重要性数值,判断各炮制品相对于生品变化的成分;
20.采用韦恩图分析各炮制品相对于生品共同变化的成分,并根据共同变化的成分的质荷比和保留时间绘制色谱分布示意图,以确定局部数据分析的目标数据范围。
21.在其中一实施例中,分析各所述炮制品和所述生品的检测数据的局部数据差异的步骤包括以下步骤:
22.将各炮制品的目标数据范围的检测数据进行主成分分析,并绘制部分主成分的得分图,根据所述得分图中点的离散性,判断目标数据范围的局部数据差异,若局部数据差异较小,进行后续步骤;
23.分别建立pls-da模型和opls-da模型,采用parn对各炮制品的目标数据范围的检测数据进行数据变换,并判断何种模型可以最大程度的体现变量对分类的预测性,以确定应选用模型;
24.采用所述选用模型对各炮制品的目标数据范围的检测数据进行处理,选择两个和/或三个主成分,绘制得分图,根据所述得分图判断各炮制品之间成分差异程度;
25.对各炮制品和生品的目标数据范围的检测数据进行差异比较,以parn进行数据变换,以所述选用模型进行差异分析,并绘制s-plot图,计算变量重要性数值,判断各炮制品相对于生品变化的成分;
26.采用韦恩图分析各炮制品相对于生品共同变化的成分,并根据共同变化的成分的质荷比和保留时间绘制色谱分布示意图,以确认各所述炮制品的质量相关信息。
27.在其中一实施例中,分析各所述炮制品和所述生品的检测数据的局部数据差异的步骤后还包括以下步骤:
28.采用xcms软件再次验证分析所述炮制品炮制前和炮制后的整体数据差异。
29.在其中一实施例中,所述大戟属中草药为甘遂,所述炮制品为醋甘遂、甘草制甘遂和豆腐制甘遂中的一种或多种。
30.在其中一实施例中,所述色谱-质谱联用方法为液相色谱-质谱联用;
31.其中,液相色谱的检测条件为:以乙腈为流动相a,0.1%甲酸水溶液为流动相b,进行梯度洗脱;和/或
32.质谱为电喷雾电离源-质谱检测器。
33.一种大戟属中草药的质量检测方法,包括以下步骤:
34.获取所述大戟属中草药的标准炮制品,并配制成检测样品;
35.采用色谱-质谱联用方法检测所述检测样品,获得标准炮制品的检测数据;
36.采用化学计量学方法分析所述检测数据,建立判别模型;
37.获取待测炮制品,并配制成检测样品;
38.采用所述色谱-质谱联用方法检测待测炮制品的检测样品,获得待测炮制品的检测数据;
39.采用化学计量学方法分析所述检测数据,并根据所述判别模型,判断所述待测炮制品质量是否符合要求
40.有益效果:
41.通过上述质量检测方法可以明确炮制前后哪些成分升高,哪些成分降低,升高或降低的成分的分子量范围以及保留时间是什么等,如此可以直观展示不同炮制品的炮制前后差异,使得研究者可以一目了然地观察炮制对有毒中药的整体影响,显示了优越的分析性能。该发明为今后有毒中药炮制的研究提供了有价值的研究方法。
附图说明
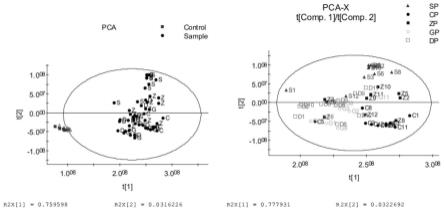
42.图1是本发明实施例中的整体数据主成分分析得分图(control-质控数据;sample-样品数据;sp-生甘遂;cp-市售醋甘遂;zp-自制醋甘遂;gp-自制甘草制甘遂;dp-自制豆腐煮甘遂);
43.图2是本发明实施例中的整体数据正交偏最小二乘判别分析得分图(1-生甘遂;2-市售醋甘遂;3-自制醋甘遂;4-自制甘草制甘遂;5-自制豆腐煮甘遂);
44.图3是本发明实施例中的甘遂不同炮制品与生甘遂整体数据差异分析s曲线图(s-plot)(黑色方块为炮制后降低成分,红色圆点为炮制后升高成分);
45.图4是本发明实施例中的韦恩图分析甘遂不同炮制品炮制前后共同变化成分(左图:炮制后共同降低成分;右图:炮制后共同升高成分);
46.图5是本发明实施例中的甘遂不同炮制品共有升高/降低成分色谱分布示意图;
47.图6是本发明实施例中的430~1000m/z范围四组数据pca得分图和dmodx诊断图;
48.图7是本发明实施例中的430~1000m/z范围四组数据opls-da二维(左图)和三维(右图)得分图;
49.图8是本发明实施例中的生甘遂和醋甘遂430~1000m/z差异成分分析s-plot;
50.图9是本发明实施例中的生甘遂和甘草制甘遂430~1000m/z差异成分分析s-plot;
51.图10是本发明实施例中的生甘遂和豆腐制甘遂430~1000m/z差异成分分析s-plot;
52.图11是本发明实施例中的韦恩图分析甘遂不同炮制品炮制前后局部数据共同变化成分(左图:炮制后共同降低成分;右图:炮制后共同升高成分);
53.图12是本发明实施例中的甘遂共有降低成分炮制前后离子强度均值图(局部数据分析)(横坐标为共有降低成分编号);
54.图13是本发明实施例中的甘遂炮制前后成分差异直观图(由xcms online软件绘
制)。
具体实施方式
55.为了便于理解本发明,下面将对本发明进行更全面的描述,并给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
56.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
57.在本发明的描述中,需要理解的是,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。在本发明的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
58.本发明一实施方法提供了一种大戟属中草药的质量检测方法,包括以下步骤:
59.s110:获取大戟属中草药炮制前的生药和炮制后的炮制品,并分别配制成检测样品;
60.可理解的,本发明的炮制前的制品是指生药,炮制后的制品为炮制品,炮制品是指将生药进行炮制后所得到的制品,例如醋甘遂、豆腐制甘遂、甘草制甘遂等。另外,步骤s110中炮制品可以为多种不同方法制备而成的炮制品,也可以为相同炮制方法不同批次的炮制品。
61.在一实施例中,本发明的大戟属中草药为甘遂。
62.在一实施例中,炮制品为醋甘遂、甘草制甘遂和豆腐制甘遂中的一种或多种。
63.在一实施例中,炮制品包括至少两种不同方法炮制而成的炮制品,各炮制品分别采用相同的方法进行检测和分析,以判定各炮制品炮制前后的质量差异和/或各炮制品之间的质量差异,进而确定有毒成分的相关参数范围,促进质量标准的建立。
64.进一步地,步骤s110包括以下步骤:
65.s111:将大戟属中草药的生药和炮制品分别进行粉碎,制得对应的粉碎物。
66.进一步地,步骤s111中粉碎物过四号筛。
67.s112:将粉碎物分别和溶剂混合,充分溶解后,过滤,收集滤液,除去溶剂,得到浓缩物。
68.进一步地,步骤s112中,溶剂为乙酸乙酯。
69.进一步地,步骤s112中,每0.1g粉碎物加4.5-5.5ml(优选为5ml)的溶剂。
70.进一步地,粉碎物和溶剂混合后,还包括超声的步骤,以促进成分的溶解;更进一步地,超声的条件为:功率120w-160w(优选为140w),频率40-45khz(优选为42khz),超声20min-40min(优选为30min)。
71.s113:将浓缩物溶解于甲醇中,并配制成预定浓度。
72.步骤s113中的浓度可以根据具体使用的仪器设备等进行选择,不应理解为对本发明的限定。
73.s120:采用色谱-质谱联用方法分别检测所述生药和所述炮制品的检测样品,获得对应的检测数据。
74.进一步地,步骤s120中,色谱-质谱联用方法为液相色谱-质谱联用。
75.进一步地,步骤s120中,大戟属中草药为甘遂,液相色谱的检测条件为:以乙腈为流动相a,0.1%甲酸水溶液为流动相b,进行梯度洗脱。
76.进一步地,梯度洗脱程序为:
77.时间/min流动相a035%乙腈154%乙腈654%乙腈770%乙腈1392%乙腈1592%乙腈17100%乙腈25100%乙腈31100%甲醇35初始流动相
78.进一步地,质谱为电喷雾电离源-质谱(esi-ms)检测器。
79.更进一步地,质谱条件为:正离子模式,喷雾压力40psi,干燥气流速7l/min,干燥气温度300℃。
80.可理解的,步骤s120中,生药及各炮制品对应的检测样品均采用基本相同的测试条件,每次测试过程中,操作及条件的选择,可以在本领域可接受的误差范围内进行变动。
81.s130:采用化学计量学方法分析各检测数据,确定炮制品和生药的成分差异。
82.本发明创新性地将质谱-化学计量学方法引入大戟属中草药的质量检测中,该方法可以对炮制品炮制前和炮制后的整体轮廓差异进行详细分析,并进一步可以分析各炮制品之间的差异,进而为分析炮制前后中药饮片的差异提供新的研究思路与方法,同时也有利于确定大戟属中草药的毒性成分,建立炮制品的质量标准,为各炮制品的质量监控提供了一种全新的思路。
83.进一步地,步骤s130包括以下步骤:
84.s131:分析各炮制品和生品的检测数据的整体数据差异。
85.在一实施例中,采用metalign软件结合simca-p软件进行整体数据差异分析。
86.在一实施例中,步骤s131中,采用主成分分析(pca)、偏最小二乘判别分析(pls-da)或正交偏最小二乘判别分析(opls-da)中至少一种方法进行分析。
87.在一实施例中,步骤s131包括以下步骤:
88.s1311:质控样品稳定性分析。
89.进一步地,步骤s1311中,质控样品为各炮制品混合后所得到的混合对照品。
90.进一步地,步骤s1311中,将混合对照样品注入色谱和质谱中,反复进行采样分析,判断色谱峰的保留时间重现性和峰高偏差是否在允许的范围内,以判断本发明的检测方法的稳定性。
91.s1312:metalign软件数据处理和导出。
92.可理解的,步骤s1312中,将色谱-质谱联用方法检测得到的检测数据,例如:质荷比-保留时间(m/z-rt)数据,导入metalign软件进行数据处理,并导出。
93.在一实施例中,metalign软件的参数设置为:峰斜率因子=1;峰阈值因子=2;峰阈值=5000;平均半高峰宽=10;色谱峰集内最小峰数=10。
94.s1313:simca-p软件分析数据质量。
95.可理解的,步骤s1313中,将metalign软件导出的数据采用simca-p软件进行分析,以判断炮制品和生品之间成分的差异,和/或炮制品之间的成分差异。
96.在一实施例中,步骤s1313中包括:
97.(1)将各炮制品的检测数据进行主成分分析(pca),并绘制部分主成分(优选炮制品的前两个主成分)的得分图,根据得分图中点的离散性,判断整体数据差异,若整体数据差异较小,进行后续步骤。
98.(2)pls-da模型和opls-da模型的选择。
99.具体地:分别建立pls-da模型和opls-da模型,采用parn对各炮制品的检测数据进行数据变换,并判断何种模型可以最大程度的体现变量对分类的预测性,以确定应选用模型。
100.在一实施例中,选择opls-da模型,其可以最大程度的体现变量对分类的预测性,且由opls-da处理后绘制的得分图能够更加直观、快速的提示成分质量的差异。
101.(3)采用选用模型对各炮制品的检测数据进行处理,选择两个和/或三个主成分,绘制得分图,根据得分图判断各炮制品之间成分差异程度。
102.可理解的,步骤(3)中选择两个主成分可以绘制得到二维图,选择三个主成分可以绘制得到三维图,以更直观、快速地提升成分之间是否存在差异。
103.(4)对各炮制品和生品的检测数据进行差异比较,以parn进行数据变换,以选用模型进行差异分析,并绘制s曲线图(s-plot图),计算变量重要性数值(vip,variable importance),判断各炮制品相对于生品变化的成分。
104.可理解的,步骤(4)中绘制的s-plot图可以反应质荷比-保留时间(m/z-rt)数据对差异的贡献程度,其中分布在左下角和右上角的数据是对差异贡献最大的数据。
105.步骤(4)中,变量重要性数值(vip,variable importance)能够定量反映质荷比-保留时间(m/z-rt)数据对分类变量的贡献率,一般大于1即认为与分类有关,即可认为与炮制差异有较大关联。
106.(5)采用韦恩图分析各炮制品相对于生品共同变化的成分,并根据共同变化的成分的质荷比和保留时间绘制色谱分布示意图,以确定局部数据分析的目标数据范围。
107.其中,步骤(5),可以采用韦恩图采用网络在线韦恩图作图软件(http://bioinfogp.cnb.csic.es/tools/venny/index.html)。
108.s132:分析各炮制品和生品的检测数据的局部数据差异。
109.在一实施例中,采用metalign软件结合simca-p软件进行局部数据差异分析。
110.需要说明的是,本发明的软件名称仅为示例,不应理解为对本发明的限制,应理解为,还可以采用与本发明所述软件相同或类似功能的软件,只要能够执行本发明所述目的操作即可。
111.步骤s132中的局部数据差异分析方法基本同整体数据分析方法,具体如上所述,二者不同之处在于,分析的数据范围不同,例如:局部数据差异分析包括以下步骤:
112.(1)将各炮制品的目标数据范围的检测数据进行主成分分析,并绘制部分主成分的得分图,根据得分图中点的离散性,判断目标数据范围的局部数据差异,若局部数据差异较小,进行后续步骤;
113.(2)分别建立pls-da模型和opls-da模型,采用parn对各炮制品的目标数据范围的检测数据进行数据变换,并判断何种模型可以最大程度的体现变量对分类的预测性,以确定应选用模型;
114.(3)采用选用模型对各炮制品的目标数据范围的检测数据进行处理后,选择两个和/或三个主成分,绘制得分图,根据得分图判断各炮制品之间成分差异程度;
115.(4)对各炮制品和生品的目标数据范围的检测数据进行差异比较,以parn进行数据变换,以选用模型进行差异分析,并绘制s-plot图(s-plot差异分析可以增加质荷比和保留时间在s-plot图中的同步显示),计算变量重要性数值,判断各炮制品相对于生品变化的成分;
116.(5)采用韦恩图分析各炮制品相对于生品共同变化的成分,并根据共同变化的成分的质荷比和保留时间绘制色谱分布示意图,以确认各炮制品的质量相关信息。
117.可理解的,步骤(5)中质量相关信息可以根据具体检测目标进行确定,在此不进行特别限定,应理解为均在本发明的保护范围内。例如检测目标为确定有毒成分,通过上述方法可以确定采用不同炮制方法进行减毒处理后,均是对色谱轮廓中的某一部分物质发生作用(共同降低的成分),由此可以确定有毒成分的质荷比和保留时间范围,进而建立质量标准。
118.s133:采用xcms软件再次验证分析各炮制品和生品的整体数据差异。
119.可理解的,步骤s133中可以采用xcms软件的操作方法进行操作,将其数据与上述步骤s131和s132的进行比对,以验证上述方法的准确性。
120.在一实施例中,步骤s133中,关键参数为线性对齐,bw=5;fwh=5;minfac=0.1。
121.本发明提供了一种大戟属中草药的质量检测方法,包括以下步骤:
122.s210:获取大戟属中草药的标准炮制品,并配制成检测样品;
123.s220:采用色谱-质谱联用方法检测检测样品,获得标准炮制品的检测数据;
124.s230:采用化学计量学方法分析检测数据,建立判别模型;
125.s240:获取待测炮制品,并配制成检测样品;
126.s250:采用色谱-质谱联用方法检测待测炮制品的检测样品,获得待测炮制品的检测数据;
127.s260:采用化学计量学方法分析检测数据,并根据判别模型,判断炮制品质量是否符合要求。
128.上述步骤s210-s260基本同s110-s130,在此不再进行赘述。不同之处在于,该方法首先确定一个标准炮制品,以该标准炮制品为对照,并确定一个判别模型,作为标准(例如:何种质荷比和保留时间的成分需要降低,降低幅度等),由此判断待测炮制品是否合格。
129.下面列举具体实施例来对本发明进行说明。
130.实施例1
131.检测条件及检测样品配制
132.⑴
色谱柱:halo c8(3mm
×
100mm,2.7μm);流动相:以乙腈为流动相a,0.1%甲酸水溶液为流动相b,流动相梯度程序为:0/1/6/7/13/15/17/25min;35/54/54/70/92/92/100/100乙腈%;25min后换为100%甲醇冲6min;之后改为初始流动相平衡4min;总运行时间为35min;电喷雾电离源-质谱(qqq-esi-ms)检测器检测,正离子模式;喷雾压力40psi;干燥气流速7l/min;干燥气温度300℃。
133.(2)样品来源:
134.sp-市售生甘遂:10批,信息如下。
135.cp-市售醋甘遂:10批,信息如下。
[0136][0137]
zp-自制醋甘遂:按照《中国药典》(2010版)所载甘遂项下炮制方法。取生甘遂50g,加酿造食醋15g,搅拌均匀,充分吸附浸泡过夜;次日取瓷蒸发皿,采用封闭电炉加热到约250℃,放入浸泡好的甘遂,翻炒20min至表面黄色至棕黄色,放冷,粉碎,备用。采用10批市售生甘遂,制备10批醋甘遂,编号zp01~zp10。
[0138]
gp-自制甘草制甘遂:按照《广东省中药饮片加工炮制手册》(1977版)所载甘遂项下炮制方法。取甘遂50g,加甘草汤(每100g甘遂用甘草20g切片煎浓汤),拌匀,浸置过夜,搅拌均匀,过夜浸至甘草汤基本吸尽;次日置不锈钢蒸锅内,蒸4小时至透心,离火候冷,减压蒸干(50℃),粉碎,备用。采用10批市售生甘遂,制备10批醋甘遂,编号gp01~gp10。
[0139]
dp-自制豆腐煮甘遂:按照《上海市中药饮片炮制规范》(2008版)所载甘遂项下炮制方法。取生甘遂50g,加水漂5日,每日换水2次,至内无干心,洗净,取出至不锈钢锅内,加水和豆腐同煮(水超过药面),煮1小时,至内无白心,取出,除去豆腐,减压蒸干(50℃),粉碎,备用。采用10批市售生甘遂,制备10批豆腐煮甘遂,编号dp01~dp10。
[0140]
(3)供试品制备:取甘遂粉末(过四号筛)0.50g,精密称定,置具塞锥形瓶中,加入乙酸乙酯25ml,密塞,超声处理(功率140w,频率42khz)30分钟,减压滤过,残渣洗涤;合并滤液;滤液蒸干,残渣加甲醇溶解,转移至5ml量瓶中,加甲醇至刻度,摇匀,即得。
[0141]
(4)分别比较了离子阱质谱检测器和三重四极杆检测器、电喷雾电离源(esi)和大气压化学电离源(apci)、正/负离子检测模式,得到了上述质谱检测条件。在上述检测方法下,甘遂整体轮廓图的响应较好。
[0142]
实施例2
[0143]
metalign结合simca-p分析炮制前后整体数据差异
[0144]
⑴
质控样品稳定性分析
[0145]
为监控质谱和色谱柱对样品分离和响应的差异,引入混合对照品作为质控样品,每10次进样,分析一次质控样品。质控样品在样品采集过程中的重复性结果表明,色谱峰的保留时间重现性和峰高偏差均较好,全部样品数据质量符合差异分析的需要。
[0146]
⑵
metalign软件数据处理和导出
[0147]
采用metalign软件导出数据。主要参数设置为峰斜率因子=1;峰阈值因子=2;峰阈值=5000;平均半高峰宽=10;色谱峰集内最小峰数=10。
[0148]
⑶
simca-p分析数据质量(异常值检测)
[0149]
将6个质控数据和50批样品数据进行主成分分析(pca),并绘制前两个主成分的得分图(score plot),观察各组数据的分布情况(见图1左图)。其中数据不进行任何处理。图1左图得分图显示质控样品(control)集中在一个狭小区域,表明质控样品数据偏差较小,整个分析时间内没有对质控样品产生明显影响,同时也表明峰对齐、基线消除等操作适当,未对质控样品产生影响。表明所得全部样品数据具可比性。剔除质控样品,仅对50批样品数据(五种炮制品,每种10份样品)绘制主成分分析得分图(见图1右图),图1右图得分图显示五组样品具有较大的离散性。但所有样品均在界值内,表明整体数据差异较小,可以进行下一步分析。
[0150]
⑷
pls-da/opls-da模型选择(整体数据分析)
[0151]
对于液相-质谱数据的模型建立,常选用pls-da和opls-da。对于pls-da和opls-da,r2y(反映模型对变量的解释程度)和q2(反映模型拟合的程度)越高越好,但二者不能相差0.3以上。
[0152]
表1整体数据差异分析中模型选择——前两个主成分r2y和q2值比较
[0153][0154]
表1数据表明采用parn进行数据变换,采用opls-da建立模型可以最大程度的体现变量对分类的预测。因此数据采用opls-da处理后,绘制前两个和前三个主成分的得分图(见图2)。
[0155]
图2左图提示不同炮制品间均有各自特点,即使市售醋炙品(图2中2)和自制醋炙品(图2中3)也有较大的差异。同时提示自制炮制品和市售炮制品间仍存在一定差异。此外豆腐制品(图2中5)和甘草制品(图2中4)在二维得分图上分离不明显,表明二者最为相似;但引入第三个主成分,绘制为三维得分图后(图2右图),还是能看到二者差异。该图分析结果提示对于中药多组间差异分析,采用opls-da得分图可以更加直观、快速的提示组间是否存在差异。
[0156]
⑸
s-plot图差异分析(整体数据分析)
[0157]
选择各炮制品和生品分别进行差异比较,以parn进行数据变换,以opls-da为模型进行两组间差异分析。以x矩阵的第一载荷因子(p[1])为横坐标,x矩阵与主成分t矩阵的相
关系数(p(crorr)[1])为y坐标进行作图,又称作s-plot。该图定性反映质荷比-保留时间(m/z-rt)数据对差异的贡献程度,其中分布在左下角和右上角的数据是对差异贡献最大的数据。
[0158]
同时计算变量重要性数值(vip,variable importance),该数值定量反映质荷比-保留时间(m/z-rt)数据对分类变量的贡献率,一般大于1即认为与分类有关,即可认为与炮制差异有较大关联。
[0159]
研究结果见图3和表2。s-plot中黑色方块代表炮制后显著降低的成分,而红丝圆点表示炮制后显著升高的成分。图中可以直观发现醋炙品(cp和zp)的s-plot较为对称,表明炮制后降低和升高成分相差不大;而甘草制甘遂(gp)和豆腐制甘遂(dp)的s-plot中降低成分一侧集中了大多数变量,表明这两种炮制品以炮制后成分降低为主。从表2也可以得到类似的结果。
[0160]
表2整体数据差异分析结果:不同炮制品升高/降低峰数(vip》1.0)
[0161][0162]
但我们更关心这些不同炮制品炮制后毒性均降低,其共同降低的成分是什么?
[0163]
⑹
韦恩图分析不同炮制品炮制前后共同变化成分(整体数据分析)
[0164]
采用韦恩图(venny)可以分析不同炮制品炮制后共同变化的成分,从而发现不同炮制方法共同作用的物质基础。
[0165]
韦恩图采用网络在线韦恩图作图软件(http://bioinfogp.cnb.csic.es/tools/venny/index.html)。
[0166]
结果发现(图4),不同炮制品炮制后共同降低成分数明显多于升高成分数。炮制后共有降低成分达到76个,而共有升高只有16个。此外通过韦恩图我们还可以发现市售醋甘遂(cp)和实验室自制醋甘遂(zp)还是有差异,两者共同降低成分仅有86个,二者还有近一半的降低成分不同。豆腐制甘遂(dp)和甘草制甘遂(gp)共同降低成分最多,达到152个。
[0167]
根据韦恩图分析的炮制后共同变化成分的质荷比和保留时间绘制色谱分布示意图(如图5)。从该图中可以非常直观的发现,11min前降低的主要是250~340m/z之间的离子,其后降低离子中可见550~650m/z离子,这些离子保留时间主要在12~18.5min。炮制后升高的离子主要在13~18min。
[0168]
此外共有成分数据(表3和4)显示,共有降低成分中仅有6个成分vip值大于2.0,提示不同炮制品侧重成分不一致,且esi对500~700m/z降低不是非常敏感。
[0169]
表3共有升高成分数据表(整体数据分析)
[0170][0171]
表4共有降低成分数据表(整体数据分析)
[0172][0173]
实施例3:本发明中metalign结合simca-p分析炮制前后局部数据差异
[0174]
上述整体数据差异分析结果发现主要降低差异物质为分子量低于300的物质,这是由于esi-ms对此类物质响应较高的原因。由于更关心分子量在430以上的二萜和三萜物质(分子量426的大戟二烯醇三萜不考虑)。因此对metalign导出的数据,剔除质荷比在430以下的数据进行局部数据差异分析。选择sp,cp,gp和dp四组数据中430~1000m/z离子进行差异分析。排除实验室自制醋炙品。
[0175]
⑴
simca-p分析局部数据质量(异常值检测)
[0176]
分析方法同整体数据分析。由于数据剔除了430m/z以下的高响应物质,需要再次
观察数据异常值情况。以pca得分图作图(选择par数据变换)。从图6可以发现在得分图中没有数据超过临界值,而在dmodx中sp01和cp05显示差异较大,但综合两个图考虑,不进行剔除。
[0177]
⑵
pls-da/opls-da模型选择(局部数据分析)
[0178]
比较pls-da和opls-da和不同的数据归一化方法所得的r2y和q2数值。结果(见表5)表明,选择par数据处理后,采用opls-da模型所得r2y值最高,而q2值在par与parn数据处理中相差不大,考虑到par变换更利于s-plot图分析。因此确定局部数据模型为数据采用par变换后,采用opsd-da建模。
[0179]
表5局部数据差异分析中模型选择——前两个主成分的r2y和q2值比较
[0180][0181]
opls-da二维得分图(见图7左)同样显示该模型下各组数据获得最大分离。豆腐制甘遂和甘草制甘遂与整体数据分析结果一样有重叠,进一步三维得分图显示(见图7右),该两组也能获得较大分离,表明该模型下能够最大程度发现组间差异。该图表明430~1000m/z局部数据在四组间仍有差异,进一步分析能够获得预期的结果。
[0182]
⑶
s-plot图局部数据差异分析
[0183]
同整体数据的s-plot差异分析方法。不同点是,此次s-plot差异分析增加了质荷比和保留时间在s-plot图中的同步显示。以图8为例:第一个图利用vip值,显示了s-plot图中哪些点与两组间差异相关性大。其中红色方块表示的是醋制后降低最多的点,而绿色圆点表示的是醋炙后升高最明显的点。而第二图就在相同s-plot上显示了这些点与质荷比的关系。其中在第一个图右上角降低区域中,分布的主要是500~599m/z的蓝色方块斑点,表明醋制后降低的主要是质荷比500~599的成分;同理升高的主要是质荷比600-699m/z的成分。第三个图进一步回答了这些成分主要分布在色谱图上哪些区域。图上明显标明右上角和左下角均为蓝色方块,表明变化的成分都是色谱图上12min后的物质。通过这三个图可以直观的回答哪些成分是显著升高的,哪些成分是显著降低;降低的这些成分的分子量范围以及在色谱图上保留时间的范围。
[0184]
通过对图8-图10三个s-plot图的分析,对于生甘遂和醋甘遂(sp/cp),可以直观发现降低成分主要为质荷比500~599的物质,而升高成分为600-699m/z的物质,且均为12min后出峰物质。在其它两组间比较中也能观察到类似的情况。不同炮制方法对500~599m/z范围内,12min后物质均有影响。则进一步采用韦恩图分析可以发现共有降低和升高成分。
[0185]
表6显示醋炙品炮制后显著升高和降低的成分相当,而甘草制甘遂和豆腐制甘遂炮制后降低成分显著多于醋甘遂。以豆腐制甘遂炮制后降低成分最多。这些结果与整体分析结果一致。只是峰数明显少于整体数据分析结果。醋甘遂炮制后升高和降低成分数相当,提示降低的成分有可能乙酰化为分子量更高的成分,这也可以从s-图中得到印证。
[0186]
表6 430~500m/z范围不同炮制品升高/降低峰数(vip》1.0,括号内为vip》2.0)
[0187][0188]
⑷
韦恩图分析不同炮制品炮制前后共同变化成分(局部数据分析)
[0189]
对三种炮制品局部数据差异分析得到的炮制后显著变化成分进行韦恩图分析,结果发现(见图11),同整体分析一样,炮制后降低成分数明显多于升高成分数。其中甘草制和豆腐制降低最多。而炮制后共有降低成分达到40个,而共有升高只有11个。
[0190]
从局部数据分析的共有降低成分数据表(表7)中,发现共有降低成分主要是集中在500~600m/z范围内离子,且主要为12min后的洗脱物质。这类物质与甘遂急性毒性部位是一致的(结果未展示)。
[0191]
从共有降低成分炮制前后离子强度均值图(图12)中,可以发现这些离子在炮制前离子强度均较低,没有明显的高含量成分,难以找到代表性的成分进行控制。
[0192]
表7共有降低成分数据表(430~1000m/z局部数据)
[0193][0194]
(注:粗体加下划线的为vip大于2.0;)
[0195]
实施例4:xcms软件可视化分析炮制前后整体数据差异
[0196]
上述采用metalign软件结合simca-p软件进行了甘遂炮制前后整体数据和局部数据的分析。整体数据分析发现炮制品降低最明显的是质荷比300左右的物质;而局部430~1000m/z分析后发现色谱图12min后500~600m/z的物质也有降低。为验证结果的可靠性,采用xcms软件进行再次整体数据分析。
[0197]
采用xcms软件,对质谱源数据直接进行分析。以生甘遂(sp)为炮制前对照,市售醋甘遂(cp)、自制醋甘遂(zp)、甘草制甘遂(gp)和豆腐煮甘遂(dp)分别与生甘遂比较。
[0198]
关键参数为线性对齐,bw=5;fwh=5;minfac=0.1。数据处理中为保证结果一致,采用不同参数进行比较,所得差异图基本一致。图13中下部红色点为炮制后降低或消失的成分,上部绿色点为炮制后升高或出现成分;点的大小代表炮制后差异大小,点越大,表示炮制后该成分含量变化越大;点的颜色代表差异统计p值,颜色越深,表明炮制后,p值越小,差异越显著。纵坐标为m/z,横坐标为色谱保留时间;中间轮廓图为各组样品10批总离子流图叠加图。
[0199]
xcms软件分析结果与metalign软件结合simca-p软件分析结果完全一致;其中xcms online提供的直观图更为直观;而simca-p软件给使用者提供的自主性更大,更利于使用者有针对性的进行分析。
[0200]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0201]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。