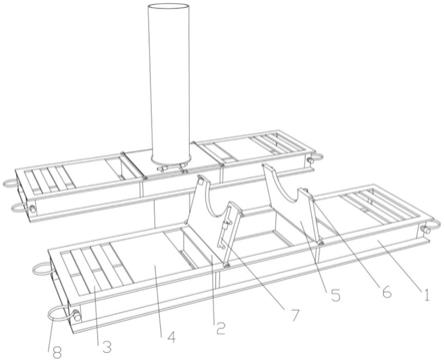
表达针对hmpv的呼吸道合胞病毒蛋白的bcg免疫原性制剂的新用途
发明领域
1.公开了可用于制备针对呼吸道病毒诸如呼吸道合胞病毒(rsv,人正肺病毒(human orthopneumovirus))和/或人偏肺病毒(human metapneumovirush,hmpv)的疫苗的免疫原性制剂,其中该制剂包括至少一种减毒的分枝杆菌(mycobacterium)菌株,优选卡介菌(bacillus calmette-gu
é
rin,bcg)菌株,其重组表达rsv的一种或多种蛋白质或免疫原性片段。
背景技术:
2.在呼吸道病毒中,呼吸道合胞病毒(rsv)和人偏肺病毒(hmpv)因其临床重要性脱颖而出,因为它们可以在婴儿和幼童中引起非常严重的感染。两种病毒的临床表现彼此无法区分,引起广泛范围的临床病例,其可能是轻微的,诸如鼻炎,或者是严重得多的,诸如肺炎或细支气管炎,其中在婴儿、早产儿、患有先天性心脏病的儿童以及在免疫抑制患者中观察到最严重的情况。rsv是全世界婴儿中急性呼吸道感染的主要病原体。根据who,这种病毒每年感染6400万人,其中160,000人死亡。rsv是2岁以下儿童感染和住院的主要原因。(www.who.int)。就人偏肺病毒而言,它是5岁以下儿童中因急性呼吸道感染而住院的第二个主要原因。
3.由这些病毒引起的感染极为频繁且是复发性的,因为实际上100%的3岁以上儿童在5岁时已出现过至少一次rsv和/或hmpv感染经历。因为这些感染不会留下完整的免疫记忆,所以再感染是频繁的,随着患者年龄的增加,严重程度会降低。
4.由这些呼吸道感染造成的健康状况对于受影响的国家具有高的经济影响。在发达国家中进行的研究估计,rsv感染的个人花费超过3,000欧元(大约$2,250,000智利比索),其中上限高达8,400欧元(大约$6,800,000智利比索)。
5.rsv和hmpv两者都被分类于肺病毒科中,该科有两个属,偏肺病毒和正肺病毒。虽然hmpv属于偏肺病毒属,但rsv属于正肺病毒属。
6.两种病毒都含有非分段的负单链rna,具有脂质包膜和相似但不完全相同的组织。rsv具有大约15kb的基因组,具有编码总共11种蛋白质的10种基因。这些蛋白质中的五种具有结构功能,对应于跨膜糖蛋白f、g和sh、核衣壳n蛋白和基质m蛋白。其他四种蛋白质m2-1、m2-2、p和l参与病毒复制和转录。其余的两种蛋白质,称为ns1和ns2,是非结构的,并且与毒力有关。另一方面,hmpv具有大约13kb的基因组,并且包括8种基因,其编码九种蛋白质:n、p、m1、f、m2-1、m2-2、sh、g和l。hmpv不包含ns1和ns2蛋白。n蛋白是rsv和hmpv这两种病毒中最保守的。
7.感染人的rsv具有不同的菌株或亚型,其中亚群a和b是在人群中占主导地位的亚群。亚群之间的主要抗原差异与g蛋白相对应,其在不同亚群之间仅保留40-44%的氨基酸。
8.由于两种病毒之间存在的差异,单一疫苗是否能同时对rsv和hmpv提供保护尚不明显或不可预测。正如我们稍后将详细说明的,本发明的疫苗是包含卡介菌(bcg)菌株的制
剂,浓度在每剂1x104至1x109菌落形成单位之间,它表达呼吸道合胞病毒(rsv)的至少一种蛋白质或免疫原性片段。令人惊讶的是,本发明人发现这种免疫原性制剂赋予了针对rsv和hmpv感染两者的保护。
9.在现有技术中,我们发现了一些为获得针对rsv的疫苗的不成功的尝试。在20世纪60年代进行的尝试包括福尔马林灭活的全病毒(rsv-fi),其在佐剂明矾的存在下肌肉注射给志愿者(1)。与预期相反,在经疫苗接种的儿童中,在自然感染rsv后,这种免疫接种产生了严重得多的呼吸病症,导致80%的疫苗接种者住院,并且其中两人死亡(2)。由疫苗接种者呈现的呼吸-肺图像的特点是罕见的嗜酸性粒细胞和中性粒细胞的浸润,连同高滴度的补体结合抗体(2)。对由于rsv感染而死亡的、用rsv-fi进行疫苗接种的儿童的肺组织的分析示出,在支气管周围区域中沉积了补体、免疫复合物并且存在嗜酸性粒细胞(3)。连同这点,动物模型中的研究示出,用rsv-fi进行疫苗接种产生基于cd4 t淋巴细胞的th2型免疫应答。在感染rsv之前已经用g蛋白进行免疫接种(4)或者已经接受了对这种糖蛋白特异的cd4 t淋巴细胞的动物中观察到了这些相同的特征。
10.在同样的意义上,th2应答不能随着时间的推移赋予针对持续病毒感染的保护,并通过分泌il-5刺激负责过敏反应和炎症高反应性的嗜酸性粒细胞,这甚至可能比病毒感染更危险。在这种类型的th2应答中,t细胞还分泌il-4,这是一种细胞因子,其诱导igg1和ige同种型抗体的生成,抑制igm、igg3、igg2a和igg2b同种型。
11.出于这些原因,针对rsv和hmpv呼吸道病毒的有效且安全的疫苗应基于cd4 t辅助淋巴细胞和分泌干扰素-γ(ifn-γ)的细胞毒性t细胞来生成th1型免疫应答。这种应答能够长期针对这些病毒感染赋予持续的保护,还诱导分泌igg2a同种型抗体的b细胞的增殖和分化,并抑制igg3、ige、igg2b和igg1同种型免疫球蛋白的产生。
12.针对rsv疫苗的当前研究已集中于分析和开发病毒亚单位,诸如f蛋白(5)、m2(6)以及g蛋白的一些保守片段(7)。另一方面,还已研究了基于rsv突变体菌株的疫苗的生成,该rsv突变体菌株诸如为对于温度敏感的(8)、在某些基因中具有缺失(9)或者关于细胞因子诸如gm-csf而言重组的(10)那些。其中一些疫苗已在i期和ii期临床试验中进行了测试,结果各不相同(11-13)。另一类针对rsv的试验性疫苗是基于蛋白f和g的疫苗,其用佐剂诸如iscom进行施用。用这种类型的疫苗进行免疫接种会针对新病毒感染在肺组织中产生增加的嗜酸性粒细胞的浸润(14),这会增加肺组织中的损伤。
13.婴儿免疫系统的特点是优先发展出th2-型免疫应答,这可能是由于在生命的前六个月期间免疫系统未成熟(15、16)。然而,如果经适当的刺激,它可以产生th1-型应答(17)。为了配制针对rsv和/或hmpv的有效且安全的疫苗,发明人已经对针对不同rsv蛋白质生成的免疫应答进行了充分研究,以便鉴定基于细胞毒性t淋巴细胞允许生成th1-型免疫应答的那些。使用细菌载体来异源表达病毒抗原具有下述优点,即它们可以用作活的减毒的载体,因为它们具有完整的侵袭能力并且公认是非病原性的。用于表达异源抗原的某些细菌载体的额外优点是它们公认的诱导th1-型免疫性的能力(18、19),这对于疫苗开发的情况非常有吸引力。卡介菌(bcg)是减毒的牛分枝杆菌(mycobacterium bovis)菌株,其被用作针对新生儿中的结核分枝杆菌(mycobacterium tuberculosis)的疫苗。从bcg被批准作为结核病疫苗以来,它已被提供给全世界超过33亿人。通过这种细菌的许多有利特点,诸如它在冻干形式下的高热稳定性,促进了它的大规模使用。此外,用这种细菌对新生婴儿进行免
疫接种是没有风险的,并且仅产生最低限度的副作用。关于bcg回复毒力的安全性和稳定性,在其被使用的多年来一直没有观察到。bcg是高度免疫原性的,并且只需一剂即可产生长期维持的免疫应答。重要的是,bcg在成人和儿童两者中均能诱导强有力的th1-型免疫应答(20)。在新生儿中通过针对结核分枝杆菌抗原(ppd)而生成的细胞类型免疫应答而证明了这种现象,这种应答能够维持很长时期(20)。
14.迄今为止,已在这种细菌系统中成功表达了几种细菌、寄生物和病毒抗原,当在动物模型中进行评价时,这被证明能够生成针对这些抗原的体液和细胞免疫(21、22)。另外,bcg具有不被母乳中存在的抗体中和的特性,因此它可以在哺乳中的儿童中用作免疫诱导剂(22)。本发明涉及免疫学制剂,其包含对于rsv蛋白质而言一种或多种减毒的重组的分枝杆菌细菌菌株,优选bcg菌株,并且可以用于制备针对呼吸道病毒尤其是rsv和hmpv的疫苗。
15.由于生成了用于消除病毒的有效和有利的免疫应答,本发明的制剂可以避免或减弱由呼吸道病毒rsv和hmpv感染引起的肺损伤。因为减毒的分枝杆菌菌株诸如bcg是强有力的th1-型免疫应答诱导剂,所以由对于rsv而言重组的bcg菌株诱导的免疫应答提供了针对由这两种病毒引起的感染的保护。
技术实现要素:
16.本发明包括免疫原性制剂,其在哺乳动物中诱导针对由呼吸道病毒引起的感染尤其是由呼吸道合胞病毒(rsv)和/或人偏肺病毒(hmpv)引起的感染的保护,或至少减弱由这些病毒引起的病理学状态。本发明的免疫原性制剂可用于制备疫苗,并且包含数个菌落形成单位(cfu)的活的减毒的重组的分枝杆菌菌株,优选卡介菌(bcg)菌株,所述菌株重组地或异源地表达呼吸道合胞病毒的一种或多种蛋白质或免疫原性片段。
17.这些rsv的蛋白质或免疫原性片段对应于rsv a或rsv b亚型的rsv ns1、ns2、n、p、m、sh、m2(orf1)、m2(orf2)、l、f或g蛋白,并且被发现以一个或多个拷贝插入到减毒的分枝杆菌菌株的细菌基因组中或染色体外质粒中,并且它们的表达受内源性或外源性、组成型或诱导型bcg启动子控制。这些rsv的蛋白质或免疫原性片段可以由bcg或其他减毒的分枝杆菌菌株表达为胞质可溶形式、分泌至细胞外的或与细胞膜结合的蛋白质。
18.本发明中公开的免疫原性制剂可以连同包含其他减毒的分枝杆菌或bcg菌株并且在下列方面不同的免疫原性制剂一起使用:它们表达的免疫原性rsv蛋白质,以及基因定位(插入到基因组中或者处于染色体外),蛋白质基因的拷贝数,诱导蛋白质表达的启动子,或者rsv免疫原性蛋白质或片段的目的地(胞质可溶的、分泌至细胞外的或与细胞膜结合的蛋白质)不同。
19.上述免疫原性制剂可用于制备疫苗,该疫苗可以与缓冲或生理盐水溶液一起皮下、经皮或真皮下施用给个体。
20.本发明的免疫原性制剂可以用于对之前已接触过或未接触过呼吸道合胞病毒或人偏肺病毒的个体进行疫苗接种,以赋予针对呼吸道病毒诸如rsv和/或hmpv的保护。
附图说明
21.图1示出了来自用表达n蛋白的于盐水溶液((pbs:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,在4℃下)中的bcg进行免疫接种的balb/c
小鼠的脾细胞的cd8 /cd69 细胞百分比(a)和(b)ifn-γ分泌。将来自动物的脾的5x105个细胞用0.5μm的rsv n蛋白刺激72小时,所述动物未经免疫接种,用1x10
7 pfu的rsv进行免疫接种,用bcg(1x10
8 cfu/小鼠在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,4℃)进行免疫接种,或用对于rsv n蛋白而言重组的bcg(1x10
8 cfu/小鼠在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温800.02%ph 7.4,4℃)进行免疫接种。随后,通过流式细胞术测定关于cd8和cd69标志物而言阳性的细胞百分比(a)。对细胞上清液进行elisa以检测分泌的ifn-γ的存在。(b)**,p值0.002,学生t检验。可以得出结论,对于rsv n蛋白而言重组的bcg菌株在用这种免疫原性制剂免疫接种的小鼠中产生了有利的t淋巴细胞应答。
22.这些结果示出,在用对于rsv n蛋白而言重组的bcg的免疫接种的应答中,这些cd8 t淋巴细胞被激活,因为它们在其表面表达激活标志物(cd69
)并向细胞外介质分泌ifn-γ,这证明了本发明的疫苗生成了th1型免疫应答。
23.图2示出了用表达rsv n蛋白的重组bcg菌株(1x10
8 cfu/小鼠,在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,4℃)或用对于rsv m2蛋白而言重组的bcg菌株(1x10
8 cfu/小鼠,在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,4℃)进行免疫接种的balb/c小鼠的体重变化曲线。用1x10
7 pfu的rsv,菌株13018-8,经鼻内感染balb/c小鼠,所述balb/c小鼠未经疫苗接种(
■
);用1x107噬斑形成单位(pfu)的经20分钟uv灭活的rsv(uv灯,312nm,功率8瓦特)(rsv-uv)进行免疫接种用不表达rsv的野生bcg(wt)菌株(1x10
8 cfu/小鼠,在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,4℃)进行免疫接种用由pmv361-n转化的bcg菌株(1x10
8 cfu/小鼠,在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,4℃)进行免疫接种(
□
);或者用由pmv361-m2转化的bcg菌株(1x10
8 cfu/小鼠,在pbs中:137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,吐温80 0.02%ph 7.4,4℃)进行免疫接种(
△
)。作为对照,包括未经疫苗接种且未感染的小鼠的组(
●
)。每天记录相对于第0天的体重变化,持续4天。**,p值0.002,学生t检验。
24.可以得出结论,用对于rsv n或m2蛋白而言重组的bcg菌株进行的小鼠免疫接种产生了有利的针对rsv感染的应答,因为当与其中在感染后观察到体重减少的未经疫苗接种的小鼠的体重相比较时,这些小鼠的体重在感染后没有显著变化。
25.图3-a示出了来自以下四个实验组的balb/c小鼠的支气管肺泡灌洗中cd11c-/cd11b
/gr1
细胞的百分比:未经免疫接种且未感染,未经免疫接种并用1x107的hmpv菌株cz0107经鼻内感染,用对于rsv n蛋白而言重组的bcg免疫接种的小鼠(1x10
8 cfu/小鼠),以及用对于hmpv p蛋白而言重组的bcg免疫接种的小鼠(1x10
8 cfu/小鼠)。
26.观察到用对于hmpv的p蛋白和rsv的n蛋白而言重组的bcg菌株免疫接种的组示出比未经免疫接种的感染组显著更少的多形核浸润。
27.图3-b示出了所研究的四组的肺中cd11c-/cd11b
/gr1
细胞的百分比。
28.如之前的实例中,观察到用对于hmpv的p蛋白和rsv的n蛋白而言重组的bcg菌株免疫接种的组示出比未经免疫接种的感染组显著更少的炎症细胞浸润。可以看出,用对于
hmpv p而言重组的bcg免疫接种的组甚至示出与未感染对照组(1)相似的结果。
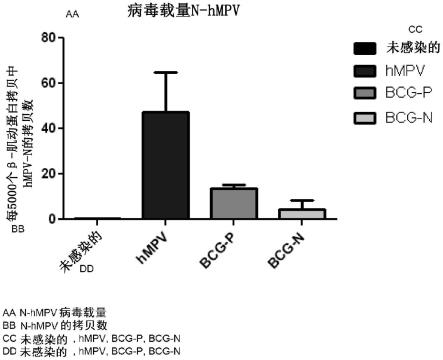
29.图4示出了通过qpcr评价四个研究组的肺组织中的病毒载量,表示为每5000个β-肌动蛋白拷贝中hmpv n蛋白的拷贝数目。
30.观察到用对于hmpv p蛋白而言重组的bcg菌株和用对于rsv n而言重组的bcg进行免疫接种的组均比未经免疫接种的感染组具有显著更低的病毒载量。
31.图5示出在三个不同的时间点:第0天(免疫接种前)、第21天(病毒攻击前)和感染后第14天,在用重组bcg-n疫苗进行免疫接种的动物的血浆中通过elisa评价的针对rsv的特异性抗体水平(以o.d.450nm表示)。
32.结果示出,用bcg-n免疫接种的动物甚至在病毒攻击之前就产生了抗rsv抗体。在用rsv攻击后,与对照组相比,在用bcg-n免疫接种的动物组中针对病毒的特异性igg免疫球蛋白的水平显著更高。
33.图6示出了通过elisa评价的在来自经免疫接种和未经免疫接种的动物的血清中,由重组bcg-n疫苗诱导的针对rsv的特异性抗体的同种型特征,以o.d.450nm表示。通过在三个不同时间的针对igg2a(图6a)或igg1(图6b)的特异性第二抗体分析免疫球蛋白的同种型。图6c示出了在感染后第14天来自通过elisa获得的数据的igg2a比igg1的o.d.450nm的比率。结果表明,在用本发明bcg n的疫苗免疫接种的动物中,感染后同种型igg2a/igg1的抗rsv免疫球蛋白的比率更高。
34.图7示出了在hep-2细胞中的rsv-gfp血清中和测定。图7a将预先在37℃下温育1小时的hep-2细胞用血清和rsv-gfp的混合物处理,并且在48小时后在落射荧光显微镜下将它们可视化。图7b通过显微术可视化的噬斑形成单位(pfu)的量化。图7c通过流式细胞术量化hep-2细胞中的gfp表达。b和c中缺失的条形表明在经处理的细胞中未检测到病毒gfp。
35.显然,通过用本发明的疫苗进行免疫接种而产生的抗体能够在体外降低rsv感染,因此这些免疫球蛋白具有对抗呼吸道合胞病毒的中和功能。
36.图8示出了在两个不同的时间:第-21天(病毒攻击前)和感染后第7天,在用重组疫苗bcg-n、bcg-p进行免疫接种的以及未经免疫接种和未感染的对照(空白)的动物血浆中,针对hmpv的特异性抗体的水平(以o.d.450nm表示)。
37.结果示出,用对于rsv n蛋白而言重组的bcg进行的免疫接种在病毒攻击之前和之后诱导针对hmpv的特异性igg水平升高,与用对于hmpv的p而言重组的bcg进行的免疫接种的比例相同。
具体实施方式
38.本发明包括可以用于制备疫苗的免疫原性制剂,该疫苗在哺乳动物中诱导针对由呼吸道病毒尤其是呼吸道合胞病毒和/或人偏肺病毒引起的感染的保护,或减弱由这些病毒引起的病理学状态。本发明的疫苗包含活的减毒的重组的分枝杆菌菌株,优选卡介菌(bcg),例如重组地或异源地表达一种或多种rsv的蛋白质或免疫原性片段的bcg danish或pasteur菌株。本发明的疫苗包括每剂1x10
4-1x10
9 cfu(菌落形成单位)的所述菌株,并且可以在施用前以冻干形式或冷稳定盐水溶液保存。
39.用于本发明的免疫原性制剂或疫苗的合适的稳定剂溶液的实例是:
[0040]-在4℃下的sauton ssi稀释溶液(125μg mgso4、125μg k2hpo4、1mg l-天冬酰胺、
12.5μg柠檬酸铁铵、18.4mg 85%甘油、0.5mg柠檬酸,在1ml的h2o中)。
[0041]-在-80℃下补充有0.02%吐温80和20%甘油的pbs(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4),或者
[0042]-体积溶液:25%体积乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(proskauer and beck's medium)(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升蒸馏水),冻干并在4℃至25℃的温度范围下储存。
[0043]
本发明的免疫原性制剂的减毒的重组的分枝杆菌细菌包含编码rsv a或rsv b亚型或者两者的至少一种rsv蛋白质或免疫原性片段的基因。呼吸道合胞病毒基因组先前已在genebank数据库中描述,登录号为nc_001803和nc_001781。
[0044]
其中,本发明的编码rsv a或rsv b亚型或者两者的至少一种rsv蛋白质或免疫原性片段的基因与所述基因库公开的序列中描述的基因(登录号为nc_001803和nc_001781)具有至少80%的同一性。
[0045]
rsv免疫原性蛋白质或片段对应于rsv ns1、ns2、n、p、m、sh、m2(orf1)、m2(orf2)、l、f或g蛋白。在优选的实施方式中,免疫原性蛋白质或片段对应于rsv的n、p、m、sh、m2(orf1)、m2(orf2)、l、f或g。
[0046]
为了获得本发明的重组菌株,将编码这些蛋白质或其免疫原性片段的基因插入到质粒中,将质粒通过任何可用的技术掺入细菌中。在一种实施方式中,使用质粒pmv361,将质粒pmv361通过电转化掺入到细菌中,并通过分枝杆菌噬菌体整合酶的作用而整合到细菌基因组中(23)。这些基因也可以插入到染色体外质粒诸如pmv261中,其通过电转化掺入分枝杆菌中并在细菌中保持在染色体外(23)。这些基因可以是一个或多个拷贝,并且它们的表达受bcg的组成型或诱导型内源启动子(例如分别为hsp60基因的启动子和acr基因的启动子)的控制。这些rsv的蛋白质或免疫原性片段可以由bcg或其他减毒的分枝杆菌菌株表达为胞质可溶的方式、分泌至细胞外的或作为与细胞膜结合的蛋白质,这是由于将呼吸道合胞病毒基因或免疫原性片段与编码充当朝向不同细菌区室的蛋白质的靶向信号的肽的dna序列相融合,例如,α-抗原基因的n-末端序列,其用于细胞外分泌,以及19kd蛋白基因的n-末端序列,其用于膜结合蛋白。
[0047]
本发明中公开的免疫原性制剂可以连同包含一种或多种减毒的分枝杆菌或bcg菌株并且在下列方面不同的免疫原性制剂一起使用:它们表达的免疫原性rsv蛋白质,以及基因定位(插入到基因组中或者处于染色体外),蛋白质基因的拷贝数,诱导蛋白质表达的启动子,或者rsv免疫原性蛋白质或片段的靶标(胞质可溶的、分泌至细胞外的或与细胞膜结合的蛋白质)不同。
[0048]
发明人已经示出,本发明的疫苗诱导th1型免疫应答,其包括产生igg2a同种型抗体的b淋巴细胞和有效的产生ifn-γ的t淋巴细胞应答两者。这保证了针对这些呼吸道病毒的体液保护以及增强本发明的免疫原性制剂的有效性和适用性两者的有效细胞应答。
[0049]
可以将本发明的疫苗与缓冲或生理盐水溶液一起皮下、经皮或真皮下施用给个体。
[0050]
如所指示的,本发明的免疫原性制剂可以用于对之前已接触过或未接触过呼吸道病毒诸如呼吸道合胞病毒或人偏肺病毒的个体进行疫苗接种,以在未来赋予针对这些呼吸
nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中,并将它们在-20℃下储存。以同样的方式,可以将菌株重悬浮于体积溶液:25%乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升蒸馏水),然后冻干并在4℃下储存。
[0059]
通过电转化(24)用衍生自质粒pmv361的质粒pmv361/n或pmv361/m2(25)转化danish bcg菌株,所述质粒仅插入到细菌基因组中一次。这些质粒分别包含rsv亚型a蛋白n和m2的基因,处于bcg hsp60基因的组成型启动子下。使所得到的重组体菌落在37℃下在补充的middlebrock 7h9培养基中生长直到od
600nm
=1,将它们在4000rpm下离心20min(eppendorf转子5702/r a-4-38型),并且以107个细菌/100μl的终浓度重悬浮在补充有20%甘油和0.02%吐温80的pbs(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)溶液中,并在-20℃下储存。以同样的方式,可以将菌株重悬浮于体积溶液:25%乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升蒸馏水),然后冻干并在4℃下储存。通过蛋白质印迹,使用rsv蛋白n和m2的抗体,发明人观察到这些bcg danish菌株重组地表达rsv亚型a蛋白n和m2。该免疫原性制剂能够赋予同时针对rsv亚型a和b的m2和n蛋白的免疫性。
[0060]
实施例iii:由106个对于rsv亚型b的f蛋白的片段而言重组的pasteur bcg菌株的细菌组成的免疫原性制剂。
[0061]
该基因以多个拷贝(2-4个拷贝/细菌)以染色体外形式存在于细菌中,并且编码rsv亚型b蛋白f的片段(从氨基酸5至200范围的片段)。该基因的表达受编码bcg的α-抗原蛋白(85kd)的基因的组成型内源性启动子的控制。此外,由该基因编码的蛋白质在其n末端具有bcg的19kda蛋白的肽信号hmkkrgltvavagaailvaglsgcssnksttgsgettttaagttaspgg该肽信号诱导该蛋白在细菌膜中表达。该免疫原性制剂在补充有0.02%吐温80和20%甘油的pbs(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中于-80℃下保存。以同样的方式,可以将菌株重悬浮于体积溶液:25%乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升蒸馏水),然后冻干并在4℃下储存。
[0062]
通过电转化(24)用衍生自质粒pmv261的质粒pmv261/f
5-200
(25)转化pasteur bcg菌株,所述质粒以多个拷贝以染色体外形式位于细菌内。该质粒编码在其n-末端处与bcg的19kd蛋白的下述信号肽相融合的rsv亚型b的f基因的片段(从氨基酸5至200的区段):hmkkrgltvavagaailvaglsgcssnksttgsgettttaagttaspgg该肽信号诱导该蛋白在细菌膜中表达。该基因的表达受编码bcg的α抗原蛋白(85kd)的基因的组成型内源性启动子的控制。使所得到的重组体菌落在37℃下在补充的middlebrock 7h9培养基中生长直到od
600 nm
=1,并在4,000rpm下离心20min(eppendorf转子5702/ra-4-38型),并且以106个细菌/100μl的终浓度重悬浮于补充有0.02%吐温80和20%甘油的pbs(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中。以同样的方式,可以将菌株重悬浮于体积溶液:25%体积乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升蒸馏水),然后以每份106个细菌的等分试样进行冻干并在25℃下储存。该免疫原性制剂能够赋予针对rsv亚
型a和b的f蛋白的免疫性。
[0063]
实施例iv:由105个同时对于rsv亚型a的n和m2基因而言重组的danish bcg菌株的细菌组成的免疫原性制剂。
[0064]
将n基因以单个拷贝插入到细菌基因组中,受bcg的组成型内源性hsp60启动子的调控,并且以胞质方式表达出蛋白质。m2基因以多个拷贝(2-4个拷贝/细菌)以染色体外形式存在于细菌中,处于编码bcg的α抗原蛋白(85kd)的基因的组成型内源性启动子的控制下。由m2基因编码的蛋白质在其n末端具有bcg的19kda蛋白的肽信号hmkkrgltvavagaailvaglsgcssnksttgsgettttaagttaspgg该肽信号诱导该蛋白在细菌膜中表达。将该免疫原性制剂保存于4℃,由重悬浮于体积溶液:25%乳糖以及补充有葡萄糖和tween 80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升冻干的蒸馏水)的细菌进行冻干,在4℃下储存。相似地,该菌株以105个细菌/100μl的终浓度保存在补充有0.02%吐温80和20%甘油的pbs溶液(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中。
[0065]
通过电转化(24)用衍生自质粒pmv361的质粒pmv361/n(25)转化danish bcg菌株,所述质粒仅插入到细菌基因组中一次。该质粒包含编码rsv n蛋白亚型a的基因,该基因在bcg hsp60基因的内源性和组成型启动子下表达。在证实所得到的bcg菌株对于rsv n蛋白而言是重组的之后,通过电转化(24)用衍生自pmv206质粒的质粒pmv206/m2(25)转化该bcg菌株,所述质粒以多个拷贝以染色体外形式位于细菌内。由m2基因编码的蛋白质在其n末端具有bcg的19kd蛋白的肽信号hmkkrgltvavagaailvaglsgcssnksttgsgettttaagttaspgg该肽信号诱导该蛋白在细菌膜中表达。使所得到的重组体菌落生长(在37℃下在补充的middlebrock 7h9培养基中)直到od
600nm
=1,在4,000rpm下离心20min(eppendorf转子5702/ra-4-38型)并以105个细菌/1ml的终浓度重悬浮于体积溶液:25%乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80;和10.0g葡萄糖/升蒸馏水)中。最后,将具有105个细菌的1ml等分试样冻干,并将等分试样在4℃下储存。相似地,该菌株以105个细菌/100μl的终浓度保存在补充有0.02%吐温80和20%甘油的pbs溶液(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中。该免疫原性制剂能够赋予针对rsv亚型a和b的n和m2蛋白的免疫性。
[0066]
实施例v:由104个对于rsv亚型a的n基因而言重组的danish bcg菌株的细菌组成的免疫原性制剂。
[0067]
该基因以单个拷贝插入到细菌基因组中,受bcg的内源性诱导型acr启动子的调控,该启动子响应于一氧化氮、低氧浓度和生长静止期而具有活性。该蛋白质的表达是细胞质的。该免疫原性制剂由以下体积溶液进行冻干:25%体积乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80和10.0g葡萄糖/升蒸馏水),在25℃下储存在稀释的sauton ssi溶液(125μg mgso4、125μg k2hpo4、1mg l-天冬酰胺、12.5μg柠檬酸铁铵、18.4mg 85%甘油、0.5mg柠檬酸于1ml的h2o中)中。相似地,该菌株以104个细菌/100μl的终浓度保存在补充有0.02%吐温80和20%甘油的pbs溶液(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中。
[0068]
通过电转化(24)用衍生自质粒pmv361的质粒pmv361
pacr
/n(25)转化danish bcg菌株,所述质粒仅插入到细菌基因组中一次。该质粒包含编码rsv n蛋白亚型a的基因,该基因在bcg acr基因的内源性和组成型启动子下表达(26)。使所得到的重组体菌落生长(在37℃下在补充的middlebrock7h9培养基中)直到od
600nm
=1,在4,000rpm下离心20min(eppendorf转子5702/ra-4-38型)并重悬浮于体积溶液:25%乳糖以及补充有葡萄糖和吐温80的proskauer和beck培养基(pbgt:0.5g天冬酰胺;5.0g磷酸二氢钾;1.5g柠檬酸镁;0.5g硫酸钾;0.5ml吐温80;和10.0g葡萄糖/升蒸馏水)中。最后,将具有104个细菌的1ml等分试样冻干,并在25℃下储存。相似地,该菌株以108个细菌/100μl的终浓度保存在补充有0.02%吐温80和20%甘油的pbs溶液(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中。该免疫原性制剂能够赋予针对rsv n蛋白亚型a和b的免疫性。
[0069]
实施例vi:由109个对于rsv亚型a的n基因而言重组的danish bcg菌株的细菌组成的免疫原性制剂。
[0070]
该基因以单个拷贝插入到细菌基因组中,受共表达噬菌体t7的聚合酶的bcg菌株中组成型表达的噬菌体t7的外源性启动子的调控。该蛋白质的表达是细胞质的。免疫原性制剂在稀释的sauton ssi溶液(125μg mgso4、125μg k2hpo4、1mg l-天冬酰胺、12.5μg柠檬酸铁铵、18.4mg 85%甘油、0.5mg柠檬酸在1ml的h2o中)中并在-20℃下储存,或可以将免疫原性制剂冻干并在4℃下储存。相似地,该菌株以109个细菌/100μl的终浓度保存在补充有0.02%吐温80和20%甘油的pbs溶液(137mm nacl;2.7mm kcl;4.3mm na2hpo4;1.47mm kh2po4,ph 7.4)中。
[0071]
通过电转化(24)用衍生自质粒pmv361的质粒pmv361
pt7
/n(25)转化danish bcg菌株,所述质粒仅插入到细菌基因组中一次。该质粒包含编码rsv n蛋白亚型a的基因,其在通过噬菌体t7聚合酶的表达而被激活的t7启动子下表达(27)。
[0072]
通过电转化(24)用衍生自质粒pmv261的质粒pmv261
amp
/polt7(25)转化所得到的bcg菌株,所述质粒以多个拷贝以染色体外形式位于细菌内。在该质粒中,针对抗生素卡那霉素(27)的抗性已被针对抗生素潮霉素(higr)的抗性替代。噬菌体t7的t7聚合酶受bcg hsp60基因的组成型启动子的控制。使所得到的重组体菌落在37℃下在补充的middlebrock 7h9培养基中生长直到od
600nm
=1,在4000rpm下离心20min(eppendorf转子5702/ra-4-38型),并且重悬浮于稀释的sauton ssi溶液(125μg mgso4、125μgk2hpo4、1mg l-天冬酰胺、12.5μg柠檬酸铁铵、18.4mg 85%甘油、0.5mg柠檬酸于1ml的h2o中)中,并在-80℃下储存。该免疫原性制剂能够赋予针对rsv n蛋白亚型a和b的免疫性。
[0073]
实施例vii:来自rsv bcg-n的针对hmpv感染的保护。
[0074]
为了确定本发明的疫苗提供针对人偏肺病毒(hmpv)的保护,预先用本发明的疫苗之一或用针对hmpv感染有效的对于hmpv的p蛋白而言重组的bcg疫苗对小鼠进行免疫接种。将这些结果与感染hmpv而没有预先免疫接种的小鼠和未感染的小鼠进行比较。
[0075]
实验组,每组3只小鼠,如下:
[0076]
1)对照,未感染,未经免疫接种
[0077]
2)感染hmpv而没有免疫接种
[0078]
3)用hpmv bcg-p免疫接种,感染hmpv
[0079]
4)用rsv bcg-n免疫接种,感染hmpv
[0080]
首先,通过流式细胞仪分析4组中肺和支气管肺泡灌洗(bal)中多形核细胞的浸润,确定cd11c-/cd11b
/gr1
多形核细胞的百分比。这些细胞的存在与对病毒感染的炎症反应直接相关。图3-a示出了研究的四组的bal中cd11c-/cd11b
/gr1
细胞的百分比。观察到,用bcg-p和bcg-n免疫接种的组示出的炎症反应比未经免疫接种的感染组显著更低。
[0081]
图3-b示出了研究的四组的肺中cd11c-/cd11b
/gr1
细胞的百分比。与先前实例一样,观察到用bcg-p和bcg-n免疫接种的组示出的炎症细胞的浸润比未经免疫接种的感染组显著更低。可以看出,用bcg-p免疫的第3组示出与未感染组(1)相似的结果。
[0082]
其次,通过定量pcr(qpcr)测定4组的肺组织中的病毒载量(图4),表示为每5,000个β-肌动蛋白拷贝中hmpv n蛋白的拷贝数目。据观察,免疫组具有的病毒载量比未经免疫接种的感染组显著更低。
[0083]
可以理解的是,本发明的疫苗提供了与重组bcg疫苗对相同hmpv病毒的蛋白(在本实例中为p蛋白)所给予的保护类似的针对hmpv感染的保护。
[0084]
实施例viii:bcg rsv-n疫苗诱导体液应答
[0085]
为了确定本发明的疫苗诱导th1型应答,6至8周龄的balb/cj小鼠接受背部皮下注射1x10
8 cfu的bcg wt或表达rsv-n蛋白的重组bcg,以每剂终体积100μl。14天后,它们接受具有相同起始剂量的加强剂(booster)。在第一次注射bcg wt或bcg-n的21天后,使用从临床分离物中获得的rsv a2菌株13018-8,对动物进行攻击。在病毒攻击前(第21天)和感染后14天获得免疫接种前血清样品(第0天)。通过elisa以1/500稀释度分析这些样品。结果示出,用bcg-n免疫接种的动物甚至在病毒攻击之前的阶段就产生抗rsv抗体,这一产生比未经免疫接种的对照和用bcg wt免疫接种的动物显著更高。在用rsv攻击后,针对病毒的特异性igg免疫球蛋白水平示出甚至更大的增加,这种增加在感染后第14天仍保持(图5)。
[0086]
为了确立由免疫产生的免疫球蛋白的同种型,通过elisa分析在测试动物血清中rsv特异性igg1和igg2a同种型抗体的水平。从感染后第7天起,与对照动物(包括用野生型bcg进行疫苗接种的动物和未经免疫接种的动物)相比,在用本发明的bcg rsv-n疫苗免疫接种的动物中观察到igg2a同种型抗体的产生更加显著地增加。另一方面,igg1同种型抗rsv免疫球蛋白示出在感染前用bcg-n进行疫苗接种的动物中增加,然而,rsv对照组和用bcg wt进行疫苗接种的动物在病毒攻击后第14天已经设法匹配它们的产生(图6-a、6-b)。后者在图6-c中得到更好的证明,其中,示出用本发明的bcg rsv-n疫苗免疫接种的动物中igg2a/igg1同种型的抗rsv免疫球蛋白的比率高于仅感染rsv的对照组。正如我们已经指出的那样,这种关系表明免疫应答极化为th1表型。
[0087]
为了确定由疫苗接种诱导的体液应答是否能够保护以免受rsv感染,在灭活补体后,在感染后第14天和病毒攻击前将rsv-gfp病毒与来自所有实验组的动物的血清一起温育,并然后用这些混合物感染hep-2细胞。在图7中,在落射荧光显微图像中,观察到与其他处理相比,预先用来自用bcg-n免疫接种的动物的血清处理的细胞中rsv-gfp的表达降低。当量化噬斑形成单位时,仅在用来自用bcg-n免疫接种的动物的感染后第14天的血清进行的处理中(图7-b),证明了该参数的显著降低,并且当通过流式细胞术分析rsv-gfp的表达时,证实了同样的趋势(比较图7-c和7-b)。
[0088]
实施例ix:在用rsv bcg-n免疫接种的动物中产生抗hmpv igg抗体。
[0089]
为了评价针对hmpv的特异性免疫球蛋白的产生,从用该病毒攻击并预先用本发明
murine airway mucosa with an attenuated salmonella live vaccine expressing oprf-opri from pseudomonas aeruginosa.infect.immun.72:6546.
[0110]
19.dhar,n.,v.rao,and a.k.tyagi.2003.skewing of the th1/th2 responses in mice due to variation in the level of expression of an antigen in a recombinant bcg system.immunol lett 88:175.
[0111]
20.marchant,a.,t.goetghebuer,m.o.ota,i.wolfe,s.j.ceesay,d.degroote,t.corrah,s.bennett,j.wheeler,k.huygen,p.aaby,k.p.mcadam,and m.j.newport.1999.newborns develop a th1-type immune response to mycobacterium bovis bacillus calmette-guerin vaccination.j immunol163:2249.
[0112]
21.cirillo,j.d.,c.k.stover,b.r.bloom,w.r.jacobs,jr.,and r.g.barletta.1995.bacterial vaccine vectors and bacillus calmette-guerin.clin infect dis20:1001.
[0113]
22.fennelly,g.j.,j.l.flynn,v.ter meulen,u.g.liebert,and b.r.bloom.1995.recombinant bacille calmette-guerin priming against measles.j infect dis 172:698.
[0114]
23.23 stover,c.k.,v.f.de la cruz,t.r.fuerst,j.e.burlein,l.a.benson,l.t.bennett,g.p.bansal,j.f.young,m.h.lee,g.f.hatfull,and et al.1991.new use of bcg for recombinant vaccines.nature 351:456.
[0115]
24.kumar,d.,b.s.srivastava,and r.srivastava.1998.genetic rearrangements leading to disruption of heterologous gene expression in mycobacteria:an observation with escherichia coli beta-galactosidase in mycobacterium smegmatis and its implication in vaccine development.vaccine16:1212.
[0116]
25.purkayastha,a.,l.a.mccue,and k.a.mcdonough.2002.identification of a mycobacterium tuberculosis putative classical nitroreductase gene whose expression is coregulated with that of the acr aene within macrophages,in standing versus shaking cultures,and under low oxygen conditions.infect immun 70:1518.
[0117]
26.yoon,y.g.,and m.d.koob.2005.transformation of isolated mammalian mitochondria by bacterial conjugation.nucleic acids res 33:e139.
[0118]
27.ahmed,s.u.,m.okamoto,t.oshikawa,t.tano,a.sasai,s.kan,t.hiroshima,h.ohue,y.moriya,y.ryoma,m.saito,and m.sato.2004.anti-tumor effect of an intratumoral administration of dendritic cells in combination with ts-1,an oral fluoropyrimidine anti-cancer drug,and ok-432,a streptococcal immunopotentiator:involvement of toll-like receptor 4.jimmunother 27:432。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。