原苏木素b在制备解热药物中的应用
技术领域
1.本发明涉及植物医药技术领域,特别是涉及原苏木素b在制备解热药物中的应用。
背景技术:
2.发热是由感染性疾病和非感染性疾病引起的体温超过正常范围的症状,是临床最为常见疾病症状之一。研究报道民间习用药材云实具有一定的解热作用。云实[caesalpinia decapetala(roth)alston]为豆科(leguminosae)云实属(caesalpinia l.)植物,药用部位为根、茎、果,具有清热除湿的功效。云实具有丰富多样的化学成分,主要含有黄酮类、萜类、苯丙酸类、甾体类和酚类化学成分。目前,还尚不清楚云实中主要起解热作用的是何种化合物。对云实中的活性化合物进行分离鉴定和药理活性方面的研究,对提高云实的有效应用具有重要的意义。
技术实现要素:
[0003]
本发明的目的是提供原苏木素b在制备解热药物中的应用,以解决上述现有技术存在的问题,本发明通过对云实中的活性化合物进行分离鉴定和作用研究证明,云实中的原苏木素b具有明显的解热作用。
[0004]
为实现上述目的,本发明提供了如下方案:
[0005]
本发明提供原苏木素b在制备解热药物中的应用。
[0006]
本发明还提供一种从云实中提取原苏木素b的方法,包括:对云实进行乙醇回流提取后,浓缩得到总浸膏,所述总浸膏经过减压硅胶柱色谱分离得到第一粗品,所述第一粗品经过聚酰胺树脂分离得到第二粗品,所述第二粗品经过反相ods柱色谱分离,提取得到所述原苏木素b的成品。
[0007]
进一步地,所述乙醇回流的具体操作包括:先用乙醇浸泡12小时,之后在60℃条件下回流提取3小时,重复提取3次。
[0008]
进一步地,所述浓缩为减压浓缩。
[0009]
进一步地,所述减压硅胶柱色谱分离的梯度洗脱条件为:ch2cl2和meoh的体积比依次为100:1、50:1、10:1和0:1。
[0010]
进一步地,所述聚酰胺树脂分离的梯度洗脱条件为:etoh和h2o的体积比依次为30:70、60:40和90:10。
[0011]
进一步地,所述反相ods柱色谱分离的梯度洗脱条件为:meoh和h2o的体积比依次为30:70、60:40和90:10。
[0012]
本发明还提供一种解热药物,有效成分包括原苏木素b。
[0013]
进一步地,所述解热药物还包括药学上可接受的载体或赋形剂。
[0014]
本发明公开了以下技术效果:
[0015]
本发明首次发现,药材云实中的成分原苏木素b在小鼠发热模型上具有解热作用,能够使发热小鼠的体温降至正常范围。
[0016]
本发明通过将云实的干燥枝用乙醇回流提取,减压浓缩后得总浸膏,通过减压硅胶柱色谱快速将其分成四个粗馏分,然后运用硅胶、聚酰胺树脂和反相ods方法对馏分进行分离纯化,得到化合物原苏木素b,该提取工艺具有操作便捷,提取率高的特点,提取率可以达到0.02%以上。
附图说明
[0017]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0018]
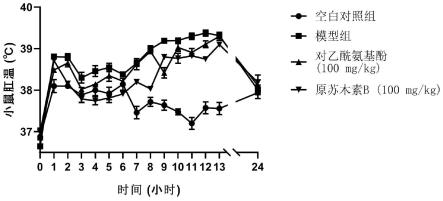
图1为实施例2小鼠实验的肛温检测结果。
具体实施方式
[0019]
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
[0020]
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值,以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
[0021]
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
[0022]
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见得的。本发明说明书和实施例仅是示例性的。
[0023]
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
[0024]
实施例1原苏木素b的制备
[0025]
云实的干燥枝10.0kg用50l 95%(80~100%可达相同效果)的乙醇浸泡12小时,加热至60℃,回流3h,提取3次,60℃(55~65℃可达相同效果)减压浓缩后得总浸膏400g,用2l甲醇溶解总浸膏,与500g硅胶(200-300目)混匀,常温挥干甲醇,得总浸膏硅胶吸附混合物,其用ch2cl2:meoh(体积比100:1,50:1,15:1,0:1)梯度洗脱,每个溶剂比例洗脱体积为8l,通过减压硅胶柱色谱分离,快速将其依次分成四个粗馏分fr.1~fr.4;将fr.1(80g)用etoh:h2o(体积比30:70,60:40,90:10)梯度洗脱,每个洗脱体积为4l,进行聚酰胺树脂分离,依次得到馏分fr.1-1~fr.1-3将fr.1-1(40g)用meoh:h2o(体积比30:70,60:40,90:10)梯度洗脱,通过反相ods柱色谱分离,依次得到馏分fr.1-1-1~fr.1-1-3;fr.1-1-2经核磁
共振谱测试(结果见表1),证明其为原苏木素b(2.5g),纯度为95%。
[0026]
表1化合物的1h(600mhz)和
13
c nmr(150mhz)
[0027][0028][0029]
注:溶剂为cd3od,氢谱测试(600mhz),碳谱测试(150mhz)。
[0030]
按照此方法制备的云实中的原苏木素b的提取率为0.025%。
[0031]
实施例2原苏木素b的解热作用实验
[0032]
1实验材料
[0033]
1.1受试品:实施例1制备的原苏木素b
[0034]
1.2仪器:ft3400型动物体温仪(南京卡尔文生物科技有限公司)
[0035]
1.3试剂:酵母粉末(大连美仑生物技术有限公司),对乙酰氨基酚(大连美仑生物技术有限公司),生理盐水(山东辰欣药业股份有限公司),其余试剂均为国产分析纯。
[0036]
1.4动物:实验动物为spf级c57bl/6j小鼠,雄性50只,6周龄,体重18~20g,购自辽
宁长生生物技术有限公司。
[0037]
2实验方法
[0038]
2.1试液配制方法
[0039]
分别取100mg原苏木素b及阳性药对乙酰氨基酚粉末,用纯水配置成10mg/ml的给药试液;根据小鼠体重及所给药剂量(100mg/kg)计算每次给药所需总药量及体积,空白对照组及模型组给予相同体积的纯水。取酵母粉末5g,与25ml生理盐水混旋,配置成酵母注射液。
[0040]
2.2发热模型的建立
[0041]
小鼠于spf环境下正常饲养5天,使其适应实验室环境,于实验前3天开始每天间隔3小时监测小鼠肛温,记录小鼠基础体温,使其适应测温操作剔除体温异常小鼠。实验开始时0小时测试小鼠基础体温,并将38只实验组小鼠背部皮下注射0.2ml 2.1制备的酵母注射液,使其发热,空白对照组10只小鼠注射相同体积的生理盐水。
[0042]
2.3随机分组及给药
[0043]
取体温升高超过1摄氏度的实验组小鼠30只随机分为3组,即模型组、对乙酰氨基酚组和原苏木素b组,对乙酰氨基酚组分别于造模后1小时、5小时和9小时灌胃给予2.1配制的乙酰氨基酚溶液;原苏木素b组分别于造模后1小时、5小时和9小时灌胃给予2.1配制的原苏木素b溶液;模型组在相同时间给予相同体积的纯水。
[0044]
2.4皮下移植瘤的观察及各指标的测定
[0045]
分别于实验的13小时内每小时测试一次小鼠体温,于造模后24小时测试小鼠肛温。
[0046]
2.5实验结果
[0047]
与空白对照组相比,模型组小鼠肛温明显升高,且发热状态持续13小时;对乙酰氨基酚及原苏木素b给药组均能够明显降低小鼠肛温,与模型组相比,具有统计学差异(图1)。因此,原苏木素b具有制备临床治疗发热药物的前景。
[0048]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。