1.本发明涉及医用生物材料领域,具体涉及一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片及其制备方法。
背景技术:
2.女性因盆底缺陷或盆底支持组织松弛引起的盆底功能障碍(pfd),是多种病因导致的盆底支持薄弱,进而导致盆腔脏器移位,连锁引发其他盆腔器官的解剖位置及其功能异常。针对盆腔脏器脱垂(pop)的手术治疗不断应用于临床。传统手术方式创伤大,术后恢复慢,术后盆腔器官脱垂复发率高。
3.目前,临床治疗盆腔脏器脱垂(pop)应用较多的为全盆底重建术,又称为全盆底悬吊术,以及腹腔镜下子宫/阴道-骶骨固定术,另外还包括经闭孔无张力阴道吊带术,阴道前、后壁补片加固术,经阴道后路悬吊术,骶棘韧带固定术,子宫骶骨悬吊术及骶尾肌筋膜固定术等。全盆底悬吊术采取经阴道植入不可吸收的聚丙烯网片治疗盆腔器官脱垂。
4.此类手术较传统的术式疗效好,具有创伤范围小、手术时间短、恢复快等优点。目前盆腔器官脱垂吊带主要以不可吸收聚酯、聚丙烯等材料为主;此类材料是细菌良好的载体,抗感染能力差,易发生网片侵蚀,植入体内易产生异物感和疼痛感,随着时间不断老化变硬,使患者生活质量下降。目前也有一些生物衍生材料作为pop治疗,比较典型的是由小肠粘膜下层等材料制备,但此类材料制备的产品如不进行交联大多随时间不断降解,无法保证远期临床效果;另外一些生物材料在处理的过程中使用交联剂,目的是提高产品的力学性能,然而交联后的产品在使用过程中会抑制伤口的愈合,短期内材料的细胞毒性增大,刺激局部组织产生长时间的炎症反应,有些交联剂在长期的组织修复中会释放交联剂单体,对局部组织和机体产生慢性毒性。
技术实现要素:
5.本发明提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片及其制备方法。本发明制备的脱细胞异体真皮悬吊补片,可以长久留存在体内无异物感,不易发生感染,又可减轻疼痛发生率,抗张强度适合,是有效治疗盆腔脏器脱垂的悬吊补片,该悬吊补片植入解剖部位后不会引起补片周围组织损伤,阴道黏膜侵蚀等并发症,无免疫排斥反应,不会因补片引起严重感染而发生二次取出,其外形设计可以使医生在手术中精准定位,避免以往补片放不平放不正而使患者手术部位因受力不均牵拉等原因引起疼痛,该产品是生物相容性良好的盆腔脏器脱垂悬吊补片。
6.一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的制备方法,包括:
7.s1、将异体皮原料依次用高渗溶液浸泡、低渗溶液浸泡;
8.s2、将步骤s1处理所得异体皮原料依次用胰蛋白酶酶解、dna水解酶酶解;
9.s3、将步骤s2处理所得异体皮原料再依次用高渗溶液浸泡和低渗溶液浸泡;
10.s4、将步骤s3处理所得异体皮原料用表面活性剂溶液浸泡、氨基酸溶液浸泡、pbs
50khz,功率200-220w。通过超声振荡更有利于使脱水后表皮和细胞脱落。
31.在一些实施例,在步骤s1中,在用低渗溶液浸泡前还包括用低渗溶液对经高渗溶液浸泡的异体皮原料进行清洗的步骤。通过清洗,一方面可以洗去高渗溶液,另一方面可以除去部分已脱落的表皮和细胞;在清洗的同时可以由于渗透压的改变使残留细胞胀破脱落。
32.在一些实施例,在步骤s2中,胰蛋白酶酶解的步骤具体为将步骤s1处理所得异体皮原料用含0.001wt%-0.5wt%胰蛋白酶和0.01wt%-0.2wt%edta的混合溶液浸泡处理。可在室温条件下处理,通常可浸泡处理1-10h。作为优选,在浸泡处理过程还进行振荡处理。例如振荡转速为80-100rpm;更优选每30-120min换液一次。通过振荡处理可以使细胞黏附度下降,从而进一步脱细胞,已达到去除抗原的目的。
33.在一些实施例,在步骤s2中,dna水解酶酶解的步骤具体可为将胰蛋白酶酶解的异体皮原料用含dna水解酶的溶液浸泡处理。该溶液中dna水解酶浓度可为3-7g/l,ph为7.0。dna水解酶酶解可在室温或25-30℃条件下进行,浸泡处理的时间可为3-7h。通过dna水解酶酶解可去除绝大部分dna。
34.在一些实施例中,步骤s3高渗溶液浸泡和低渗溶液浸泡的条件与步骤s1不同。
35.本发明研究发现,将经胰蛋白酶酶解和dna水解酶的异体皮原料再次用高渗溶液浸泡和低渗溶液浸泡处理,可以进一步脱去细胞。还令人惊喜地发现,这样可以更好地固定胶原蛋白,并且使得所制备的产品的力学性能满足盆腔脏器脱垂治疗所需的张力。所制备的全盆底脱垂悬吊补片植入体内后,可与自体组织融合,牢固的固定并支撑盆腔器官,随形性好无异物感,随着组织的长入可以加固其支撑作用,从而彻底缓解脱垂症状提高生活质量。
36.在一些实施例中,作为优选,当所用高渗溶液为甘油溶液时,步骤s3所用高渗溶液的浓度高于或等于步骤s1所用高渗溶液的浓度,更优选高于步骤s1所用高渗溶液的浓度10-50%,或者高于10-30%。
37.在一些实施例中,步骤s3所用高渗溶液的浓度为85%-98%(v/v),例如85%(v/v)、88%(v/v)、90%(v/v)、95%(v/v)、98%(v/v)。
38.在一些实施例中,步骤s1可重复多次,例如1-5次,具体例如1次、2次、3次、4次或5次。
39.在一些实施例中,步骤s1包括先用低浓度甘油溶液(10%-50%)浸泡、低渗溶液(纯化水)浸泡;然后用高浓度甘油溶液(50%-98%)浸泡、低渗溶液(纯化水)浸泡。研究发现这样处理可以使细胞和表皮进一步过度失水和吸水胀破,使接下来酶处理时更好的去细胞去除抗原。
40.在一些实施例,步骤s4中优选将步骤s3处理所得异体皮原料依次用表面活性剂溶液浸泡、氨基酸溶液浸泡、pbs缓冲液浸泡。这样可以洗脱残留的细胞碎片,营养脱细胞异体真皮并洗脱残留试剂使脱细胞异体真皮处于最好的使用状态。
41.在一些实施例,所用表面活性剂溶液为0.2wt%-0.6wt%tritonx-200溶液。优选于室温振荡1-3h,振荡转速为80-100rpm,每10-30min换液一次。
42.在一些实施例,所用氨基酸溶液的浓度为0.2wt%-1wt%。所用氨基酸可选自谷氨酸、甘氨酸、丙氨酸或天门冬氨酸中的至少一种或几种。例如于室温浸泡2-4h。
43.在一些实施例,步骤s5优选将步骤s4处理所得异体皮原料依次用纯化水漂洗、pbs缓冲液(ph7.2-7.4)浸泡处理(例如2-4h)及生理盐水清洗。纯化水漂洗过程优选超声处理,例如纯化水漂洗5次,每次25khz超声处理2min。
44.在一些实施例,还包括将步骤s5处理所得异体皮原料直接包装灭菌的步骤,或进行冷冻干燥后包装、辐射灭菌的步骤。
45.在一些实施例,冷冻干燥的参数:-80℃-50℃预冻2-4h,-50℃-20℃真空冷冻干燥大于8h。
46.在一些实施例,对于将步骤s5处理所得异体皮原料直接包装灭菌的产品(即未经冻干处理),还包括在步骤s1前将待处理的异体皮原料事先裁切的步骤。对于这类产品,事先裁切可以避免产品的二次污染。具体裁切的形状或样式可参见下文。
47.在一些实施例,对于将步骤s5处理所得异体皮原料进行冷冻干燥后包装、辐射灭菌的产品,还包括在冷冻干燥后裁切的步骤;或者还包括在使用前将产品裁切,然后复水的步骤。具体裁切的形状或样式可参见下文。
48.本发明所述用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的制备方法不使用交联剂。
49.本发明中异体皮原料可来源于自愿捐献者(例如非活体)的皮肤。
50.本发明还包括所述方法制备的用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片。
51.本发明由上述的制备方法制备得到的脱细胞真皮没有破坏胶原组织的结构,使结构更加致密。
52.在一些实施例中,所述用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,包括:本体部分;固定部分,设置在所述本体部分的外围;用于固定于或连接患者自身组织;其中,所述本体部分的外周至少设有一个突出部;用于操作者在手术过程中定位和填充。
53.进一步地,所述本体部分上还设有孔,用于液体渗透和细胞长入。
54.可以理解的是,本发明的上述实施例在不冲突的情况下,可以相互结合来获得更多的实施例。在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合。
55.手术:本发明悬吊补片适用于经阴道置入补片手术,经闭孔无张力阴道吊带术,阴道前、后壁补片加固术,经阴道后路悬吊术,骶棘韧带固定术,子宫骶骨悬吊术及骶尾肌筋膜固定术等术式,但需要根据手术情况及医生的需求选择不同形状和样式的悬吊补片。不同样式的补片放置位置不同,其中h型既可以横放又可以竖放入植入部位,其他样式需要竖着植入患处,依据手术方式不同做出不同选择。
56.本发明至少具有以下有益效果之一:
57.本发明提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片及其制备方法,通过对原料皮进行处理,获得医生临床使用效果较好的样式形状,该样式中段四边三角形的设计满足医生手术时精准定位的要求,可以解决因视野局限而无法将补片在解剖部位展平使其术后在体内受力不匀等问题,另外此设计还起到填充缺损组织的目的,使补片更好的与组织融合,修复组织,增强组织张力。在制备处理过程中,使用甘油溶液等高渗溶液和低渗溶液(水或其他)对异体皮肤进行反复的处理,以达到去表皮脱细胞、固定组织结构
的目的,并对产品进行不同试剂配合洗脱,以达到进一步去细胞、去免疫原、灭活细菌、病毒、营养产品的目的,此工艺温和不刺激,可以完整保留胶原结构和基底膜结构,处理后的产品抗张强度适宜,用于盆腔脏器脱垂的治疗在临床上有很好的临床效果。
58.本发明采用生物材料脱细胞异体真皮作为原料制备全盆底悬吊补片,该材料经过物理化学处理后,可完整的脱表皮去细胞,无免疫排斥反应,其力学性能可满足盆腔脏器脱垂治疗所需的张力,所制备的全盆底脱垂悬吊补片植入体内可与自体组织融合,牢固的固定并支撑盆腔器官,随形性好无异物感,随着组织的长入可以加固其支撑作用,从而彻底缓解脱垂症状提高生活治疗。中央部分的脱细胞异体真皮部分使得尿道后壁不会产生来自于吊带的压力,从理论上避免了传统吊带(永久非吸收吊带)由于缺血性压力而导致尿潴留、尿道糜烂及吊带侵蚀等并发症。通过本方法制备的脱细胞异体真皮悬吊补片,在很好的解决盆腔器官脱垂的问题的基础上可以减少并发症、异物感、疼痛感的出现,本发明设计的盆腔器官脱垂脱细胞异体真皮悬吊补片的形状更有利于医生操作及手术过程精准定位,治愈效果更佳。
附图说明
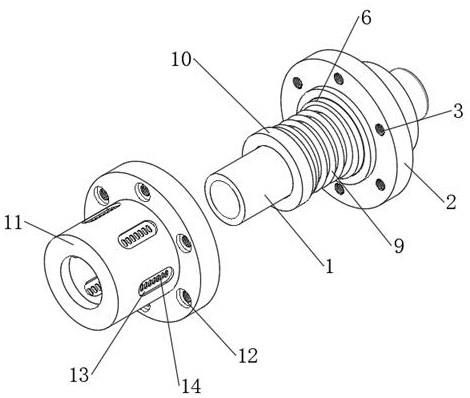
59.图1-图9为本发明实施例用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的结构示意图。
具体实施方式
60.以下实施例用于说明本发明,但不用来限制本发明的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购买得到的常规产品。
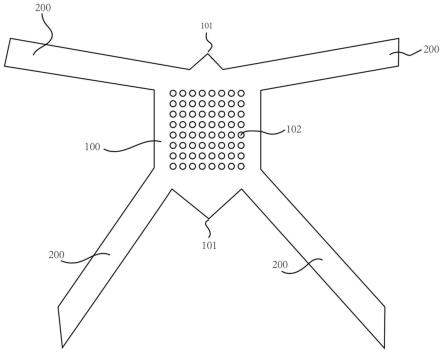
61.如图1、图2、图3、图4、图5、图6、图7、图8、图9所示,本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,包括:本体部分100;固定部分200,设置在所述本体部分100的外围;用于固定于或连接患者自身组织;其中,所述本体部分100的外周至少设有一个突出部101;用于操作者在手术过程中定位和填充。
62.在一些实施例中,所述本体部分100可以是长方形、正方形、梯形、圆形、椭圆形,或其他不规则形状。
63.在一些实施例中,当所述本体部分100是长方形、正方形、梯形或近似长方形、正方形、梯形时,其长边可以为2cm-20cm,宽边可以为2cm-20cm。
64.在一些实施例中,所述本体部分的厚度为0.6-2.0mm。
65.在一些实施例中,所述突出部101为三角形或近似三角形,或其它形状。
66.在一些实施例中,所述突出部101为三角形,其顶角(指远离所述本体部分中心的一侧)大于0
°
小于180
°
,例如大于30
°
小于180
°
,或为60
°‑
150
°
。
67.在一些实施例中,所述固定部分200可为1个、2个、3个、4个或更多。通常可为3-4个。
68.在一些实施例中,所述固定部分200可为条状或带状。其长度可为1-15cm,宽度可为0.5-3cm。
69.在一些实施例中,所述固定部分200厚度可为0.6-2.0mm。
70.在一些实施例中,可在所述本体部分100上缝合或直接剪裁出所述突出部101和/或所述固定部分200。
71.如图1、图3、图4、图6、图7、图9所示,在一些实施例中,所述本体部分100上还设有孔102,用于液体渗透和细胞长入。
72.在一些实施例中,所述孔102的孔径为0.5mm-2mm,孔的行间距和列间距2mm-3.5mm。优选所述孔102置于所述本体部分100的中间位置,孔距两侧边缘距离大于5mm。这样可以便于手术中器械使用或不易撕裂。
73.在一些具体实例中用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的形状及尺寸如图2所示。
74.在一些具体实例中用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的形状及尺寸如图3所示。其中,本体部分100上还设有圆孔102,孔径1.5mm,相邻孔间距2mm。
75.在一些具体实例中用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的形状及尺寸如图5所示。厚度为2mm。
76.在一些具体实例中用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的形状及尺寸如图6所示,厚度为2mm。其中,本体部分100上还设有圆孔102,孔径1.5mm,相邻孔间距2mm。
77.在一些具体实例中用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的形状及尺寸如图8所示。厚度为1.5mm。
78.在一些具体实例中用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片的形状及尺寸如图9所示,厚度为1.5mm。其中,本体部分100上还设有圆孔102,孔径1.5mm,相邻孔间距2mm。
79.上述用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片可采用下文实施例方法制备,可先将原料皮(异体皮)剪裁再进行处理,也可处理后再进行裁切。
80.以下力学性能检测参考标准:gb/t 1040.3-2006《塑料拉伸性能的测定第3部分:薄塑和薄片的试验条件》。
81.实施例1
82.本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
83.(1)将原料皮(异体皮)剪裁(形状及尺寸如图6所示)。将剪裁后的原料皮置于甘油浓度为50%(v/v)的甘油盐水溶液(所用的溶剂为生理盐水)室温浸泡处理10h。将甘油盐水溶液浸泡后的原料皮取出,用纯化水清洗5遍,生理盐水浸泡2h,纯化水清洗5遍。
84.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.05%胰蛋白酶溶液、0.01%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡2h小时,终止酶反应。
85.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为6g/l,ph为7.0的dna水解酶(dnase)中,30℃反应3h,取出后终止酶反应,纯化水清洗5遍。
86.(3)将步骤(2)处理的原料皮置于甘油浓度为85%(v/v)的甘油溶液(所用的溶剂为75%(v/v)乙醇)中,充分反应,于33℃下浸泡处理10h;每浸泡0.5h超声振荡10min后换液,超声条件:50khz,220w。
87.将甘油溶液浸泡后的原料皮取出置于水中漂洗5遍(每次25khz超声处理5min)后,然后置于水中室温浸泡12h。
88.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于0.2%(v/v)tritonx-200溶液中室温摇床振荡浸泡2h,每浸泡30min换液一次,振荡转速80rpm。
89.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出,用纯化水漂洗后,置于质量百分比0.5%谷氨酸和质量百分比0.2%甘氨酸1:1混合的溶液中室温浸泡2h。
90.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡2h。
91.(5)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
92.本实施例产品经检测拉伸强度44n,断裂伸长率23%,在临床使用中即满足盆腔脏器脱垂需要又可以满足患者术后患处对力学的要求,不易复发,临床反馈效果良好,无疼痛。
93.实施例2
94.本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
95.(1)将原料皮(异体皮)剪裁(形状及尺寸如图6所示)。
96.将剪裁后的置于甘油浓度为30%(v/v)的甘油盐水溶液(所用的溶剂为生理盐水)室温浸泡处理7h。将甘油盐水溶液浸泡后的的原料皮取出纯化水清洗5遍,生理盐水浸泡2h,纯化水清洗5遍。
97.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.025%胰蛋白酶溶液、0.02%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,终止酶反应。
98.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为5g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,取出后终止酶反应,纯化水清洗5遍。
99.(3)将步骤(2)处理的原料皮置于甘油浓度为98%(v/v)的甘油溶液(所用的溶剂为75%(v/v)的乙醇),于33℃下浸泡处理10h;每浸泡2h超声振荡10min后换液,超声条件:50khz,220w。
100.将甘油溶液浸泡后的原料皮取出置于纯化水中漂洗5遍后(每次25khz超声处理5min),然后置于纯化水中,室温浸泡12h。
101.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于0.25%(v/v)tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
102.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出,用纯化水漂洗后置于浓度为质量百分比0.5%甘氨酸溶液,室温浸泡2h;
103.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡2h;
104.(5)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
105.本实施例产品经检测拉伸强度56n,断裂伸长率18%,在临床使用中即满足盆腔脏
器脱垂需要,又可以满足患者术后患处对力学的要求,不易复发,临床反馈效果良好,无疼痛。
106.实施例3
107.本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
108.(1)将原料皮(异体皮)剪裁(形状及尺寸如图8所示)。
109.将剪裁后的(异体皮)置于甘油浓度为30%(v/v)的甘油盐水溶液(所用的溶剂为生理盐水),室温浸泡处理5h。将甘油盐水溶液浸泡后的原料皮取出纯化水清洗5遍,生理盐水浸泡4h,纯化水清洗5遍。然后置于50mmtris-hcl和3mmedta混合溶液中,室温震荡浸泡6h,振荡转速为100rpm。纯化水清洗5遍,置于10mmtris缓冲液,室温震荡浸泡6h,振荡转速为100rpm。纯化水清洗5遍。
110.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.025%胰蛋白酶溶液、0.02%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,终止酶反应。
111.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为5g/l、ph为7.0的dna水解酶(dnase)中,30℃反应4h,取出后终止酶反应,纯化水清洗5遍。
112.(3)将步骤(2)处理的原料皮置于甘油浓度为98%(v/v)的甘油溶液(所用的溶剂为75%(v/v)乙醇),于33℃下浸泡处理10h;每浸泡2h超声振荡10min后换液,超声条件:50khz,220w。
113.将甘油溶液浸泡后的原料皮取出置于纯化水中漂洗5遍后(每次25khz超声处理5min)置于纯化水中,室温浸泡12h。
114.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于体积百分比为0.4%tritonx-100室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
115.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于浓度为质量百分比0.5%谷氨酸溶液,室温浸泡2h。
116.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡2h;
117.(5)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
118.本实施例产品经检测拉伸强度48n,断裂伸长率19%,在临床使用中即满足盆腔脏器脱垂需要,又可以满足患者术后患处对力学的要求,不易复发,临床反馈效果良好,无疼痛。
119.实施例4
120.本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
121.(1)将原料皮(异体皮)剪裁(形状及尺寸如图5所示)。
122.将剪裁后的原料皮置于甘油浓度为10%(v/v)的甘油盐水溶液(所用的溶剂为生理盐水),室温浸泡处理10h。将甘油盐水溶液浸泡后的的原料皮取出纯化水清洗5遍,生理盐水浸泡2h,纯化水5遍,置于50mmtris缓冲液、1.5mmkcl、1.5mmnacl混合溶液中,室温震荡
浸泡10h,振荡转速为100rpm。纯化水清洗5遍,10mmtris缓冲液清洗1遍,置于10mmtris缓冲液,室温震荡浸泡8h,振荡转速为100rpm。纯化水清洗5遍。
123.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.025%胰蛋白酶溶液、0.02%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,终止酶反应。
124.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后于浓度为5g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,取出后终止酶反应,纯化水清洗5遍。
125.(3)将步骤(2)处理的原料皮置于甘油浓度为体积百分比98%的甘油溶液(所用的溶剂为75%(v/v)乙醇)中,于33℃下浸泡处理10h;每浸泡2h超声振荡10min后换液,超声条件:50khz,220w。
126.将甘油溶液浸泡后的原料皮取出置于纯化水中漂洗5遍后(每次25khz超声处理5min)置于纯化水中,室温浸泡12h。
127.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于体积百分比为0.5%tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
128.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于质量百分比0.5%谷氨酸和质量百分比0.2%甘氨酸1;1混合的溶液中室温浸泡2h。
129.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡2h。
130.(5)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
131.本实施例产品经检测拉伸强度44n,断裂伸长率20%,在临床使用中即满足盆腔脏器脱垂需要,又可以满足患者术后患处对力学的要求,不易复发,临床反馈效果良好,无疼痛。
132.实施例5
133.本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
134.(1)将原料皮(异体皮)剪裁(形状及尺寸如图6所示)。
135.将剪裁后的原料皮置于甘油浓度为30%(v/v)的甘油盐水溶液(所用的溶剂为生理盐水),室温浸泡处理5h;将甘油盐水溶液浸泡后的原料皮取出纯化水清洗5遍,生理盐水浸泡4h,纯化水5遍。然后置于50mmtris-hcl和3mnacl混合溶液中,室温震荡浸泡6h,振荡转速为100rpm。纯化水清洗5遍,置于10mmtris缓冲液,室温震荡浸泡6h,振荡转速为100rpm。纯化水清洗5遍。
136.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.02%胰蛋白酶溶液、0.01%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,取出后终止酶反应,纯化水清洗5遍。
137.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为3g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,终止酶反应。
138.(3)将步骤(2)处理的原料皮置于甘油浓度为体积百分比85%的甘油溶液(所用的溶剂为75%(v/v)乙醇)中,于33℃下浸泡处理10h;每浸泡2h超声振荡10min后换液,超声条
件:50khz,220w。
139.将甘油溶液浸泡后的原料皮取出置于纯化水中漂洗5遍后(每次25khz超声处理5min)置于纯化水中,室温浸泡12h,每2h换液一次。
140.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于体积百分比为0.3%tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
141.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于浓度为质量百分比0.5%谷氨酸和0.5%甘氨酸1:1混合溶液,室温浸泡2h。
142.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡4h。
143.(5)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
144.本实施例产品经检测拉伸强度54n,断裂伸长率12%,在临床使用中即满足盆腔脏器脱垂需要,又可以满足患者术后患处对力学的要求,不易复发,临床反馈效果良好,无疼痛。
145.实施例6
146.本实施例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
147.(1)将原料皮(异体皮)置于甘油浓度为10%(v/v)的甘油溶液(所用的溶剂为生理盐水溶液)室温浸泡处理6h。
148.将甘油溶液浸泡后的步骤(1)中的原料皮取出置于纯化水中漂洗5遍(每次25khz超声处理5min)后置于纯化水中,室温浸泡7h。
149.将原料皮取出,置于甘油浓度为50%(v/v)的甘油溶液(所用的溶剂为生理盐水溶液),室温浸泡处理6h。然后纯化水清洗5遍。
150.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.25%胰蛋白酶溶液、0.05%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,取出后终止酶反应,纯化水清洗5遍。
151.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为5g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,终止酶反应。
152.(3)将步骤(2)处理的原料皮置于甘油浓度为85%(v/v)的甘油溶液(所用的溶剂为75%(v/v)乙醇)中,于33℃下浸泡处理10h;每浸泡2h超声振荡10min后换液,超声条件:50khz,220w。
153.将甘油溶液浸泡后的原料皮取出置于纯化水中漂洗5遍(每次25khz超声处理5min)后置于纯化水中,室温浸泡7h。
154.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于表面活性剂溶液中浸泡处理,在本实施例中选择体积百分比为0.4%tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm;
155.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于浓度为质量百分比0.8%谷氨酸溶液,室温浸泡2h。
156.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每
次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡2h。
157.(5)低温冷冻干燥:将原料皮剪裁(形状及尺寸如图5所示)。
158.包装和灭菌:将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
159.本实施例产品经检测拉伸强度46n,断裂伸长率14%,在临床使用中即满足盆腔脏器脱垂需要,又可以满足患者术后患处对力学的要求,不易复发,临床反馈效果良好,无疼痛。
160.对比例1
161.本对比例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
162.(1)将原料皮(异体皮)剪裁成与实施例5相同的形状及尺寸。
163.(2)胰蛋白酶酶解处理:将剪裁后的原料皮置于0.02%胰蛋白酶溶液、0.01%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,取出后终止酶反应,纯化水清洗5遍。
164.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为3g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,终止酶反应。
165.(3)表面活性剂溶液浸泡处理:将步骤(2)中处理的原料皮取出置于体积百分比为0.3%tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
166.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于浓度为质量百分比0.5%谷氨酸和0.5%甘氨酸1:1混合溶液,室温浸泡2h。
167.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡4h。
168.(4)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
169.本对比例产品经检测拉伸强度57n,断裂伸长率15%,虽然力学要求可以满足临床使用中对盆腔脏器脱垂需要,但此种处理方法不能彻底脱细胞和表皮,免疫原性要求无法满足,会产生免疫排斥反应,因此不可应用于人体。
170.对比例2
171.本对比例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
172.(1)将原料皮(异体皮)剪裁成与实施例5相同的形状及尺寸。
173.将剪裁后的原料皮置于甘油浓度为体积百分比30%的甘油盐水溶液(所用的溶剂为生理盐水),室温浸泡处理5h;将甘油盐水溶液浸泡后的原料皮取出纯化水清洗5遍,生理盐水浸泡4h,纯化水5遍。然后置于50mmtris-hcl和3mnacl混合溶液中,室温震荡浸泡6h,振荡转速为100rpm。纯化水清洗5遍,置于10mmtris缓冲液,室温震荡浸泡6h,振荡转速为100rpm。纯化水清洗5遍。
174.(2)胰蛋白酶酶解处理:将步骤(1)处理的原料皮置于0.02%胰蛋白酶溶液、0.01%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,取出后终止酶反应,纯化水清洗5遍。
175.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度
为3g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,终止酶反应。
176.(3)表面活性剂溶液浸泡处理:将步骤(2)中处理的原料皮取出置于体积百分比为0.3%tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
177.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于浓度为质量百分比0.5%谷氨酸和0.5%甘氨酸1:1混合溶液,室温浸泡2h。
178.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡4h。
179.(4)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
180.本对比例产品经检测拉伸强度47n,断裂伸长率30%,在临床使用中可以满足盆腔脏器脱垂需要,但是在患者长期术后恢复中,无法满足患处对力学的要求,易复发,且dna残留较高。
181.对比例3
182.本对比例提供一种用于盆腔脏器脱垂治疗的脱细胞异体真皮悬吊补片,制备方法如下:
183.(1)将原料皮(异体皮)剪裁成与实施例5相同的形状及尺寸。
184.(2)胰蛋白酶酶解处理:
185.将剪裁后的原料皮置于0.02%胰蛋白酶溶液、0.01%edta混合液中浸泡振荡,用pbs缓冲溶液调ph值至7.4,振荡转速为100rpm,浸泡3小时,取出后终止酶反应,纯化水清洗5遍。
186.dna水解酶处理:将胰蛋白酶酶解处理的原料皮取出用纯化水漂洗5遍后,于浓度为3g/l,ph为7.0的dna水解酶(dnase)中,30℃反应4h,终止酶反应。
187.(3)将步骤(2)处理的原料皮置于甘油浓度为体积百分比85%的甘油溶液(所用的溶剂为乙醇为体积百分比0.5%的水溶液),于33℃下浸泡处理10h;每浸泡2h超声振荡10min后换液,超声条件:50khz,220w。
188.将甘油溶液浸泡后的原料皮取出置于纯化水中漂洗5遍后(每次25khz超声处理5min)置于纯化水中,室温浸泡12h,每2h换液一次。
189.(4)表面活性剂溶液浸泡处理:将步骤(3)中处理的原料皮取出置于体积百分比为0.3%tritonx-200室温摇床振荡浸泡1h,每浸泡30min换液一次,振荡转速80rpm。
190.氨基酸溶液浸泡处理:将表面活性剂溶液浸泡处理的原料皮取出用纯化水漂洗后置于浓度为质量百分比0.5%谷氨酸和0.5%甘氨酸1:1混合溶液,室温浸泡2h。
191.pbs缓冲液浸泡处理:将氨基酸溶液浸泡处理的原料皮取出用纯化水漂洗5次(每次25khz超声处理2min)后置于pbs缓冲液(ph7.2-7.4)中室温浸泡4h。
192.(4)包装和灭菌:pbs缓冲液浸泡处理后,用生理盐水漂洗两遍并装袋封口保存,然后将包装好的产品经钴-60灭菌,灭菌辐射剂量25-40kgy。
193.本对比例产品经检测拉伸强度46n,断裂伸长率22%,在临床使用中满足盆腔脏器脱垂需要,也满足患者术后患处对力学的要求,但dna残留较高,易发生免疫排斥反应。
194.实验例1
195.按照yy/t 0606.25-2014《动物源性生物材料dna残留量测定法:荧光染色法》中规
定的检测方法检测dna残留。检测结果见下表1。
196.表1dna残留(ng/mg)
[0197][0198]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。