放射疗法系统中的电子快门
1.相关申请的交叉引用
2.本技术要求于2018年7月28日提交的美国临时申请号62/711,483的权益。
背景技术:
3.除非本文另外指出,否则本节中描述的方法不是本技术中的权利要求的现有技术,并且不由于包含在本节中而被承认是现有技术。
4.放射疗法是针对特定靶标组织(计划靶标体积)(诸如,癌性肿瘤)的局部治疗。理想地,放射疗法对计划靶标体积执行,以使得周围的正常组织免于接受超过指定公差的剂量,从而将对健康组织造成损害的风险最小化。在进行放射疗法之前,成像系统通常被用来提供靶标组织和周围区域的三维图像。根据这样的成像,可以估计靶标组织的尺寸和质量,并且生成适当的治疗计划,并确定计划的靶标体积。
5.为了在放射疗法期间将规定剂量正确地供应到计划靶标体积(即,靶标组织),患者应相对于提供放射疗法的线性加速器正确定位。通常,在治疗之前和治疗期间检查剂量和几何数据,以确保正确放置患者并确保所实施的放射疗法治疗与先前计划的治疗匹配。该过程被称为图像引导放射疗法(igrt),并且涉及在放射治疗被递送至计划靶标体积的同时,使用成像系统来查看靶标组织。igrt并入了来自治疗计划的成像坐标,以确保患者在放射疗法设备中被正确对准,以进行治疗。
技术实现要素:
6.根据本公开的至少一些实施例,放射疗法系统被配置为在治疗期间,生成针对靶标体积的体积图像数据,其中体积图像数据不会由于x射线图像噪声而退化,x射线图像噪声由治疗x射线的散射引起。结果,如此生成的体积图像数据可以被用来更准确地检测在施加治疗x射线期间发生的分次内运动。例如,利用靶标体积的这种更高质量的体积图像数据,由于屏气丧失和/或由于蠕动引起的解剖学变化而引起的靶标体积的分次内运动可以被更容易地检测。因此,放射疗法系统可以执行图像引导放射疗法(igrt),图像引导放射疗法使用x射线成像而不是磁共振成像(mri)来监视分次内运动。所检测的解剖学变化然后可以经由患者重新定位和/或治疗修改来补偿,或者当前的治疗可以被中止。
7.在一些实施例中,在igrt过程期间,治疗x射线和成像x射线的时域交织防止了治疗x射线的散射降低被用于生成靶标体积的体积图像数据的x射线图像的质量。在这样的实施例中,在一个或多个成像间隔期间,成像x射线被递送至靶标体积,并且在成像间隔之间,治疗x射线的一个或多个脉冲被递送至靶标体积。在治疗x射线的脉冲被定时为在成像间隔期间发生的情况下,治疗x射线的脉冲被抑制在成像间隔期间发生,并且被重新安排为在与成像间隔或后续成像间隔不重合的稍后时间发生。
8.在一些实施例中,治疗x射线被递送到靶标体积,同时成像x射线也被递送到靶标体积来生成靶标体积的体积图像数据。即,在成像x射线被递送到靶标体积的成像间隔期间,治疗x射线的一个或多个脉冲也被递送到靶标体积。在这样的实施例中,在x射线成像设
备的每个像素中,图像信号在成像间隔的各部分中累积,在成像间隔中,成像x射线被递送到靶标体积;并且在治疗x射线的脉冲期间,图像信号被防止在每个像素中累积。
9.前述发明内容仅是例示性的,而无意于以任何方式进行限制。除了上述例示性方面、实施例和特征之外,通过参考附图和以下详细描述,其他方面、实施例和特征将变得显而易见。
附图说明
10.通过结合附图进行的以下描述和所附权利要求,本公开的前述和其他特征将变得更加显而易见。这些附图仅描绘了根据本公开的若干实施例,并且因此不应被视为对其范围的限制。通过使用附图,将以附加的特异性和细节来描述本公开。
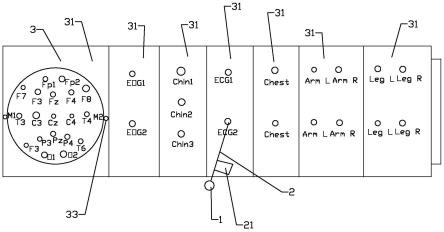
11.图1是可以有益地实现本公开的各个方面的放射疗法系统的透视图。
12.图2示意性地图示了根据本公开的各种实施例的图1的放射系统的驱动台和机架。
13.图3示意性地图示了根据本公开的一个实施例的x射线成像仪的截面图。
14.图4示意性地图示了根据本公开的各种实施例的图1的放射系统的驱动台和机架。
15.图5示意性地图示了根据本公开的各种实施例的基于由图1的放射疗法系统中包括的一个或多个x射线成像仪生成的投影图像而构造的数字体积。
16.图6a是根据本公开的一个实施例的像素检测器元件的电路图。
17.图6b是根据本公开的另一实施例的像素检测器元件的电路图。
18.图7a是图示了根据本公开的一个实施例的在治疗间隔期间施加治疗束脉冲以及在成像间隔期间施加成像束脉冲的示意性时序图。
19.图7b是图示了根据本公开的另一实施例的在治疗间隔期间施加治疗束脉冲以及在成像间隔期间施加成像束脉冲的示意性时序图。
20.图8阐述了根据本公开的一个或多个实施例的放射疗法过程的流程图。
21.图9是图示了根据本公开的一个实施例的成像束脉冲在成像间隔期间的定时的示意性时序图,成像间隔的持续时间比两个治疗束脉冲之间的时间间隔更短。
22.图10是根据本公开的一个实施例的包括电子快门的像素检测器元件的电路图。
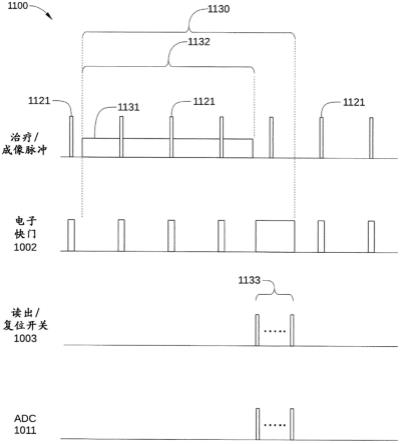
23.图11是图示了根据本公开的一个实施例的在成像间隔期间施加治疗束脉冲和成像束脉冲的示意性时序图。
24.图12阐述了根据本公开的一个或多个实施例的放射疗法过程的流程图。
具体实施方式
25.在以下详细描述中,参考了构成其一部分的附图。在附图中,除非上下文另外指出,否则相同的符号通常标识相同的组件。在详细描述、附图和权利要求中描述的例示性实施例并不意味着是限制性的。在不脱离此处呈现的主题的精神或范围的情况下,可以利用其他实施例并且可以进行其他改变。容易理解,如本文中整体描述的以及在附图中图示的本公开的各方面可以以各种不同配置来布置、替换、组合和设计,所有这些都被明确地构想并构成本公开的一部分。
26.简介
27.图像引导放射疗法(igrt)被用于治疗在经受自主移动的身体区域(诸如,肺部)或
者经受非自主移动的身体区域(诸如,由蠕动影响的器官)中的肿瘤。igrt涉及使用成像系统来查看靶标组织(也被称为“靶标体积”),同时对其进行放射治疗。在igrt中,来自先前确定的治疗计划的靶标体积的基于图像的坐标与在施加治疗束期间确定的靶标体积的基于图像的坐标进行比较。以此方式,处于风险中的周围器官的变化和/或靶标体积相对于放射疗法系统的运动或变形可以被检测。因此,基于日常的位置和形状,对处于风险中的器官的剂量极限可以被精确地实施,并且患者的位置和/或治疗束可以被调整,以将放射剂量更精确地靶向肿瘤。例如,在胰腺肿瘤治疗中,处于风险的器官包括十二指肠和胃。这些处于风险的器官相对于靶标体积的形状和相对位置每天都可能显著变化。因此,准确地适应处于风险中的这种器官的形状和相对位置使得能够将剂量逐步增加至靶标体积并获得更好的治疗效果。
28.在一些常规的igrt放射系统中,在经由诸如金种子的基准标记物施加治疗束期间,检测到软组织的运动。然而,基准标记物的使用、特别是放置标记物所需的侵入性外科手术具有许多缺点。具体而言,腹腔镜下插入基准标记物需要附加的时间和临床资源,诸如,手术室、麻醉、抗生素以及众多其他医学专家的参与。
29.备选地,在一些常规igrt放射系统中,软组织的运动在施加治疗束期间,经由磁共振成像(mr1)来检测。但是,基于mri的igrt也有缺点。首先,基于mri的igrt系统通常比采用x射线成像的放射疗法系统更大、更复杂且更昂贵。其次,经由mri来检测靶标体积的运动或变形通常涉及监视与穿过靶标体积的2d切片相关联的图像。结果,在被监视的2d切片之外(或垂直)的任何地方发生的靶标体积运动或变形难以被检测,这可能严重影响所施加的放射剂量的准确性。
30.备选地,在一些常规igrt放射系统中,软组织的运动在施加治疗x射线期间,经由也直接穿过靶标体积的成像x射线来检测。例如,针对靶标体积的体积图像数据可以基于靶标体积的x射线投影图像来重建,x射线投影图像使用计算机断层扫描(ct)或锥束ct(cbct)过程来生成。在ct或cbct过程中,多个x射线投影图像通过穿过靶标体积并到达x成像设备的成像x射线来生成。因为存在x射线被施加到靶标体积,同时成像x射线被x射线成像设备接收的时间间隔,在这样的时间间隔期间生成的x射线投影图像可能包括由散射的治疗x射线引起的显著图像噪声,散射的治疗x射线被x射线成像设备捕获。例如,当典型的兆伏(mv)治疗x射线和千伏(kv)成像x射线被采用时,来自患者、治疗台和机器组件的散射mv放射的幅度可能会超过所有其他图像噪声。因为这样的图像噪声的泊松分布分量不能被滤除,所以x射线投影图像的图像质量被降低。因此,基于这样的x射线图像而对分次内运动的检测造成负面影响。
31.鉴于上述情况,本领域中需要改进的系统和技术,以确保在治疗束被递送至靶标体积的同时,靶标体积保持适当定位,以在放射疗法系统中进行治疗。根据本文所述的各种实施例,放射系统被配置为生成靶标体积的高质量x射线图像,高质量x射线图像不会由于来自散射治疗x射线的图像噪声而退化。在图1中图示了一个这样的实施例。
32.系统概述
33.图1是可以有益地实现本公开的各个方面的放射疗法系统100的透视图。放射疗法(rt)系统100是被配置为使用x射线成像技术来近实时地检测分次内运动的放射系统。因此,rt系统100被配置为针对体内指示放射治疗的任何地方的病变、肿瘤和状况来提供立体
定向放射外科手术和精确放射疗法。这样,rt系统100可以包括生成高能x射线的兆伏(mv)治疗束的一个或多个线性加速器(linac)、千伏(kv)x射线源、x射线成像仪并且在某些实施例中,还包括mv电子门禁成像设备(epid)。例如,本文描述了配置有圆形机架的放射疗法系统100。在其他实施例中,放射疗法系统100可以被配置有能够经由滑环连接而无限旋转的c型机架。
34.通常,rt系统100能够在施加mv治疗束期间,对靶标体积进行kv成像,使得igrt过程可以使用x射线成像而不是mri来执行。rt系统100可以包括所有都设置在治疗室内的一个或多个触摸屏101、卧榻运动控制装置102、孔103、基座定位组件105、设置在基座定位组件105上的卧榻107以及图像采集和治疗控制计算机106。rt系统100还包括远程控制控制台110,远程控制控制台110被设置在治疗室外部并且能够从远程位置进行治疗递送和患者监视。基座定位组件105被配置为将卧榻107相对于孔103精确地定位,并且运动控制装置102包括诸如按钮和/或开关的输入设备,输入设备使得用户能够操作基座定位组件105来将卧榻107相对于孔103自动且精确地定位到预定位置。运动控制装置102还使得用户能够将卧榻107手动定位到预定位置。在一些实施例中,rt系统100还包括在治疗室中用于患者监视的一个或多个相机(未示出)。
35.图2示意性地图示了根据本公开的各种实施例的rt系统100的驱动台200和机架210。为了清楚起见,图2中省略了盖、基座定位组件105、卧榻107以及rt系统100的其他组件。驱动台200是针对rt治疗系统110的组件的固定支撑结构,包括机架210以及用于可旋转地移动机架210的驱动系统201。驱动台200搁置和/或被固定在rt治疗系统110外部的支撑表面,诸如,rt治疗设施的地板。机架210被旋转地耦合到驱动台200,并且是rt系统100的各种组件所安装的支撑结构,各种组件包括线性加速器(linac)204、mv电子门禁成像设备(epid)205、成像x射线源206和x射线成像仪207。在rt治疗系统110的操作期间,机架210在由驱动系统201致动时,围绕孔103旋转。
36.驱动系统201旋转地致动机架210。在一些实施例中,驱动系统201包括可以被固定到驱动台200的线性电机,并与安装在机架210上的磁轨道(未示出)交互。在其他实施例中,驱动系统201包括用于使得机架210围绕孔201精确地旋转的另一合适的驱动机构。linac 204生成高能x射线(或在一些实施例中为电子)的mv治疗束230,并且epid 205被配置为利用治疗束230来获取x射线图像。成像x射线源206被配置为将锥形的x射线束(在本文中被称为成像x射线231)引导通过rt系统100的等中心203,到达x射线成像仪207,并且等中心203通常对应于待治疗的靶标体积209的位置。在图2所示的实施例中,x射线成像仪207被描绘为平面设备,而在其他实施例中,x射线成像仪207可以具有弯曲配置。
37.x射线成像仪207接收成像x射线231,并且从中生成合适的投影图像。根据某些实施例,这样的投影图像然后可以被用来针对数字体积来构造或更新成像数据的各部分,数字体积对应于包括靶标体积209的三维(3d)区域。即,这样的3d区域的3d图像根据投影图像来重建。在实施例中,锥形束计算机断层扫描(cbct)和/或数字断层合成(dts)可以被用来处理由x射线成像仪207生成的投影图像。cbct通常被用于在相对长的采集弧上采集投影图像,例如,在机架210旋转180
°
或更大角度时采集投影图像。结果,成像体积的高质量3d重建可以被生成。cbct通常在放射疗法会话开始时被采用以生成所设置的3d重建。例如,cbct可以在施加治疗束230之前立即被采用以生成3d重建,从而确认了靶标体积209没有移动或改
变形状。
38.相反,在igrt过程的各部分期间,部分数据重建由rt系统100来执行,其中,部分图像数据被用于生成靶标体积209的3d重建。例如,当机架210旋转经过治疗弧的同时,治疗束230被引导到等中心203时,dts图像采集可以被执行来生成靶标体积209的图像数据。因为dts图像采集在相对较短的采集弧上执行,例如,在大约10
°
至60
°
之间执行,靶标体积209的形状和位置的近实时反馈可以在igrt过程期间通过dts成像来提供。
39.在一些实施例中,x射线成像仪207包括其上形成有像素检测器元件的矩阵或阵列的玻璃板,像素检测器元件各自将入射的x射线光子转换为电荷。在x射线成像仪207被配置为间接平板检测器的实施例中,x射线成像仪207中的闪烁体材料被入射的x射线激发并发射光,光被多个光电二极管检测。每个光电二极管针对最终将变成数字图像的不同像素生成信号(例如,与入射光强度成比例的电荷)。x射线成像仪207中包括的编码器然后解释这些信号中的每一个,并且为每个信号分配与该信号成比例的值。x射线成像仪207的一个这样的实施例在图3中图示。
40.图3示意性地图示了根据本公开的一个实施例的x射线成像仪207的截面图。如图所示,x射线成像仪207包括在衬底302上形成的光敏元件和检测器电路装置层301。附加地,x射线成像仪207包括在光敏元件和检测器电路装置层301上形成的闪烁体材料303的层。还示出了入射x射线309,入射x射线309在由成像x射线源206(图2所示)生成之后,穿过患者、样本或其他感兴趣对象。光敏元件和检测器电路装置层301、衬底302以及闪烁体材料303一起形成x射线成像阵列305。注意,光敏元件和检测器电路装置层301通常由多个处理层形成,并且x射线成像阵列305可以包括在图3中未图示的附加材料层。
41.光敏元件和检测器电路装置层301通常包括多个像素检测器元件310。每个像素检测器元件310包括光敏元件,诸如,光电二极管、光电门或光电晶体管以及适合于作为x射线成像仪207中的像素检测器元件来操作的任何其他电路。例如,光敏元件和检测器电路装置层301还可以包括薄膜晶体管(tft),其用于从像素检测器元件中读出数字信号。闪烁体材料303可以包括一个或多个材料层,包括但不限于硫氧化钆(gd2o2s:tb)、钨酸镉(cdwo4)、锗酸铋(bi4ge3o12或bgo)、碘化铯(csi)或铯碘化铊(csi:tl)等。
42.在一些实施例中,在检测器电路装置层301中包括的tft包括使得能够将更多的晶体管并入像素检测器元件310中的一个或多个特定半导体材料,诸如,铟镓锌氧化物(igzo)、低温多晶硅半导体材料以及多晶硅材料。备选地,在一些实施例中,检测器电路装置层301中包括的晶体管可以基于使得更复杂的电路能够被包括在单个像素检测器元件310中的互补金属氧化物半导体(cmos)技术。由于cmos中的电荷载流子迁移率非常高时,晶体管可以做得非常小,并且因此与其他技术相比,切换引起的电荷注入可以被显著减少。
43.在图3所示的实施例中,x射线成像仪207被描绘为间接平板检测器,其中,x射线光子被转换为其他光子,其他光子进而被检测并转换为电荷。在其他实施例中,x射线成像仪207可以是直接平板检测器(fpd)。在直接fpd中,入射x射线光子在非晶态硒层中被直接转换为电荷,并且其中所产生的电荷图案通过合适的硬件(诸如,薄膜晶体管(tft)阵列、有源矩阵阵列、微等离子线寻址等)来读出。
44.在图2所示的实施例中,rt系统100包括单个x射线成像仪和单个对应的成像x射线源。在其他实施例中,rt系统100可以包括两个或更多个x射线成像仪,x射线成像仪各自具
有对应的成像x射线源。在图4中图示了一个这样的实施例。
45.图4示意性地示出了根据本公开的各种实施例的rt系统100的驱动台400和机架410。驱动台400和机架410在配置上与图2中的驱动台200和机架200基本相似,不同之处在于,在机架410上安装的rt系统100的组件包括第一成像x射线源406、第一x射线成像仪407、第二成像x射线源408和第二x射线成像仪409。在这样的实施例中,在rt系统100中包括多个x射线成像仪有助于在较短的图像采集弧上生成(用于重建靶标体积的)投影图像。例如,当rt系统100包括两个x射线成像仪和对应的x射线源时,用于采集某个图像质量的投影图像的图像采集弧可以是用于使用单个x射线成像仪和x射线源来采集相似图像质量的投影图像的图像采集弧的大约一半。
46.由x射线成像仪207(或由第一x射线成像仪407和第二x射线成像仪409)生成的投影图像被用于针对3d区域内包括靶标体积的患者解剖结构的数字体积构造成像数据。备选地或附加地,这样的投影图像可以被用于更新与3d区域相对应的数字体积的现有成像数据的各部分。以下结合图5来描述这样的数字体积的一个实施例。
47.图5示意性地图示了根据本公开的各种实施例的数字体积500,数字体积500基于由rt系统100中包括的一个或多个x射线成像仪生成的投影图像来构造。例如,在一些实施例中,投影图像可以由单个x射线成像仪(诸如,x射线成像仪207)来生成,并且在其他实施例中,投影图像可以由多个x射线成像仪(诸如,第一x射线成像仪407和第二x射线成像仪409)来生成。
48.数字体积500包括解剖学图像数据的多个体素501(虚线),其中每个体素501对应于数字体积500内的不同位置。为了清楚起见,图5中仅示出了单个体素501。数字体积500对应于包括靶标体积510的3d区域。在图5中,数字体积500被描绘为8
×8×
8体素立方体,但是实际上,数字体积500通常包括更多的体素,例如比图5所示的数量级大的数量级。
49.为了讨论的目的,靶标体积510可以指代针对特定治疗的总肿瘤体积(gtv)、临床靶标体积(ctv)或计划靶标体积(ptv)。gtv描绘了可以被看到或成像的总肿瘤的位置和范围;ctv包括gtv以及通常无法成像的亚临床疾病传播的附加余量;并且ptv是被设计为在不会对附近处于风险中的器官造成不利影响的情况下,确保适当的放射疗法剂量被实际递送到ctv的几何概念。因此,ptv通常大于ctv,但在某些情况下也可以在某些部分中被减小,以在处于风险的器官周围提供安全余量。ptv通常基于在治疗时间之前执行的成像来确定,并且本公开的实施例促进了ptv与患者解剖结构在治疗时的当前位置的对准。
50.根据以下描述的各个实施例,与数字体积500的每个体素501相关联的图像信息由单个或多个x射线成像仪例如经由cbct过程生成的投影图像来构造。在一些实施例中,与数字体积500的体素501中的一些或全部相关联的图像信息由单个或多个x射线成像仪经由dts过程生成的投影图像来更新。例如,这样的dts过程可以在所计划的治疗的一部分开始之后并且在所计划的治疗完成之前采用。以这种方式,靶标体积510的位置和形状可以在进行治疗的同时确认。因此,如果靶标体积510的足够部分被检测为延伸到阈值区域之外,则治疗可以被中止或修改。在这种情况下,治疗的修改可以通过调整患者位置和/或治疗束来实现。
51.成像和治疗x射线的时域交织
52.在使用期间,治疗束通常会在所有方向上生成大量散射放射,包括从患者、治疗台
和机器组件发出的散射放射。结果,大量的mv散射可能入射在x射线成像仪(例如,图2中的x射线成像仪207或图4中的第一x射线成像仪407和第二x射线成像仪409)上。在某些情况下,这样的x射线散射量甚至可能超过成像x射线的幅度。因此,在一些实施例中,治疗束与成像x射线的时域交织可以被用来减少或消除治疗束的x射线散射对检测成像x射线的干扰。即,在这样的实施例中,成像x射线(例如,图2中的成像x射线231)向靶标体积510和治疗束(例如,图2中的治疗束230)的递送定时被优化。在这样的实施例中,成像x射线和治疗束被脉冲化或以其他方式被间歇地激活,使得当成像x射线被x射线成像仪接收时,治疗束不被递送到靶标体积510。
53.图6a是根据本公开的一个实施例的像素检测器元件310的电路图600。由电路图600图示的像素检测器元件310的实施例被包括在x射线成像仪中,x射线成像仪使得治疗束与成像x射线能够时域交织。像素检测器元件310可以被包括在rt系统100的x射线成像仪中,诸如被包括在图2中的x射线成像仪207或图4中的第一x射线成像仪407或第二x射线成像仪409中。像素检测器元件310包括光电二极管601、复位开关602、读出开关603以及在一些实施例中的电压跟随器604。如图所示,光电二极管601经由复位开关602而被通信地耦合到参考电压v
ref
,并且经由读出开关603和电压跟随器604而被通信地耦合到数据线610。备选地,在一些实施例中,参考电压v
ref
和偏置电压606(例如,接地)的位置被反转。在这样的实施例中,当复位开关602闭合时,光电二极管601的一侧被连接到偏置电压606。
54.在操作中,当由图3中的闪烁体材料303生成的光子入射在光电二极管601上时,光电二极管601产生电荷。当读出开关603闭合时,由光电二极管601累积的电荷被读出到数据线610,并且通过模数转换器(adc)611而被转换为数字信号,模数转换器(adc)611在像素检测器元件310外部并且被耦合到数据线610。在像素检测器元件310包括电压跟随器604的实施例中,当复位开关602闭合时,由光电二极管601累积的电荷被复位。
55.图6b是根据本公开的另一实施例的像素检测器元件310的电路图620。图6b中所示的像素检测器元件310的实施例与图6a中所示的像素检测器元件310的实施例基本类似,但以下情况除外。首先,像素检测器元件310不包括电压跟随器604。第二,光电二极管601不经由复位开关602直接耦合至参考电压v
ref
。相反,光电二极管601经由复位开关622和如图所示的数据线610而被耦合至参考电压v
ref
。备选地,在一些实施例中,复位开关622被集成到adc 611中。在任一情况下,在这样的实施例中,每当复位开关602闭合时,读出开关603闭合,使得在该时间期间光电二极管中的信号累积被避免。
56.根据图6a和图6b所示的实施例,施加治疗束脉冲被限制到治疗间隔,而施加成像束脉冲被限制到成像间隔,使得由治疗束脉冲生成的噪声被防止由光电二极管601捕获。在图7a和图7b中图示了这样的实施例。
57.图7a是图示了根据本公开的一个实施例的在治疗间隔720期间施加治疗束脉冲721以及在成像间隔730期间施加成像束脉冲731的示意性时序图700。具体而言,图7a适用于图6a所示的像素检测器元件310的实施例。图7a中还描绘了治疗束脉冲721和成像束脉冲731相对于复位开关602、读出开关603的断开和闭合以及adc 611的激活的定时。
58.在治疗间隔720期间,一个或多个治疗束脉冲721被引导至靶标体积。在图7a所示的实施例中,治疗间隔720被示出为具有三个治疗束脉冲721,但是实际上,治疗间隔720可以包括多达一百个或更多个治疗束脉冲。在一些实施例中,典型的治疗束脉冲721(例如,图
2中的治疗束230的脉冲)的持续时间大约为5微秒(μs),并且大约每1至10毫秒(ms)被递送。在这样的实施例中,治疗束脉冲721的持续时间比在成像间隔730期间发生的成像束脉冲731的持续时间显著更短。附加地,在治疗间隔720期间,复位开关602闭合,使得光电二极管601被耦合到参考电压v
ref
并且无法产生电荷。因此,即使来自治疗束脉冲721的散射的x射线撞击图5中的闪烁体层503,光电二极管601也不能累积这样的潜在的图像噪声作为电荷,闪烁体层503生成入射在光电二极管601上的光子。
59.在每个成像间隔730期间,一个或多个成像束脉冲731被引导至靶标体积。在图7所示的实施例中,单个成像束脉冲731被图示。在一些实施例中,典型的成像束脉冲731(例如,图2中的成像x射线231的脉冲)的持续时间大约为10ms,并且被用来生成靶标体积的单个投影图像。在这样的实施例中,大约每30ms-50ms采集一个这样的图像。一个或多个成像束脉冲731在每个成像间隔730的照射部分732期间发生,并且在每个像素检测器元件310中累积的信号从每个成像间隔730的读出部分733中的每个像素读出。如图所示,复位开关602在成像间隔730期间断开,使得由成像束脉冲731生成并入射在光电二极管601上的光子将图像信号累积在光电二极管601中。此外,读出开关603在每个成像间隔730期间闭合,例如与x射线成像仪的其他光电二极管(未示出)同步并激活adc 611。这样,图像信号在每个成像间隔730的读出部分733期间,从x射线成像仪的每个光电二极管601读出。
60.如图所示,治疗间隔720和成像间隔730在时间上不重叠,而是在时域中交织。因此,在治疗间隔720期间发生的散射x射线不能被光电二极管601寄存为电荷。在图7a所示的实施例中,成像间隔730的持续时间735大于两个治疗束脉冲721之间的时间间隔725。结果,在其中治疗束脉冲721以规则间隔被引导穿过靶标体积的实施例中,一个或多个治疗束脉冲721必须被定时为在每个成像间隔730期间发生。在这样的实施例中,这样的治疗束脉冲721被抑制引导穿过靶标体积,使得光电二极管601不累积由散射的x射线引起的电荷。被抑制的治疗束脉冲721使用虚线来指示。在图7a所示的实施例中,成像间隔730被示出为包括经抑制的单个治疗束脉冲721。实际上,根据成像间隔730的持续时间735和两个治疗束脉冲721之间的时间间隔725,单个成像间隔730可以包括从经抑制的0个治疗束脉冲721到经抑制的100个或更多个治疗束脉冲721的任何值。
61.在一些实施例中,治疗控制计算机106(图1所示)执行用于确定光电二极管601的复位开关602是否断开的逻辑操作,从而指示成像间隔730正在进行。在这样的实施例中,治疗控制计算机106然后防止linac 204生成被禁止的一个或多个治疗束脉冲721。此外,在一些实施例中,在治疗控制计算机106中包括的剂量逻辑可以使得附加的治疗束脉冲721在治疗分次结束时被施加到靶标体积,以恢复由于消除所抑制的治疗束脉冲721而损失的剂量。
62.在图7a所示的实施例中,成像间隔730的持续时间735大于两个治疗束脉冲721之间的时间间隔725,并且一个或多个治疗束脉冲721被定时为在每个成像间隔730期间发生。通过减小成像间隔730的持续时间735,需要被抑制的治疗束脉冲721的数目可以被减少或消除,从而防止或减少由于被抑制的治疗束脉冲721造成的剂量损失。在一些实施例中,每个照射部分732的持续时间736通过在照射部分732期间递送更高功率的成像束脉冲731来减少。因此,在这样的实施例中,rt系统100的x射线成像仪包括具有高达约10kw的功率的x射线管。
63.备选地或附加地,在一些实施例中,每个读出部分733的持续时间737通过更快地
执行光电二极管601的读出操作来减少。例如,在每个像素检测器元件310中包括电压跟随器604使得能够非常快速地读出光电二极管601,这是因为像素检测器元件310的电路不受电路的电阻器-电容器(rc)时间常数的限制。
64.图7b是图示了根据本公开的另一实施例的在治疗间隔720期间施加治疗束脉冲721以及在成像间隔730期间施加成像束脉冲731的示意性时序图750。具体而言,图7b适用于图6a所示的像素检测器元件310的实施例。时序图750与图7a中的时序图700基本相似,不同之处在于,在这样的配置中,每当复位开关602闭合时,读出开关603闭合,使得防止了在该时间期间光电二极管601中的信号累积。
65.图8阐述了根据本公开的一个或多个实施例的放射疗法过程的流程图。方法可以包括如框801-840中的一个或多个所图示的一个或多个操作、功能或动作。尽管框以顺序被图示,但是这些框可以并行地和/或以与本文所述的顺序不同的顺序来执行。而且,各个框可以基于期望的实现方式而被组合为更少的框、被划分为附加的框和/或被去除。尽管结合图1至图7的系统描述了方法,但是本领域技术人员将理解,任何适当配置的放射疗法系统都在本公开的范围内。
66.在方法步骤之前,针对包括靶标体积510的数字体积500所设置的体积(3d)图像数据被采集。例如,患者被定位在rt系统100的卧榻107上,并且所设置的体积图像数据通过例如cbct图像采集来生成。所设置的体积图像数据包括数字体积500中每个体素501的图像信息。当通过cbct处理产生时,所设置的体积图像数据可以包括数字体积500的数百个不同的数字x射线投影图像。数字体积的自动分割和可变形配准然后被执行,随后进行患者位置调整。自动分割包括在数字体积500中划定靶标体积和处于风险的器官。可变形配准调整在较早的计划阶段针对靶标体积510和处于风险的任何器官生成的轮廓。可变形配准过程补偿了靶标体积510和处于风险中的器官的形状和相对位置的变化,变化例如由于胃、结肠和膀胱充盈、肿瘤缩小和其他因素而引起。当适用时,患者的当前位置还被调整,以将靶标体积510与现在修改的计划靶标体积精确对准。例如,卧榻107的位置可以被自动和/或手动地调整为使得靶标体积510与所修改的计划靶标体积对准。
67.当执行当前rt分次的一个治疗弧被发起时,方法800从步骤801开始。在步骤801中,患者屏气开始。在一些实施例中,rt治疗包括多个分次(即,多个治疗弧)。备选地,在其他实施例中,rt治疗由单个治疗弧组成。
68.在步骤802中,治疗控制计算机106使得机架210沿第一方向连续旋转通过治疗弧。
69.在步骤803中,在机架210沿第一方向连续旋转的同时,治疗控制计算机106开始将一系列治疗x射线脉冲(诸如治疗束脉冲721或821)引导至靶标体积510。
70.在步骤804中,治疗控制计算机106选择待被引导到靶标体积510的下一治疗束脉冲。
71.在步骤805中,治疗控制计算机106确定下一成像间隔730是否被定时为在所选的下一治疗束脉冲之前开始。如果是,则方法800进行到步骤820;如果不是,则方法800进行到步骤806。
72.在步骤806中,治疗控制计算机106确定所选的下一治疗束脉冲是否被定时为在成像间隔730期间发生。如果是,则方法800进行至步骤830;如果不是,则方法800进行到步骤807
73.在步骤807中,治疗控制计算机106使得下一所选的治疗束脉冲被引导至靶标体积510。
74.在步骤808中,治疗控制计算机106确定在治疗弧中是否存在任何剩余的治疗间隔720或成像间隔730。如果是,则方法800返回到步骤804,并且下一治疗束脉冲被选择;如果不是,则方法800进行到步骤840,并且方法800终止。
75.步骤820响应于治疗控制计算机106确定下一成像间隔730被定时为在所选的下一治疗束脉冲之前开始而被执行。在步骤820中,治疗控制计算机106使得下一成像间隔730开始。具体地,复位开关602在成像间隔730期间断开,使得x射线成像仪中的每个光电二极管601可以累积电荷,并且读出开关603闭合,使得图像信号从光电二极管601读出。在步骤820被执行时,方法800进行到步骤806。
76.步骤830响应于治疗控制计算机106确定所选的下一治疗束脉冲被定时为在成像间隔730期间发生而被执行。在步骤830中,治疗控制计算机106抑制一个或多个治疗束脉冲721在当前成像间隔730期间被引导穿过靶标体积。
77.在可选步骤831中,治疗控制计算机106更新被引导至靶标体积510的一系列治疗束脉冲721。
78.在一些实施例中,成像间隔介于一系列多个治疗束脉冲之间,并且结果,对治疗束脉冲的抑制未被执行。在图9中图示了一个这样的实施例。
79.图9是图示了根据本公开的一个实施例的在成像间隔930期间的成像束脉冲931的定时的示意性时序图900,成像间隔930的持续时间935比两个治疗束脉冲921之间的时间间隔925更短。在图9中也描绘了在治疗间隔930、复位开关602和读出开关603的断开和闭合以及adc 611的激活期间,治疗束脉冲921的定时。如图所示,时间间隔925的持续时间长于成像间隔930。因此,对治疗束脉冲921的抑制未被执行。
80.在一些实施例中,由于电压跟随器604启用的简短的读出部分933,成像间隔930的持续时间可以被缩短为小于时间间隔925。备选地或附加地,由于由足够高功率的成像x射线源启用的简短的照射部分932,成像间隔930的持续时间可以被缩短为小于时间间隔925。备选地或附加地,将每个治疗束脉冲921分离的时间间隔925可以被延长,例如高达至大约10ms。因此,在一个示例实施例中,x射线图像在大约1ms到5ms内采集,并且治疗束脉冲921每6ms(或更长时间)被引导至靶标体积。因此,每个成像间隔930可以在每个治疗束脉冲921之间执行。
81.电子快门
82.在一些实施例中,治疗x射线被递送到靶标体积,同时成像x射线也被递送到靶标体积,以生成靶标体积的体积图像数据。即,在成像x射线被x射线成像设备接收的成像间隔期间,治疗x射线的一个或多个脉冲也被引导至靶标体积。然而,在这样的实施例中,x射线成像设备的每个像素中包括的电子快门防止了图像信号在治疗x射线的脉冲被引导到靶标体积的成像间隔的各部分期间累积。以下结合图10至图12来描述一个这样的实施例。
83.图10是根据本公开的一个实施例的包括电子快门1002的像素检测器元件310的电路图1000。在该实施例中,像素检测器元件310使得x射线成像仪能够在成像间隔期间接收成像x射线,在成像间隔中,治疗x射线的脉冲也被引导至靶标体积。具体地,当治疗x射线被引导到靶标体积时,电子快门1002防止电荷在与像素检测器元件310相关联的信号积分器
1004中累积。
84.像素检测器元件310包括光电二极管1001、电子快门1002、读出/复位开关1003和信号积分器1004。在一些实施例中,像素检测器元件310还包括电容器复位开关1005。图10所示的像素检测器元件310的实施例可以被包括在rt系统100的x射线成像仪中,诸如被包括在图2中的x射线成像仪207或者图4中的第一x射线成像仪407或第二x射线成像仪409中。如图所示,光电二极管1001经由电子快门1002而被通信地耦合到参考电压v
ref
,并且经由信号积分器1004和读出/复位开关1003而被通信地耦合到数据线1010。在一些实施例中,v
ref
可以是任何合适的参考电压,例如,接地或0v。光电二极管1001是确实需要存储足够电荷来产生图像信号的二极管。例如,在一些实施例中,光电二极管1001被配置为不包括用于存储电荷的本征半导体区域的pn二极管。备选地,在一些实施例中,光电二极管1001被配置为可以存储比pn二极管显著更多的电荷的pin二极管。常规x射线成像仪中的像素检测器元件通常被配置为pin二极管。在一些实施例中,信号积分器1004是电压积分器、电流积分器或电荷积分器。在一些实施例中,信号积分器1004如图所示由单个晶体管1004a和单个电容器1004b形成。备选地,在其他实施例中,任何其他技术上可行的电荷积分设备可以被用作信号积分器1004。
85.在操作中,当由图5中的闪烁体材料503生成的光子入射在光电二极管1001上时,光电二极管1001产生电荷或图像信号。电荷被累积在信号积分器1004中,信号积分器1004被包括在像素检测器元件310中并且在光电二极管1001外部。当读出/复位开关1003闭合时,由光电二极管1001累积的电荷然后被读出到数据线1010,并通过adc 1011转换为数字信号,adc 1011在像素检测器元件310外部并且被耦合到数据线1010。在一些实施例中,电容器复位开关1005也闭合来将信号积分器1004复位。根据各种实施例,在治疗束脉冲被引导至靶标体积510的时间间隔期间,电子快门1002闭合,使得信号积分器1004不接收由散射的治疗束脉冲引起的附加图像信号。因此,由治疗束脉冲生成的噪声被防止由光电二极管1001捕获。图11中图示了一个这样的实施例。
86.图11是图示了根据本公开的一个实施例的在成像间隔1130期间施加治疗束脉冲1121和成像束脉冲1131的示意性时序图1100。在图11中还描绘了电子快门1002、读出/复位开关1003以及adc 1011的激活相对于治疗束脉冲1121和成像束脉冲1131的断开和闭合定时。
87.成像间隔1130包括照射部分1132和读出部分1133。在照射部分1132期间,至少一个成像束脉冲1131被引导至靶标体积并且被rt系统100的x射线成像仪接收。在一些实施例中,典型的成像束脉冲1131(例如,图2中的成像x射线231的成像束脉冲)的持续时间大约为10ms,并且被用来生成靶标体积的单个投影图像。在这样的实施例中,大约每30ms-50ms采集一个这样的图像。在读出部分1133期间,对于在x射线成像仪中包括的每个像素检测器元件310,该像素检测器元件310的信号积分器1004中存储的图像信号被读出到adc 1011。具体地,读出/复位开关1003在读出部分1133期间闭合,例如与x射线成像仪的其他像素检测器元件310(未示出)同步并且与adc 1011的激活同步。以这种方式,在每个成像间隔1130的读出部分1133期间,图像信号从x射线成像仪的每个信号积分器1004被读出。
88.如图所示,在成像间隔1130之前、期间和之后,一个或多个治疗束脉冲1121被引导至靶标体积。在一些实施例中,典型的治疗束脉冲1121(例如,图2中的治疗束230的脉冲)的
持续时间为大约5μs,并且大约每1ms-10ms被递送。根据图11所示的实施例,当治疗束脉冲1121被引导至靶标体积510时,电子快门1002闭合。因此,当电子快门1002闭合时,光电二极管1001的输出被耦合至接地,并且信号积分器1004不能从光电二极管1001接收附加的图像信号。因此,即使来自治疗束脉冲1121的散射x射线撞击图5中的闪烁体层503并且生成入射在光电二极管1001上的光子,信号积分器1004也不能将这种潜在的图像噪声累积为电荷。
89.图12阐述了根据本公开的一个或多个实施例的放射疗法过程的流程图。方法可以包括框1201-1230中的一个或多个所示出的一个或多个操作、功能或动作。尽管框以顺序被图示,但是这些框可以并行地和/或以与本文所述的顺序不同的顺序来执行。而且,各种框可以基于期望的实现方式而被组合为更少的框、被划分为附加的框和/或被消除。尽管结合图1至图5、图10和图11的系统描述了方法,但是本领域技术人员将理解,任何适当配置的放射疗法系统在本公开的范围内。
90.在方法步骤之前,如以上结合方法800所述,执行类似的设置过程,包括采集针对数字体积500的体积图像数据、执行自动分割和可变形配准以及在rt治疗之前,将患者定位。
91.当执行当前rt分次的一个治疗弧被发起时,方法1200从步骤1201处开始。在步骤1201中,患者屏气开始。在一些实施例中,rt治疗包括多个分次。备选地,在其他实施例中,rt治疗由单个治疗弧组成。
92.在步骤1202中,治疗控制计算机106使得机架210沿第一方向连续旋转穿过治疗弧。
93.在步骤1203中,在机架210沿第一方向连续旋转的同时,治疗控制计算机106开始将一系列治疗x射线脉冲、诸如治疗束脉冲721或821引导至靶标体积510。
94.在步骤1204中,治疗控制计算机106选择待被引导至靶标体积510的下一治疗束脉冲。
95.在步骤1205中,治疗控制计算机106确定所选的下一治疗束脉冲是否被定时为在成像间隔1130期间发生。如果是,则方法1200进行到步骤1206;如果不是,则方法1200进行到步骤1210。
96.在步骤1206中,在将所选的下一治疗束脉冲引导至靶标体积510之前,治疗控制计算机106使得每个像素检测器元件310中的电子快门1002闭合。例如,在一些实施例中,治疗控制计算机106使得光电检测器10001的输出被通信地耦合到接地。因此,治疗控制计算机106防止图像信号在x射线成像仪的每个信号积分器1004中累积。
97.在步骤1207中,治疗控制计算机106使得所选的下一治疗束脉冲被引导至靶标体积510。
98.在步骤1208中,治疗控制计算机106使得每个像素检测器元件310中的电子快门1002断开。例如,在一些实施例中,治疗控制计算机106使得来自光电检测器10001的输出从接地通信地解耦。因此,治疗控制计算机106使得图像信号能够在x射线成像仪的每个信号积分器1004中再次累积。
99.在步骤1210中,治疗控制计算机106确定在治疗弧中是否存在任何剩余的治疗束脉冲。如果是,则方法1200返回步骤1204,并且下一治疗束脉冲被选择;如果不是,则方法1200进行到步骤820,并且方法800终止。
100.在步骤1210中,治疗控制计算机106将所选的下一治疗束脉冲引导至靶标体积510,并且方法1200进行到步骤1210。
101.作为例示,本公开的实施例已针对包括圆形机架并生成靶标体积的体积图像数据的rt系统进行了描述。然而,本文所述的各种实施例也可以在具有其他配置和/或执行靶标体积的二维成像的rt系统中有利地实现。例如,本公开的各种实施例可以被有利地应用于被配置为执行荧光检查、串行成像或触发成像的放射系统。在这样的实施例中,x射线成像仪、治疗束发生器和/或成像x射线源可以不被耦合到旋转机架,或者可以在机架静止时使用。
102.上述实施例的实现方式使得x射线成像仪能够在不会由于治疗束散射而引起图像噪声的情况下,在igrt期间收集靶标体积的成像数据。有利地,靶标体积相对于放射疗法系统的运动或变形和/或处于危险中的周围器官的变化可以被更可靠地检测和补偿。因此,能够更准确地适应处于危险中的器官以及靶标体积的形状和相对位置,从而有助于获得更好的治疗效果。
103.已出于例示的目的给出了各种实施例的描述,但是这些描述并不旨在是穷举的或限于所公开的实施例。在不脱离所描述的实施例的范围和精神的情况下,许多修改和变型对于本领域普通技术人员将是显而易见的。
104.本实施例的各方面可以被体现为系统、方法或计算机程序产品。因此,本公开的各方面可以采取完全硬件实施例、完全软件实施例(包括固件、驻留软件、微代码等)或组合了通常可以被整体称为“电路”、“模块”或“系统”的软件和硬件方面的实施例的形式。此外,本公开的各方面可以采取在其上体现了计算机可读程序代码的一个或多个计算机可读介质中体现的计算机程序产品的形式。
105.一个或多个计算机可读介质的任何组合可以被利用。计算机可读介质可以是计算机可读信号介质或计算机可读存储介质。计算机可读存储介质可以是例如但不限于电子、磁性、光学、电磁、红外或半导体系统、装置或设备,或前述的任何合适的组合。计算机可读存储介质的更具体示例(非详尽列表)将包括以下内容:具有一个或多个电线的电连接、便携式计算机磁盘、硬盘、随机存取存储器(ram)、只读存储器(rom)、可擦除可编程只读存储器(eprom或闪存)、光纤、便携式光盘只读存储器(cd-rom)、光学存储设备、磁存储设备或任何其他前述的适当组合。在本文挡的上下文中,计算机可读存储介质可以是可以包含或存储供指令执行系统、装置或设备使用或与其结合使用的程序的任何有形介质。
106.尽管本文已公开了各个方面和实施例,但是其他方面和实施例对于本领域技术人员将是显而易见的。本文所公开的各个方面和实施例是出于例示的目的,而不是旨在进行限制,其中真实的范围和精神由所附权利要求指示。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。