1.本发明属于医药技术领域,具体涉及一种改进的复方苦参注射液uplc 检测方法。
背景技术:
2.复方苦参注射液是由苦参和白土苓2味中药经现代科学方法精制而成的中药注射液,收载于国家药品标准中,具有清热利湿,凉血解毒,散结止痛的功效,用于癌肿疼痛、出血。现代研究表明其具有抗肿瘤、抗炎、镇痛、提高机体免疫力等多种药理作用,临床上广泛用于非小细胞肺癌、原发性肝癌、消化道癌及恶性胸腔积水等重症疾病的辅助治疗。
3.生物碱是复方苦参注射液主要的药性成分。现有复方苦参注射液国家药品标准(ws
3-b-2752-97-2014)中只收载了苦参碱、氧化苦参碱及甲基氧化偶氮甲醇樱草糖苷的hplc含量测定方法以及指纹图谱检测,缺乏较为多样的科学的质量评价方法。超高效液相色谱法具有分离效率高、分析速度快、检测灵敏度高等特点,已广泛应用于中药及中成药的检测。通过查阅相关文献,发现苦参在uplc方面的研究较少,而白土苓未有该方面的研究。
4.张黄琴等“山西产苦参花中生物碱类和黄酮类成分的分析与评价”采用uplc-tq-ms联用技术,对山西长治产苦参花中7个生物碱类及7个黄酮类成分进行分析测定。该方法采用乙腈-醋酸铵作为流动相,与标准中指纹图谱条件较为相似,注射液在本条件下色谱峰形较差。
5.在翁泽斌等“山西产苦参种子生物碱类化学成分分析及其资源化价值探讨”中,采用uplc-qtof-ms与uplc-tq-ms联用技术分析了苦参成熟干燥种子中生物碱类资源性化学成分的组成及其含量,该方法同样采用了乙腈-醋酸铵作为流动相,不太适用于复方苦参注射液。
6.因此,为了更科学全面的评价复方苦参注射液产品的内在质量,有必要提供一种能够同时完成复方苦参注射液多种成分的含量测定与指纹图谱的检测方法,为复方苦参注射液中质量控制提供快速、高效的技术方法,减轻检验工作量。
技术实现要素:
7.针对以上技术现状,本发明提供一种改进的利用uplc的复方苦参注射液的活性成分含量及指纹图谱的检测方法。具体发明如下:
8.本发明所述复方苦参注射液的活性成分含量及指纹图谱的检测方法采用超高效液相色谱法进行检测,所述超高效液相色谱条件包括色谱柱为 acquity uplc csh
tm c
18
;所述活性成分为苦参碱、氧化苦参碱、甲基氧化偶氮甲醇樱草糖苷、槐果碱、氧化槐果碱以及槐定碱。
9.本发明方法中,作为实施方案之一,所述超高效液相色谱条件中流动相为0.15%-0.25%磷酸二氢钾溶液-甲醇梯度洗脱,优选0.2%磷酸二氢钾溶液-甲醇梯度洗脱。
10.本发明方法中,作为实施方案之一,所述超高效液相色谱条件中洗脱梯度如下:
[0011][0012]
本发明方法中,作为实施方案之一,所述超高效液相色谱条件包括柱温为28℃-32℃,优选30℃。
[0013]
本发明方法中,作为实施方案之一,所述超高效液相色谱条件包括流速为0.3ml/min。
[0014]
本发明方法中,作为实施方案之一,所述超高效液相色谱条件包括检测波长为209nm-213nm,优选211nm;
[0015]
本发明方法中,作为实施方案之一,所述超高效液相色谱条件包括进样量为0.8μl-1.2μl,优选1μl。
[0016]
本发明方法中,作为实施方案之一,超高效液相色谱法进一步包括:
[0017]
(1)空白溶液配制:磷酸调节磷酸二氢钾溶液的ph值至3.0,0.2%磷酸二氢钾溶液-甲醇=85∶15的混合溶液,过滤即得。
[0018]
本发明方法中,作为实施方案之一,采用超高效液相色谱法进一步包括:
[0019]
(2)对照品溶液配制:
[0020]
精密称取苦参碱对照品,氧化苦参碱对照品,氧化槐果碱对照品适量,加空白溶液制成每1ml含苦参碱0.33mg,氧化苦参碱0.85mg,氧化槐果碱 0.25mg的混合对照品溶液ⅰ,摇匀,即得;
[0021]
精密称取槐果碱对照品,槐定碱对照品,甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成每1ml含槐果碱0.09mg,槐定碱0.08mg,甲基氧化偶氮甲醇樱草糖苷0.08mg的混合对照品溶液ⅱ,摇匀,即得;
[0022]
精密量取混合对照品溶液ⅰ、ⅱ2ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀即得;可选择地同法制备2份。
[0023]
本发明方法中作为实施方案之一,对照品溶液中对照品的含量可以在以下的范围内:
[0024]
苦参碱优选范围为0.28-0.40mg,最佳范围为0.33mg;氧化苦参碱优选范围为0.72-1.06mg,最佳范围为0.85mg;氧化槐果碱优选范围为 0.21-0.31mg,最佳范围为0.25mg;槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷优选范围均为0.07-0.11mg,最佳范围分别为0.09mg,0.08mg,0.08mg。
[0025]
本发明方法中,作为实施方案之一,超高效液相色谱法进一步包括:
[0026]
(3)供试品溶液配制:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0027]
本发明方法中,作为实施方案之一,本发明所述复方苦参注射液中活性成分含量的检测方法,所述方法包括:
[0028]
超高效液相色谱条件为:
[0029][0030]
(1)空白溶液配制:磷酸调节磷酸二氢钾溶液的ph值至3.0,0.2%磷酸二氢钾溶液-甲醇=85∶15的混合溶液,过滤即得。
[0031]
(2)对照品溶液配制:
[0032]
精密称取苦参碱对照品,氧化苦参碱对照品,氧化槐果碱对照品适量,加空白溶液制成每1ml含苦参碱0.33mg,氧化苦参碱0.85mg,氧化槐果碱 0.25mg的混合对照品溶液ⅰ,摇匀,即得;
[0033]
精密称取槐果碱对照品,槐定碱对照品,甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成每1ml含槐果碱0.09mg,槐定碱0.08mg,甲基氧化偶氮甲醇樱草糖苷0.08mg的混合对照品溶液ⅱ,摇匀,即得;
[0034]
精密量取混合对照品溶液ⅰ、ⅱ2ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀即得;可选择地,同法制备2份;
[0035]
(3)供试品溶液配制:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0036]
(4)按空白溶液、对照品、供试品进样顺序,注入液相色谱仪,记录色谱图,外标法计算各活性成分的含量。
[0037]
本发明方法中,作为实施方案之一,本发明所述复方苦参注射液的指纹图谱的检测方法,其特征在于,所述方法包括构建复方苦参注射液的含有苦参碱、氧化苦参碱、甲基氧化偶氮甲醇樱草糖苷、槐果碱、氧化槐果碱、槐定碱、番石榴酸、槐胺碱、以及三叶豆紫檀苷的指纹图谱。
[0038]
本发明方法中,作为实施方案之一,所述方法包括:超高效液相色谱条件为:
[0039][0040]
(1)空白溶液配制:磷酸调节磷酸二氢钾溶液的ph值至3.0,0.2%磷酸二氢钾溶液-甲醇=85∶15的混合溶液,过滤即得。
[0041]
(2)对照品溶液配制:
[0042]
精密称取苦参碱对照品,氧化苦参碱对照品,氧化槐果碱对照品适量,加空白溶液制成每1ml含苦参碱0.33mg,氧化苦参碱0.85mg,氧化槐果碱 0.25mg的混合对照品溶液ⅰ,摇匀,即得;
[0043]
精密称取槐果碱对照品,槐定碱对照品,甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成每1ml含槐果碱0.09mg,槐定碱0.08mg,甲基氧化偶氮甲醇樱草糖苷0.08mg的混合对照品溶液ⅱ,摇匀,即得;
[0044]
精密量取混合对照品溶液ⅰ、ⅱ2ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀即得,可选择地同法制备2份;
[0045]
(3)供试品溶液配制:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0046]
(4)按空白溶液、对照品、供试品进样顺序进样,构建复方苦参注射液的含有苦参碱、氧化苦参碱、甲基氧化偶氮甲醇樱草糖苷、槐果碱、氧化槐果碱、槐定碱、番石榴酸、槐胺碱、以及三叶豆紫檀苷的指纹图谱
[0047]
(5)按空白溶液、对照品、供试品进样顺序,注入液相色谱仪,记录色谱图,外标法计算各活性成分的含量。
[0048]
本发明方法中,作为实施方案之一,所述方法包括:
[0049]
以氧化苦参碱为参考,所述共有特征峰的相对保留时间分别为:槐胺碱的峰相对保留时间为0.389
±
0.02;甲基氧化偶氮樱草糖苷的峰相对保留时间为0.469
±
0.04;苦参碱的峰相对保留时间为0.637
±
0.04;槐果碱的峰相对保留时间为0.767
±
0.03;槐定碱的峰相对保留时间为0.819
±
0.02;氧化槐果碱的峰相对保留时间为0.925
±
0.02;氧化苦参碱的峰相对保留时间为1.0;番石榴酸的峰相对保留时间为1.055
±
0.03;三叶豆紫檀苷的峰相对保留时间为2.097
±
0.05。
[0050]
本发明方法中,作为实施方案之一,所述方法进一步包括,氧化苦参碱、苦参碱、氧化槐果碱峰面积的rsd不得大于2.0%,保留时间rsd应不大于2.0%,槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷峰面积的rsd 不得大于3.0%,保留时间rsd应不大于3.0%,含量检测指标的理论板数不得低于3000,拖尾因子不得大于2.0。
[0051]
本发明中,作为实施方案之一,以7号峰为参考,共有特征峰的相对峰面积分别为:1号峰相对峰面积为0.032;2号峰相对峰面积为0.073;3 号峰相对峰面积为0.466;4号峰相对峰面积为0.183;5号峰相对峰面积为 0.107;6号峰相对峰面积为0.422;7号峰相对峰面积为1.0;8号峰相对峰面积为0.222;9号峰相对峰面积为0.056;其中所述1号峰为槐胺碱,2号峰为甲基氧化偶氮樱草糖苷,3号峰为苦参碱,4号峰为槐果碱,5号峰为槐定碱,6号峰为氧化槐果碱,7号峰为氧化苦参碱,8号峰为番石榴酸,9 号峰为三叶豆紫檀苷。
[0052]
相对于现有复方苦参注射液的检测方法,本发明采用超高效液相色谱法,能够同时测定复方苦参注射液中6种成分,并用该方法构建色谱指纹图谱,为复方苦参注射液中质量控制提供快速、高效的技术方法,减轻检验工作量。
附图说明
[0053]
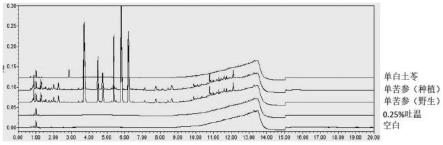
图1为实施例1的空白与阴性样品结果图。
[0054]
图2为实施例1的6个指标成分线性图。
[0055]
图3-1为实施例2的标准对照指纹图谱。
[0056]
图3-2为实施例2的供试品指纹图谱。
[0057]
图4为实施例2的重复性指纹图谱。
[0058]
图5为实施例2的精密度指纹图谱。
[0059]
图6为实施例2的稳定性指纹图谱。
[0060]
图7-1为实施例2的不同色谱柱指纹图谱。
[0061]
图7-2为实施例2的不同仪器指纹图谱。
[0062]
图7-3为实施例2的仪器1色谱柱2中10批样品叠加图谱。
[0063]
图7-4为实施例2的仪器1色谱柱2对照指纹图谱。
[0064]
图7-5为实施例2的仪器1色谱柱3中10批样品叠加图谱。
[0065]
图7-6为实施例2的仪器1色谱柱3对照指纹图谱。
[0066]
图7-7为实施例2的仪器2色谱柱1中10批样品叠加图谱。
[0067]
图7-8为实施例2的仪器2色谱柱1对照指纹图谱。
[0068]
图7-9为实施例2的仪器3色谱柱1中10批样品叠加图谱。
[0069]
图7-10为实施例2的仪器3色谱柱1对照指纹图谱。
[0070]
图7-11为实施例2的不同条件下对照指纹图谱叠加图谱。
[0071]
图8为实施例2的生产工艺关键点指纹图谱。
[0072]
图9为实施例3-1的结果图,从下到上的曲线为:供试品1、供试品2。
[0073]
图10-1为实施例3-2中色谱条件1的结果图,从下到上的曲线为:样品、槐果碱、氧化槐果碱、苦参碱与氧化苦参碱;
[0074]
图10-2为实施例3-2中色谱条件2的结果图;
[0075]
图10-3为实施例3-2中色谱条件3的结果图。
[0076]
图10-4为实施例3-2中色谱条件4的结果图;
[0077]
图10-5分别为实施例3-2中色谱条件5的结果图;
[0078]
图10-6为实施例3-2中各个对照品按上述条件进样后与供试品的叠加图,其中色谱峰定位(从下到上曲线)为:样品、苦参碱、氧化苦参碱、槐果碱、氧化槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷、番石榴酸、三叶豆紫檀苷、槐胺碱、n-甲基金雀花碱。
[0079]
图11-1为实施例3-3中方法1的结果图。
[0080]
图11-2为实施例3-3中方法2的结果图;
[0081]
图11-3为实施例3-3中方法3的结果图。
[0082]
图11-4为实施例3-3的方法4的结果图。
[0083]
图11-5为实施例3-3中方法5的结果图。
[0084]
图11-6为实施例3-3中方法6的结果图;
[0085]
图12-1为实施例3-4中考察条件1的结果图;
[0086]
图12-2为实施例3-4中考察条件2的结果图;
[0087]
图12-3为实施例3-4中考察条件3的结果图;
[0088]
图12-4为实施例3-4中考察条件4的结果图;
[0089]
图12-5为实施例3-4中考察条件5的结果图;
[0090]
图12-6为实施例3-4中考察条件6的结果图;
[0091]
图12-7为实施例3-4中考察条件7的结果图。
具体实施方式
[0092]
以下实施例和试验例用于进一步阐述本发明,但不以任何的方式限制本发明的有效范围。
[0093]
仪器
[0094][0095]
对照品
[0096][0097][0098]
实施例1的供试品
[0099]
名称批号来源复方苦参注射液20181138山西振东制药股份有限公司复方苦参注射液20181034山西振东制药股份有限公司复方苦参注射液20181139山西振东制药股份有限公司
复方苦参注射液20181203山西振东制药股份有限公司复方苦参注射液20181204山西振东制药股份有限公司复方苦参注射液20181209山西振东制药股份有限公司复方苦参注射液20181212山西振东制药股份有限公司复方苦参注射液20181213山西振东制药股份有限公司复方苦参注射液20181214山西振东制药股份有限公司复方苦参注射液20181215山西振东制药股份有限公司
[0100]
实施例2的供试品
[0101][0102][0103]
试剂
[0104]
名称批号来源级别磷酸二氢钾018823mreadhplc磷酸0160318北京化工厂分析级甲醇10985407 902默克两合有限公司hplc
[0105]
实施例1复方苦参注射液活性成分的检测方法
[0106]
1.色谱条件、样品配制、系统适用性要求、计算公式、限度要求
[0107][0108]
2.验证具体内容
[0109]
2.1系统适用性
[0110]
(1)实验步骤
[0111]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0112]
对照品溶液配制:精密称取苦参碱对照品,氧化苦参碱对照品,氧化槐果碱对照品适量,加空白溶液制成每1ml含苦参碱0.33mg,氧化苦参碱 0.85mg,氧化槐果碱0.25mg的混合对照品溶液ⅰ,摇匀,即得;
[0113]
精密称取槐果碱对照品,槐定碱对照品,甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成每1ml含槐果碱0.09mg,槐定碱0.08mg,甲基氧化偶氮甲醇樱草糖苷0.08mg的混合对照品溶液ⅱ,摇匀,即得。
[0114]
精密量取混合对照品溶液ⅰ、ⅱ2ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀。
[0115]
供试品溶液配制:精密量取复方苦参注射液1ml(批号为20181138),置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0116]
进样程序要求
[0117]
进样顺序
[0118]
顺序样品针数1空白溶液1针2对照品溶液5针(连续进针)
3供试品溶液1针
[0119]
(2)结果报告
[0120]
对照品溶液连续进样5次的峰面积及保留时间的rsd值。
[0121]
表2.1-1对照品溶液峰面积及保留时间结果
[0122][0123]
表2.1-2系统适用性结果
[0124][0125][0126]
(3)结论
[0127]
从结果中来看,对照品溶液连续进样5次,氧化苦参碱、苦参碱、氧化槐果碱峰面积的rsd均小于2.0%,保留时间rsd均小于2.0%,槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷峰面积的rsd均小于3.0%,保留时间rsd均小于3.0%;六个指标成分的理论板数大于3000,拖尾因子均小于 2.0,符合要求。
[0128]
2.2专属性
[0129]
(1)实验步骤
[0130]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0131]
阴性样品溶液配制:精密量取单苦参注射液(野生及种植)、单白土苓注射液各1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为阴性样品溶液。
[0132]
0.25%吐温溶液配制:称定0.25g吐温80,加水溶解至100ml,摇匀,滤过,取续滤液作为0.25%吐温溶液。
[0133]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0134]
供试品溶液配制:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,备用。
[0135]
滤膜干扰样品配制:取供试品溶液(批号为20181138),一份离心;一份滤过,弃去不同的体积(1ml、3ml、5ml、7ml、9ml)。
[0136]
进样程序要求
[0137]
进样顺序
[0138][0139][0140]
(2)结果报告参见图1及下表。
[0141]
表2.2-1滤膜干扰实验结果 (弃去不同体积相对于离心样品的面积百分比)
[0142][0143]
(3)结论
[0144]
从结果中来看,空白溶液、空白流动相、0.25%吐温80溶液对样品没有干扰,单苦参阴性样品溶液(野生苦参及种植苦参)对甲基氧化偶氮甲醇樱草糖苷无干扰,单白土苓阴性样品溶液对生物碱无干扰。
[0145]
弃去不同体积后供试品溶液指标成分面积与离心供试品溶液指标成分面积的百分比相对含量在95.0%~102.0%之间,吸附可忽略不计。
[0146]
2.3线性和范围
[0147]
(1)实验步骤
[0148]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0149]
线性贮备液配制:精密称取苦参碱对照品,氧化苦参碱对照品,氧化槐果碱对照品适量,加空白溶液制成每1ml含苦参碱0.33mg,氧化苦参碱 0.85mg,氧化槐果碱0.25mg的混合对照品溶液ⅰ,摇匀,即得;精密称取槐果碱对照品,槐定碱对照品,甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成每1ml含槐果碱0.09mg,槐定碱0.08mg,甲基氧化偶氮甲醇樱草糖苷0.08mg的混合对照品溶液ⅱ,摇匀,即得。
[0150]
对照品溶液1:精密量取混合对照品溶液ⅰ、ⅱ各0.5ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀。
[0151]
对照品溶液2:精密量取混合对照品溶液ⅰ、ⅱ各1ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀。
[0152]
对照品溶液3:精密量取混合对照品溶液ⅰ、ⅱ各2ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀。
[0153]
对照品溶液4:精密量取混合对照品溶液ⅰ、ⅱ各3ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀。
[0154]
对照品溶液5:精密量取混合对照品溶液ⅰ、ⅱ各4ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀。
[0155]
进样程序要求
[0156]
进样顺序
[0157][0158][0159]
(2)结果报告
[0160]
各指标成分的回归方程及相关系数及线性图结果参见图2。
[0161]
(3)结论
[0162]
线性相关系数≥0.999,符合标准。
[0163]
2.4准确度
[0164]
(1)实验步骤
[0165]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0166]
对照品溶液配制:参引2.1项下对照品溶液配制方法,同法配制两份。
[0167]
50%回收率溶液配制:精密量取复方苦参注射液0.5ml,置50ml量瓶中,分别加入混合对照品溶液ⅰ、ⅱ各2.5ml后,加空白溶液至刻度,摇匀,滤过,作为50%回收率溶液(同法配制3份)。
[0168]
100%回收率溶液配制:精密量取复方苦参注射液0.5ml,置50ml量瓶中,分别加入混合对照品溶液ⅰ、ⅱ各5ml后,加空白溶液至刻度,摇匀,滤过,作为100%回收率溶液(同法配制3份)。
[0169]
150%回收率溶液配制:精密量取复方苦参注射液0.5ml,置50ml量瓶中,分别加入混合对照品溶液ⅰ、ⅱ各7.5ml后,加空白溶液至刻度,摇匀,滤过,作为150%回收率溶液(同法配制3份)。
[0170]
进样顺序
[0171][0172][0173]
(2)结果报告
[0174]
表2.4-1甲基氧化偶氮甲醇樱草糖苷含量回收率测试结果
[0175][0176]
表2.4-2苦参碱含量回收率测试结果
[0177][0178]
表2.4-3槐果碱含量回收率测试结果
[0179][0180]
表2.4-4槐定碱含量回收率测试结果
[0181][0182][0183]
表2.4-5氧化槐果碱含量回收率测试结果
[0184][0185]
表2.4-6氧化苦参碱含量回收率测试结果
[0186][0187]
(3)结论
[0188]
供试品中苦参碱、氧化苦参碱、氧化槐果碱、槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷回收率范围均在95%~105%之间,9份回收率rsd 均小于3%,符合要求。
[0189]
2.5重复性
[0190]
(1)实验步骤
[0191]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0192]
对照品溶液配制:参引2.1项下对照品溶液配制方法,同法配制两份。
[0193]
供试品溶液配制:精密量取复方苦参注射液1ml(批号2081138),置 50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。平行操作6份。
[0194]
进样程序要求
[0195]
进样顺序
[0196]
顺序样品针数1空白溶液1针2对照品1溶液5针(连续测试)3对照品2溶液2针4供试品-1溶液1针5供试品-2溶液1针6供试品-3溶液1针7供试品-4溶液1针8供试品-5溶液1针9供试品-6溶液1针10对照品1溶液1针
[0197]
(2)结果报告
[0198]
表2.5重复性测试结果
[0199][0200]
(3)结论
[0201]
从结果中来看,6份供试品中苦参碱、氧化苦参碱、氧化槐果碱含量结果rsd均小于3.0%,槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷含量结果rsd均小于4.0%,表明供试品重复性良好。
[0202]
2.6精密度
[0203]
(1)实验步骤
[0204]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0205]
对照品溶液配制:参引2.1项下对照品溶液配制方法,同法配制两份。
[0206]
供试品溶液配制:精密量取复方苦参注射液1ml(批号为20181138),置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0207]
进样程序要求
[0208]
进样顺序
[0209][0210][0211]
(2)结果报告
[0212]
表2.6精密度测试结果
[0213][0214]
(3)结论
[0215]
从结果中可以看出,连续进样6针,供试品中苦参碱、氧化苦参碱、氧化槐果碱含量结果rsd均小于3.0%,槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷含量结果rsd均小于4.0%,说明供试品精密度良好。
[0216]
2.7溶液稳定性
[0217]
(1)实验步骤
[0218]
空白溶剂配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0219]
对照品溶液配制:参引2.1项下对照品溶液配制方法,同法配制两份。
[0220]
供试品溶液配制:精密量取复方苦参注射液1ml(批号为20181138),置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0221]
进样程序要求
[0222]
进样顺序
[0223]
顺序样品针数1空白溶液1针2对照品1溶液5针(连续测试)3对照品2溶液2针4供试品-0h1针5供试品-1h1针6供试品-2h1针7供试品-4h1针8供试品-8h1针9供试品-16h1针10供试品-24h1针11对照品1溶液1针
[0224]
(2)结果报告
[0225]
表2.7稳定性测试结果
[0226][0227][0228]
(3)结论
[0229]
从结果中来看对照品溶液与供试品溶液放置24小时,供试品中苦参碱、氧化苦参碱、氧化槐果碱含量结果rsd小于3.0%,槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷含量结果rsd小于4.0%,表明供试品在24小时内稳定。
[0230]
计算各时间点指标成分面积与0小时指标成分面积的百分比,对照品和供试品溶液每个时间点的结果与初始结果相比,相对含量在
[0231]
98.0%~102.0%之间,溶液稳定性良好。
[0232]
2.8耐用性
[0233]
(1)实验步骤
[0234]
变动的色谱条件见下表。
[0235][0236]
空白溶液配制:0.2%磷酸二氢钾溶液-甲醇=85∶15混合溶液,过滤即得。
[0237]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0238]
供试品溶液配制:分别精密量取各批次复方苦参注射液1ml,置50ml 量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0239]
进样程序要求。
[0240]
(不同考察条件均按此进样顺序进样)
[0241]
进样顺序
[0242]
顺序样品针数1空白溶液1针2对照品1溶液5针3对照品2溶液2针4供试品-11针5供试品-21针6供试品-3~供试品-9每供试品1针7供试品-101针8对照品1溶液1针
[0243]
注:对照品和供试品溶液在检测时间范围内稳定则不用重新配制,若溶液不稳定,改变色谱条件时,需要临用重新配制对照品及供试品溶液。
[0244]
(2)结果报告
[0245]
表2.9含量耐用性测试结果
[0246]
[0247]
[0248][0249]
(3)结论
[0250]
供试品溶液,不同条件下苦参碱、槐果碱、氧化槐果碱、氧化苦参碱含量基本一致,各批次样品rsd值均小于3%,甲基氧化偶氮甲醇樱草糖苷rsd值小于5%,耐用性良好。在仪器2色谱柱1条件下槐定碱各批次样品含量均较低,因此rsd值小于10%,耐用性在可接受范围。
[0251]
实施例2复方苦参注射液uplc指纹图谱方法学验证考察
[0252]
1.色谱条件、洗脱条件、样品配制等
[0253][0254]
2验证内容
[0255]
2.1系统适用性
[0256]
(1)实验步骤
[0257]
空白溶液配制:甲醇-0.2%磷酸二氢钾=15∶85,过滤即得。
[0258]
对照品溶液配制:精密称取苦参碱对照品,氧化苦参碱对照品,氧化槐果碱对照品适量,加空白溶液制成每1ml含苦参碱0.33mg,氧化苦参碱 0.85mg,氧化槐果碱0.25mg的混合对照品溶液ⅰ,摇匀,即得;精密称取槐果碱对照品,槐定碱对照品,甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成每1ml含槐果碱0.09mg,槐定碱0.08mg,甲基氧化偶氮甲醇樱草糖苷0.08mg的混合对照品溶液ⅱ,摇匀,即得;精密称取三叶豆紫檀苷对照品,槐胺碱对照品,n-甲基金雀花碱对照品适量,加空白溶液制成每1ml含三叶豆紫檀苷0.08mg,槐胺碱0.08mg,n-甲基金雀花碱0.09mg 的混合对照品溶液ⅲ,摇匀,即得。精密量取混合对照品溶液ⅰ、ⅱ、ⅲ各2ml,置10ml量瓶中,用空白溶液稀释至刻度,摇匀,即得。
[0259]
供试品溶液:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0260]
进样顺序及要求见下表。
[0261]
进样顺序
[0262]
顺序样品针数1空白溶液1针2对照品溶液5针(连续进针)3供试品溶液1针
[0263]
(2)结果报告
[0264]
对照品溶液连续进样5次的峰面积及保留时间的rsd值。
[0265]
表2.1-1对照品溶液峰面积及保留时间结果
[0266][0267]
表2.1-2系统适用性结果
[0268][0269]
(3)结论
[0270]
从结果中来看,对照品溶液连续进样5次,氧化苦参碱、苦参碱、氧化槐果碱峰面积的rsd均小于2.0%,保留时间rsd均小于2.0%,槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷峰面积的rsd均小于3.0%,保留时间 rsd均小于3.0%;六个指标成分的理论板数大于3000,拖尾因子小于2.0,符合要求。
[0271]
2.2指纹图谱建立
[0272]
(1)实验步骤
[0273]
空白溶液:甲醇-0.2%磷酸二氢钾=15∶85混合溶液,过滤即得。
[0274]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0275]
各批次供试品溶液:分别精密量取各批次复方苦参注射液1ml,置50ml 量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0276]
进样顺序及要求见下表。
[0277]
进样顺序
[0278][0279][0280]
(2)结果报告
[0281]
以10批复方苦参注射液的色谱指纹图谱为基础,使用药典委员会推荐的《中药色谱指纹图谱相似度评价系统》2012版进行数据处理,将供试品 1(s1)色谱峰作为参照图谱,采用中位数法,时间窗0.1,经多点校正后,进行全峰匹配,生成标准对照指纹图谱及共有模式。参见图3-1~图3-2及下表。
[0282]
表2.2-1各批次指纹图谱与对照指纹相似度结果
[0283][0284][0285]
表2.2-2各批次非共有峰结果
[0286]
供试品非共有峰面积总峰面积非共有峰面积占比%2018113874.012242.643.302018113966.452476.852.682018120346.582329.112.002018120456.142279.622.462018120957.612291.592.512018121253.142381.772.232018121352.582473.872.132018121438.362328.471.652018121547.412395.861.982018103439.672413.801.64
[0287]
(3)结论
[0288]
经与对照品比对,可以得出1号峰为槐胺碱,2号峰为甲基氧化偶氮樱草糖苷,3号峰为苦参碱,4号峰为槐果碱,5号峰为槐定碱,6号峰为氧化槐果碱,7号峰为氧化苦参碱,8号峰为番石榴酸,9号峰为三叶豆紫檀苷。
[0289]
从结果中来看,10批样品与对照指纹相似度大于0.9,非共有峰面积占比小于5%。
[0290]
2.3重复性
[0291]
(1)实验步骤
[0292]
空白溶液配制:甲醇-0.2%磷酸二氢钾=15∶85,过滤即得。
[0293]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0294]
供试品溶液配制:精密量取同批号6份复方苦参注射液1ml,置50ml 量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0295]
进样顺序及要求见下表。
[0296]
进样顺序
[0297]
顺序样品针数1空白溶液1针2对照品溶液5针(连续测试)3供试品-1溶液1针4供试品-2溶液1针5供试品-3溶液1针6供试品-4溶液1针7供试品-5溶液1针8供试品-6溶液1针9对照品溶液1针
[0298]
(2)结果报告参见图4
[0299]
表2.3-1重复性共有峰模式相似度结果
[0300][0301][0302]
表2.3-2重复性共有峰相对保留时间结果
[0303][0304]
表2.3-3重复性共有峰峰面积结果
[0305][0306]
(3)结论
[0307]
从结果中来看,6份供试品中相似度大于0.99,各共有峰相对保留时间及峰面积rsd值小于3%,因此重复性良好。
[0308]
2.6精密度
[0309]
(1)实验步骤
[0310]
空白溶液配制:甲醇-0.2%磷酸二氢钾=15∶85,过滤即得。
[0311]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0312]
供试品溶液配制:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻
度,摇匀,滤过,取续滤液作为供试品溶液。
[0313]
进样顺序及要求见下表。
[0314]
进样顺序
[0315]
顺序样品针数1空白溶液1针2对照品溶液5针(连续测试)3供试品溶液6针4对照品溶液1针
[0316]
(2)结果报告参见图5及下表
[0317]
表2.4-1精密度共有峰模式相似度结果
[0318][0319][0320]
表2.4-2精密度共有峰相对保留时间结果
[0321][0322]
表2.4-3精密度共有峰峰面积结果
[0323][0324][0325]
(3)结论
[0326]
从结果中来看,供试品连续进样6针后相似度大于0.99,各共有峰相对保留时间及峰面积rsd值均小于3%,符合要求。
[0327]
2.7溶液稳定性
[0328]
(1)实验步骤
[0329]
空白溶液配制:甲醇-0.2%磷酸二氢钾=15∶85,过滤即得。
[0330]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0331]
供试品溶液配制:精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0332]
进样顺序及要求如下表。
[0333]
进样顺序
[0334]
顺序样品针数1空白溶液1针2对照品溶液5针(连续测试)3供试品-0h1针4供试品-1h1针5供试品-2h1针6供试品-4h1针7供试品-8h1针8供试品-16h1针9供试品-24h1针10对照品溶液1针
[0335]
(2)结果报告参见图6及下表
[0336]
表2.5-1稳定性共有峰模式相似度结果
[0337][0338]
表2.5-2稳定性共有峰相对保留时间结果
[0339][0340]
表2.5-3稳定性共有峰峰面积结果
[0341][0342]
(3)结论
[0343]
从结果中来看,供试品在24小时内相似度大于0.99,各共有峰的相对保留时间及峰面积rsd值均小于3%,因此供试品在24小时内稳定。
[0344]
2.8耐用性
[0345]
(1)实验步骤
[0346]
空白溶液配制:甲醇-0.2%磷酸二氢钾=15∶85,过滤即得。
[0347]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0348]
供试品溶液配制:分别精密量取复方苦参注射液1ml,置50ml量瓶中,加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0349]
分别取上述溶液1μl在不同条件下注入高效液相色谱仪,进样顺序及要求见下表(不同考察条件均按此进样顺序进样)。
[0350]
进样顺序
[0351][0352][0353]
(3)结果报告
[0354]
表2.8-1色谱条件变动的参数
[0355][0356]
(2)结果报告
[0357]
①
以批号20181138为供试品,考察供试品对色谱柱及仪器的耐用性,结果参见图7-1及下表。
[0358]
表2.8-2不同色谱柱共有峰模式相似度结果
[0359][0360][0361]
表2.8-3不同色谱柱共有峰相对保留时间结果
[0362][0363]
表2.8-4不同色谱柱共有峰峰面积结果
[0364][0365]
不同仪器耐用性结果参见图7-2及下表
[0366]
表2.8-5不同仪器共有峰模式相似度结果
[0367][0368]
表2.8-6不同仪器共有峰相对保留时间结果
[0369][0370]
表2.8-7不同仪器共有峰峰面积结果
[0371][0372]
②
以10批复方苦参注射液的色谱指纹图谱为基础,分别建立不同色谱柱及仪器的指纹图谱并生成对照指纹图谱,考察生成的对照指纹图谱相似度。参见图7-3~图7-11及下表。
[0373]
表2.8-8相似度结果(仪器1色谱柱2)
[0374][0375][0376]
表2.8-9相似度结果(仪器1色谱柱3)
[0377][0378]
表2.8-10相似度结果(仪器2色谱柱1)
[0379][0380][0381]
表2.8-11相似度结果(仪器3色谱柱1)
[0382][0383]
表2.8-12相似度结果(不同对照指纹图谱)
[0384][0385]
(3)结论
[0386]
从结果中来看,不同色谱柱考察结果中,各共有峰相似度大于0.99,相对保留时间rsd小于3%,峰面积小于5%;不同仪器考察结果中,各共有峰相似度大于0.99,相对保留时间及峰面积的rsd小于10%,说明仪器对该方法有影响,但在可接受范围内。
[0387]
10批样品在不同考察条件下,相似度均大于0.99,所生成的对照指纹图谱之间相似度大于0.99,因此从相似度的结果来看,该方法耐用性较好。
[0388]
2.9生产工艺关键点考察
[0389]
(1)实验步骤
[0390]
空白溶液配制:甲醇-0.2%磷酸二氢钾=15∶85,过滤即得。
[0391]
对照品溶液配制:参引2.1项下对照品溶液配制方法。
[0392]
供试品溶液配制:根据各关键点体积量,计算得取样量,其中关键点1 取1ml至25ml量瓶中,关键点2与6为取5ml至50ml量瓶中,关键点4 为取2ml至25ml量瓶中,关键点5为取1ml至100ml量瓶中,其余各关键点为取1ml至50ml量瓶中,所有样品均加空白溶液至刻度,摇匀,滤过,取续滤液作为供试品溶液。
[0393]
进样顺序及要求如下表。
[0394]
进样顺序
[0395]
[0396][0397]
(2)结果报告参见图8
[0398]
表2.9-1生产工艺共有峰模式相似度结果
[0399][0400][0401]
(3)结论
[0402]
从结果中来看,生产工艺关键点相似度在0.451-0.754之间,生产工艺关键点8-22
(水沉药液-灭菌后样品)彼此间相似度较高,大于0.9。
[0403]
实施例3-1~3-4uplc条件摸索
[0404]
实施例3-1(供试品制备考察)
[0405]
实验步骤:
[0406]
3-1.1空白溶液配制:磷酸调节磷酸二氢钾溶液的ph值至3.0,0.34%磷酸二氢钾溶液-甲醇=85∶15的混合溶液,过滤即得。
[0407]
3-1.2对照品溶液制备:分别精密量取苦参碱、氧化苦参碱、氧化槐果碱、槐果碱、槐定碱、甲基氧化偶氮甲醇樱草糖苷对照品适量,加空白溶液制成溶液分别为0.2mg/ml、0.4mg/ml、0.2mg/ml、0.05mg/ml、0.05mg/ml、 0.05mg/ml的对照品溶液。
[0408]
3-1.3供试品溶液制备:取复方苦参注射液样品,精密量取0.5ml,置 25ml量瓶中,加空白溶液稀释至刻度,摇匀,滤过,作为供试品溶液1。取复方苦参注射液样品,精密量取1ml,置50ml量瓶中,加空白溶液稀释至刻度,摇匀,滤过,作为供试品溶液2。
[0409]
3-1.4色谱条件
[0410]
色谱柱:色谱柱:acquity uplc csh
tm c
18 1.7μm,2.1mm
×
100mm;检测波长:211nm,柱温:30℃,流速:0.3ml/min;流动相a:甲醇,流动相b:0.2%磷酸二氢钾(磷酸调ph值至3.0)梯度洗脱。
[0411]
3-1.5按上述色谱条件,分别将供试品1进样0.5μl,供试品2进样1μl。
[0412]
3-1.6实验结果:参见图9。
[0413]
综上,采用供试品溶液2制备方法(1ml样品加空白溶液稀释至50ml) 制备供试品。
[0414]
实施例3-2(流动相考察)
[0415]
实验步骤:
[0416]
3-2.1空白溶液配制:参见实施例3-1空白溶液配制。
[0417]
3-2.2对照品溶液配制:分别精密量取槐胺碱、番石榴酸、n-甲基金雀花碱、三叶豆紫檀苷对照品适量,加空白溶液分别制成0.05mg/ml、0.1mg/ml、 0.05mg/ml、0.1mg/ml对照品溶液,其余同实施例3-1对照品溶液配制。
[0418]
3-2.3供试品溶液配制:取复方苦参注射液样品,精密量取1ml,置50ml 量瓶中,加空白溶液稀释至刻度,摇匀,滤过,作为供试品溶液。
[0419]
3-2.4色谱条件考察:
[0420]
色谱条件1:
[0421]
色谱柱:acquity uplc csh
tm c
18 1.7μm,2.1mm
×
100mm
[0422]
检测波长:211nm,柱温:30℃,流速:0.4ml/min,进样量:1μl
[0423]
流动相a:0.01m甲酸铵水溶液 b:乙腈:0.01m甲酸铵水溶液(9:1) 洗脱条件:
[0424][0425]
实验结果:参见图10-1。
[0426]
色谱条件2:
[0427]
色谱柱:acquity uplc csh
tm c
18 1.7μm,2.1mm
×
100mm
[0428]
检测波长:211nm,柱温:30℃,流速:0.3ml/min,进样量:1μl
[0429]
流动相a:乙腈 b:0.34%磷酸二氢钾(磷酸调ph至3.0)
[0430][0431]
实验结果:参见图10-2。
[0432]
色谱条件3:
[0433]
流动相调整如下,其余同色谱条件2。
[0434]
流动相a:甲醇 b:10mmol碳酸氢铵(ph9.0)
[0435][0436]
实验结果:参见图10-3
[0437]
色谱条件4:
[0438]
流动相调整如下,其余同条件2。
[0439]
流动相a:甲醇 b:0.34%磷酸二氢钾(磷酸调ph至3.0)
[0440][0441][0442]
实验结果:参见图10-4
[0443]
色谱条件5:
[0444]
流动相调整如下,其余同条件2。
[0445]
流动相a:甲醇 b:0.2%磷酸二氢钾(磷酸调ph至3.0)
[0446]
[0447]
实验结果:参见图10-5,各个对照品按上述条件进样后与供试品的叠加图参见10-6。
[0448]
综上,甲醇-0.2%磷酸二氢钾作为流动相条件最佳。
[0449]
实施例3-3(流动相梯度考察):
[0450]
实验步骤:
[0451]
3-3.1空白溶液配制:参见实施例3-1空白溶液配制。
[0452]
3-3.2供试品溶液配制:参见实施例3-2供试品溶液配制。
[0453]
3-3.3梯度条件考察:
[0454]
色谱柱:acquity uplc csh
tm c
18 1.7μm,2.1mm
×
100mm
[0455]
流速:0.3ml/min,柱温:30℃,检测波长:211nm,进样量:1μl
[0456]
流动相a:甲醇 b:0.2%磷酸二氢钾(磷酸调ph至3.0)
[0457]
梯度洗脱程序分别为:
[0458]
方法1:
[0459][0460]
实验结果:参见图11-1
[0461]
方法2:
[0462][0463]
实验结果:参见图11-2
[0464]
方法3:
[0465][0466]
实验结果:参见图11-3
[0467]
方法4:
[0468][0469]
实验结果:参见图11-4
[0470]
方法5:
[0471][0472]
实验结果:参见图11-5
[0473]
方法6:
[0474][0475]
实验结果:参见图11-6
[0476]
综上,方法5的洗脱程序条件最佳。
[0477]
实施例3-4(色谱柱、柱温及流速考察)
[0478]
实验步骤:
[0479]
3-4.1空白溶液配制:参见实施例3-1空白溶液配制。
[0480]
3-4.2供试品溶液配制:参见实施例3-1供试品溶液1配制。
[0481]
3-4.3条件考察:
[0482]
考察条件1:
[0483]
色谱柱:agilent poroshell 120ec-c
18 4μm,4.6mm
×
100mm
[0484]
流速:0.3ml/min 柱温:30℃ 检测波长:211nm 进样量:1μl
[0485]
流动相a:甲醇 b:0.34%磷酸二氢钾(磷酸调ph至3.0)
[0486][0487]
实验结果:参见图12-1
[0488]
考察条件2:
[0489]
色谱柱:acquity uplc csh
tm c
18 1.7μm,2.1mm
×
100mm;检测波长:211nm,进样量:1μl,流速:0.3ml/min,柱温:35℃
[0490]
洗脱程序参见实施例3-3,梯度条件同实施例3-3中考察方法5。
[0491]
实验结果:参见图12-2
[0492]
考察条件3:
[0493]
进样量:0.5ul,其余同考察条件2,梯度洗脱程序调整如下:
[0494][0495]
实验结果:参见图12-3
[0496]
考察条件4:
[0497]
进样量:0.5μl,流速:0.3ml/min、0.28ml/min,其余同考察条件2,洗脱程序调整如下:
[0498][0499]
实验结果:参见图12-4
[0500]
考察条件5:
[0501]
进样量:0.5μl,流速0.28ml/min,其余同考察条件2,洗脱程序调整如下:
[0502][0503][0504]
实验结果:参见图12-5
[0505]
考察条件6:
[0506]
柱温:30℃,进样量:0.5μl,流速0.28ml/min,其余同考察条件2,洗脱程序调整如下:
[0507][0508]
实验结果:参见图12-6
[0509]
考察条件7:
[0510]
柱温:30℃,进样量:0.5μl,流速0.25ml/min,其余同考察条件2,洗脱程序调整如下:
[0511][0512]
实验结果:参见图12-7
[0513]
综上,最佳色谱柱为acquity uplc csh
tm c
18 1.7μm, 2.1mm
×
100mm,最佳流速为0.3ml/min,最佳柱温为30℃。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。