1.本发明涉及有机合成领域,具体地指一种纤维素负载金属氧化物催化材料及其应用于制备手性硼化物的方法。
背景技术:
2.手性硼烷是很多有机分子的中间体。过渡金属催化α,β-不饱和化合物的不对称共轭加成是有效构建新的碳立体中心的关键方法,然而构建立体碳-硼键的现有方法很苛刻,例如需要大量配体和无水无氧操作。因此如何高效构建手性硼化物成为了研究的重点。α,β-不饱和酯硼加成后的产物是药物开发的通用构建模块。与多电子的烯烃或炔烃相比,对α,β-不饱和酯的研究较少,产生的碳-硼键可以很容易通过1,2-迁移和suzuki-miyaura交叉偶联转化为碳-氧键、碳-氮键和碳-碳键。过渡金属中铜催化α,β-不饱和受体的对映选择性硼加成反应有催化剂廉价易得,配体用量少,产物对映选择性好等优点,成为了研究的热点。
3.但迄今为止,铜催化α,β-不饱和底物的α-取代的反应仍然面临着严峻的挑战,例如用现有的催化方法催化三取代烯烃底物的反应性不高,非立体特异性质子化使其对映选择性控制复杂化,缺乏温和的中性条件来避免或减少差向异构化和副产物的形成。因此,此类反应的成功案例非常少见。到目前为止,关于α,β不饱和底物的不对称催化β-硼化的工作主要集中在碱性条件下铜催化剂的使用上。2014年,文献(org.lett.2014,16,1426-1429)报道了cu催化β-取代的α-脱氢氨基酸衍生物的不对称共轭硼氢化反应,以氯化亚铜为铜源,(s,sp)-ip-foxap为配体,叔丁醇钠为碱,甲醇为质子源,分子筛为添加剂,四氢呋喃为溶剂,常温下实现了多种α-脱氢氨基酸衍生物的不对称共轭硼氢化反应。但该反应在氩气氛围下进行,实验操作复杂,条件苛刻,同时配体的用量巨大,成本昂贵,还伴随着大量碱的使用,造成环境污染,不适合工业生产。为了实现高对映选择性和温和中性的条件,发展一种简便易操作、条件温和、成本低廉,以高产率对α,β-不饱和酯进行不对称硼化反应的绿色环保的新方法是迫切需要的。
技术实现要素:
4.本发明的目的是解决上述背景技术的不足,提供一种纤维素负载异质结催化材料及其制备方法、应用于制备手性硼化物的方法,克服现有技术中存在的如下不足:反应需要无水无氧操作和大量手性配体,成本高,无法工业化;反应时需要进行碱的添加,催化剂无法回收利用。
5.本发明以纤维素负载异质结催化材料(cell@cuti)催化α,β-不饱和酯的不对称硼加成反应,利用纤维素结构中含有大量游离的羟基,可与金属离子鳌合,对铜的络合作用更强。tio2将铜充分分散,具有更大的比表面积,催化活性更高。能在纯水中实现催化反应,无需添加任何碱,同时能多次回收利用,符合绿色化学的理念,非常适合工业化应用。
6.本发明的技术方案为:一种纤维素负载异质结催化材料的制备方法,其特征在于,
包括以下步骤:
7.a.将钛酸丁酯的乙醇溶液加入ph值3~4的醋酸乙醇溶液中,50~60℃下搅拌0.5~1h得到白色凝胶,将白色凝胶烘干、研磨、600℃煅烧后得到tio2粉末;
8.b.将cu(oac)2加入naoh溶液中,再依次加入tio2粉末和抗坏血酸进行充分搅拌,过滤得到产物后洗涤烘干,得到cu2o/tio2混合粉末,其中cu(oac)2、tio2、抗坏血酸和naoh物质的量比=1:(0.5~2):(1~2):(2~3);
9.c.将cu2o/tio2混合粉末置于甲醇溶液中,搅拌形成cu2o/tio2悬浮液,加入纤维素在室温下搅拌12~24h,分离产物并洗涤烘干得到纤维素负载异质结催化材料cell@cuti。
10.优选的,步骤a中钛酸丁酯的乙醇溶液由钛酸丁酯、无水乙醇按体积比1:(3~4)混合得到;
11.ph值3~4的醋酸乙醇溶液由冰醋酸、蒸馏水、无水乙醇按体积比1:(5~7):(15~20)混合后滴加盐酸调节ph值得到;
12.所述钛酸丁酯与冰醋酸的体积比(5~6):1。
13.优选的,步骤a中白色凝胶在80~100℃下烘干24~36h、研磨、600℃下煅烧2~4h得到tio2粉末。
14.优选的,步骤c中cu2o/tio2混合粉末所含cu2o和纤维素的物质的量之比为1:(15~18)。
15.本发明提供一种纤维素负载异质结催化材料,由以上任一所述的纤维素负载异质结催化材料的制备方法制备得到。
16.本发明还提供上述纤维素负载异质结催化材料在α,β-不饱和酯硼化反应中的应用,包括以下步骤:
17.1)将α,β-不饱和酯i、联硼酸频那醇酯、纤维素负载异质结催化材料cell@cuti和配体(r,s)-josiphos四种物质加入到甲苯中预溶解,再加入水在室温下搅拌3~6h反应,其中α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti所含铜、配体(r,s)-josiphos的摩尔比为1:(1.2~2):(0.01~0.02):(0.01~0.03),化学反应方程式如下:
[0018][0019]
其中,r为苯基,对氯苯基、2-苯基乙基、邻甲基苯基或噻吩基;
[0020]
2)反应结束后,反应液进行过滤后,滤液分离提纯得到手性硼加成产物ii;沉淀物洗涤干燥离心后,回收纤维素负载异质结催化材料cell@cuti循环使用。
[0021]
配体(r,s)-josiphos名称为(r)-(-)-1[(s)-2-(二苯基膦)二茂铁]乙基二环己基膦,为市售产品(购自安耐吉公司),其结构式如下:
[0022][0023]
其中,ph指苯基,cy指环己烷。
[0024]
α,β-不饱和酯i合成步骤参照文献合成(catalytic asymmetric boration of acyclicα,β-unsaturated esters and nitriles angew.chem.2008,120,151-153.),反应式如下,产物用核磁共振仪(nmr)对其结构进行表征。
[0025][0026]
优选的,步骤1)中α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti所含铜、配体(r,s)-josiphos四种物质的摩尔比为1:1.2:0.01:0.01。
[0027]
优选的,步骤1)催化材料cell@cuti所含铜:水:甲苯用量之比为0.002mmol:(1.8~2)ml:(0.1~0.2)ml。
[0028]
优选的,步骤1)中室温下混合搅拌反应3h。
[0029]
优选的,步骤2)中所得滤液分离提纯得到手性硼加成产物ii具体步骤包括:反应液用乙酸乙酯萃取,得到含有产物的有机相,再经过无水na2so4干燥,过滤,旋蒸去除多余有机溶剂,所得粗产品经薄层层析方法分离,得到纯净的手性硼加成产物ii。本发明将硼加成产物ii通过氧化进一步转化为相应的羟基化合物ⅲ,用于测定对映选择性,通过比较羟基化合物ⅲ的旋光度与文献中的旋光度来确定立体化学构型,为本领域常见操作,反应式如下:
[0030][0031]
本发明中联硼酸频哪醇酯[b2(pin)2]与cell@cuti催化材料中的活性中心铜生成铜硼中间体,与α,β-不饱和酯发生硼加成反应生成烯醇铜中间体,中间体在质子源水的作用下快速质子化,生成硼加成产物。该反应中水提供质子源作用,使烯醇铜中间体发生质子化过程生成目标产物,并实现催化材料的再生。在反应过程中水既是质子源也是溶剂。
[0032]
本发明的有益效果为:
[0033]
1.纤维素载体具有良好的生物相容性,绿色环保,固载金属铜效果好,同时具有较长的使用寿命,纤维素负载异质结催化材料在反应完成后可方便地借助固液分离方法与反应体系中其它组分分离,经过简单的再生便可重复使用,因此可大大降低生产成本,同时也可以明显减少各种环境污染问题。
[0034]
2.本发明仅需要使用较低的催化剂用量和较低的配体用量,即可获得较高的转化率和对映选择性。大大降低了反应成本,更适合工业生产。
[0035]
3.本发明反应条件温和,以纯水为溶剂,甲苯为添加剂,无需添加任何碱,在室温
下即可进行反应,且反应时间短,简便易操作,反应条件更加绿色,减少了对环境的污染。
[0036]
4.本发明应用性广,可用于各种不同类型的α,β-不饱和酯的不对称硼加成,从而获得相应的手性产物。
附图说明
[0037]
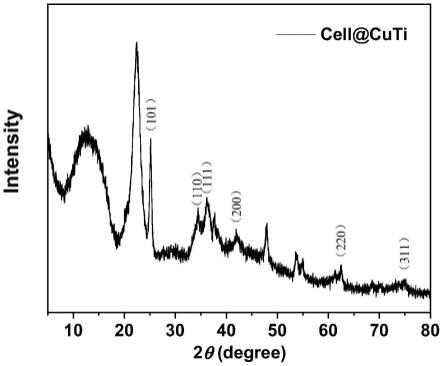
图1为纤维素负载异质结催化材料(cell@cuti)的x射线衍射图谱;
[0038]
图2为实施例2中目标产物的核磁氢谱图;
[0039]
图3为实施例2中目标产物的核磁碳谱图;
[0040]
图4为对比例1中目标产物的消旋体的高效液相图;
[0041]
图5为实施例2中目标产物的高效液相图。
具体实施方式
[0042]
下面具体实施例对本发明作进一步的详细说明。实施例中所用的药品未经特别说明均为市售产品,所用方法未经特别说明均为本领域常规方法。
[0043]
实施例1
[0044]
本实施例提供一种纤维素负载金属氧化物催化材料的制备方法,包括以下步骤:
[0045]
a.tio2的制备:
[0046]
配置溶液1:将20ml的钛酸四丁酯和70ml的无水乙醇加入到烧杯中,搅拌20min,形成黄色澄清溶液;
[0047]
配置溶液2:将4ml冰醋酸、20ml蒸馏水和70ml的无水乙醇加入烧杯,搅拌20min,并滴加1mol/l hcl,控制ph值在3~4之间,得到溶液2;
[0048]
将溶液1加到溶液2中,在50℃下水浴搅拌1h得到白色凝胶,将白色凝胶置于80℃下烘箱干燥24h得到黄色晶体,研磨得到黄色粉末,将黄色粉末在600℃下煅烧2h,得到tio2粉体;
[0049]
b.cu2o/tio2的制备
[0050]
取0.0802g naoh加入到20ml蒸馏水中搅拌溶解得到naoh溶液;将1mmol cu(oac)2加入naoh溶液,搅拌混合;再加入1.5mmol步骤1)制备得到的tio2加入并搅拌15-30min;继续加入1mmol抗坏血酸,搅拌15min;反应结束后,离心分离产物,洗涤,最后将产物置于80℃的干燥箱中干燥15h,得到cu2o/tio2混合粉末,通过icp检测出cu2o和tio2的物质的量之比为1:1.5;
[0051]
c.纤维素负载cu2o/tio2的制备
[0052]
将步骤b所得cu2o/tio2混合粉末、30ml甲醇加入100ml圆底烧瓶中,搅拌均匀形成cu2o/tio2悬浮液,加入纤维素室温下搅拌12h。将反应混合体系抽滤、洗涤,最后将残余物收集放置于80℃干燥箱中干燥,制得纤维素负载cu2o/tio2催化材料,简记为cell@cuti。其中,cu2o/tio2混合粉末中所含cu2o和纤维素的物质的量之比为1:18,纤维素大量过量目的是使纤维素能充分负载催化活性成分。
[0053]
步骤c所得纤维素负载异质结催化材料(cell@cuti)经过电感耦合等离子体光谱仪icp测试得到,铜含量为0.2mmol/g。
[0054]
步骤c所得纤维素负载异质结催化材料(cell@cuti)的x射线衍射图谱见图1。图中
23
°
的高峰是纤维素的特征峰。30
°
,36
°
,43
°
,61
°
,74
°
的(110),(111),(200),(220),(311)是cu2o的特征峰,证明催化活性成分是一价铜。25
°
的(101)晶面可以证明是锐钛矿型tio2,通过xrd分析可得纤维素成功负载cu2o/tio2。
[0055]
实施例2
[0056]
本实施例提供催化材料cell@cuti在α,β-不饱和酯i与联硼酸频那醇酯试剂的硼加成反应中的应用,包括以下步骤:
[0057]
1)将α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti(实施例1制备)和配体(r,s)-josiphos四种物质加入到0.2ml甲苯中预溶解,再加入1.8ml水在室温下搅拌3h,发生α,β-不饱和酯的不对称硼化反应,其中α,β-不饱和酯i 0.20mmol、联硼酸频那醇酯0.24mmol、催化材料cell@cuti(10.0mg)所含铜0.002mmol、配体(r,s)-josiphos 0.002mmol,本实施例α,β-不饱和酯i为2-烯-3-噻吩丙酸乙酯,其中r为噻吩基,反应式如下:
[0058][0059]
2)反应结束后,反应液经过滤操作,所得沉淀物用水和乙醇反复交替洗涤、干燥、离心,回收催化材料cell@cuti循环使用;滤液用乙酸乙酯萃取(3
×
10ml),得到含有产物的有机相,再经过无水na2so4干燥,过滤,旋蒸去除多余有机溶剂,所得粗产物用柱层析纯化得到手性硼加成产物ii(r为噻吩基)。
[0060]
随后通过氧化进一步转化为相应的手性羟基化合物ⅲ,用于测定对映体过量。通过比较手性羟基化合物ⅲ的旋光度与文献中的旋光度来确定立体化学。向步骤2)所得手性硼加成产物ii加入四水合硼酸钠244mg和5ml四氢呋喃水的混合溶剂,其中四氢呋喃和水的体积比为3:2。反应4h后,过滤整个反应体系以乙酸乙酯(3
×
10ml)萃取,分离出有机相后,用无水na2so4干燥,过滤,旋转蒸发除去溶剂。残余物用石油醚/乙酸乙酯混合溶剂=5:1(v/v)柱层析纯化得到手性羟基化合物ⅲ,产物收率为90%(36.04mg),ee(对映体过量百分数)值达到98%。反应式如下:
[0061][0062]
硼加成产物氧化后产物ⅲ的核磁氢谱和碳谱如下所示,图谱如图2和图3。
[0063]1h nmr(400mhz,chloroform-d)δ=6.97(d,j=5.0hz,2h),5.38(dd,j=7.8,4.8hz,1h),4.19(q,j=7.2hz,2h),3.50(s,1h),3.01-2.64(m,2h),1.27(t,j=7.2hz,3h).
[0064]
13
c nmr(100mhz,chloroform-d)δ=172.06,146.20,126.74,124.92,123.66,66.57,61.07,43.08,14.18.
[0065]
hplc(dialcel chiralcel as-h,nhexane/iproh=99/1,flow rate 0.3ml/min);tr=31.8min(s,major),tr=33.4min(r,minor).
[0066]
[α]
28d
=
–
47.6
°
(c=0.28,chcl3).
[0067]
目标产物(手性羟基化合物ⅲ)的高效液相数据如下,图谱如图5所示:
[0068]
图4为目标产物的消旋体的hplc图谱,可以确定该物质出峰位置31.2min和32.7min,
[0069]
图5为目标产物的hplc图谱,通过积分的31.87min处峰面积和33.46min处峰面积比为90:10,所以ee(对映体过量)值为80%。
[0070]
实施例2表明,在催化材料cell@cuti的催化条件下,2-烯-3-噻吩丙酸乙酯的转化率很高,其硼加成产物的收率达到了90%,ee值达到98%。
[0071]
本实施例催化材料cell@cuti循环连续使用6次后,第7次应用于本实施例的硼加成反应,产物的收率为79%,ee值为75%。
[0072]
对比例1
[0073]
本对比例提供α,β-不饱和酯i与联硼酸频那醇酯试剂发生硼加成反应得到消旋体的步骤:
[0074]
1)将α,β-不饱和酯i、联硼酸频那醇酯、无水硫酸铜、4-甲基吡啶四种物质加入2ml水在室温下搅拌3h,发生α,β-不饱和酯的硼化反应,其中α,β-不饱和酯i 0.20mmol、联硼酸频那醇酯0.24mmol、无水硫酸铜0.002mmol、4-甲基吡啶0.01mmol,本对比例α,β-不饱和酯i为2-烯-3-噻吩丙酸乙酯,其中r为噻吩基,反应式如下:
[0075][0076]
2)反应结束后,反应液用乙酸乙酯萃取(3
×
10ml),得到含有产物的有机相,再经过无水na2so4干燥,过滤,旋蒸去除多余有机溶剂,所得粗产物用柱层析纯化得到无手性硼加成产物ii’(r为噻吩基)。
[0077]
随后通过氧化进一步转化为相应的无手性羟基化合物
ⅲ’
,用于测定对映体过量。向步骤2)所得硼加成产物ii加入四水合硼酸钠244mg和5ml四氢呋喃水的混合溶剂,其中四氢呋喃和水的体积比为3:2。反应4h后,过滤整个反应体系以乙酸乙酯(3
×
10ml)萃取,分离出有机相后,用无水na2so4干燥,过滤,旋转蒸发除去溶剂。残余物用石油醚/乙酸乙酯混合溶剂=5:1(v/v)柱层析纯化得到无手性的羟基化合物ⅲ,产物收率为95%(38.04mg),反应式如下:
[0078][0079]
本对比例得到的无手性羟基化合物
ⅲ’
应用于实施例2中羟基化合物ⅲee值的测
定,hplc图谱如图4所示,实施例3-6中可按本对比例同样的方法制备无手性羟基化合物
ⅲ’
(区别仅为α,β-不饱和酯i中的选用r不同)。
[0080]
实施例3
[0081]
本实施例提供催化材料cell@cuti在α,β-不饱和酯i与联硼酸频那醇酯试剂的硼加成反应中的应用,包括以下步骤:
[0082]
1)将α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti(实施例1制备)和配体(r,s)-josiphos四种物质加入到0.2ml甲苯中预溶解,再加入1.8ml水在室温下搅拌3h,发生α,β-不饱和酯的不对称硼化反应,其中α,β-不饱和酯i 0.20mmol、联硼酸频那醇酯0.24mmol、催化材料cell@cuti(10.0mg)所含铜0.002mmol、配体(r,s)-josiphos 0.002mmol,本实施例α,β-不饱和酯i为2-烯-3-对氯苯基丙酸乙酯,其中r为对氯苯基,反应式如下:
[0083][0084]
2)反应结束后,反应液经过滤操作,所得沉淀物用水和乙醇反复交替洗涤、干燥,回收催化材料cell@cuti循环使用;滤液用乙酸乙酯萃取(3
×
10ml),得到含有产物的有机相,再经过无水na2so4干燥,过滤,旋蒸去除多余有机溶剂,所得粗产物用柱层析纯化得到手性硼加成产物ii(r为对氯甲苯基);
[0085]
随后通过氧化进一步转化为相应的羟基化合物ⅲ,用于测定对映体过量。通过比较羟基化合物ⅲ的旋光度与文献中的旋光度来确定立体化学。在步骤2)所得硼加成产物ii加入四水合硼酸钠244mg和5ml四氢呋喃水的混合溶剂,其中四氢呋喃和水的体积比为3:2。反应4h后,过滤整个反应体系,以乙酸乙酯(3
×
10ml)萃取,分离出有机相后,用无水na2so4干燥,过滤,旋转蒸发除去溶剂。残余物用石油醚/乙酸乙酯混合溶剂=5:1(v/v)柱层析纯化得到手性羟基化合物ⅲ,产物收率为84%(38.41mg),ee值达到79%.
[0086]
反应式如下:
[0087][0088]
硼加成产物氧化后产物ⅲ的核磁氢谱和碳谱如下所示。
[0089]1h nmr(400mhz,chloroform-d)δ=7.32(s,4h),5.10(dd,j=7.9,4.9hz,1h),4.18(q,j=7.1hz,2h),3.45(s,1h),2.93-2.56(m,2h),1.26(t,j=7.1hz,3h).
[0090]
13
c nmr(100mhz,chloroform-d)δ=172.36,140.93,133.46,128.70,127.09,69.62,61.07,43.16,14.18.
[0091]
hplc(dialcel chiralcel ad-h,nhexane/iproh=97/3,flow rate 0.5ml/min);tr=44.2min(s,major),tr=46.5min(r,minor)。
[0092]
[α]
28d
=
–
45.8
°
(c=0.25,chcl3).
[0093]
实施例3表明,在催化材料cell@cuti的催化条件下,2-烯-3-对氯苯基丙酸乙酯的转化率很高,其硼加成产物的收率达到了84%,ee值达到79%。
[0094]
实施例4
[0095]
本实施例提供催化材料cell@cuti在α,β-不饱和酯i与联硼酸频那醇酯试剂的硼加成反应中的应用,包括以下步骤:
[0096]
1)将α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti(实施例1制备)和配体(r,s)-josiphos加入到0.2ml甲苯中预溶解,再加入1.8ml水在室温下搅拌3h,发生α,β-不饱和酯的不对称硼化反应,其中α,β-不饱和酯i 0.20mmol、联硼酸频那醇酯0.24mmol、催化材料cell@cuti(10.0mg)所含铜0.002mmol、配体(r,s)-josiphos 0.002mmol,本实施例α,β-不饱和酯i为2-烯-3-邻甲基苯基丙酸乙酯,其中r为邻甲基苯基,反应式如下:
[0097][0098]
2)反应结束后,反应液经过滤操作,所得沉淀物用水和乙醇反复交替洗涤、干燥,回收催化材料cell@cuti循环使用;滤液用乙酸乙酯萃取(3
×
10ml),得到含有产物的有机相,再经过无水na2so4干燥,过滤,旋蒸去除多余有机溶剂,所得粗产物用柱层析纯化得到手性硼加成产物ii(r为邻甲基苯基);
[0099]
随后通过氧化进一步转化为相应的羟基化合物ⅲ,用于测定对映体过量。通过比较羟基化合物ⅲ的旋光度与文献中的旋光度来确定立体化学。在步骤2)所得硼加成产物ii加入四水合硼酸钠244mg和5ml四氢呋喃水的混合溶剂,其中四氢呋喃和水的体积比为3:2。反应4h后,过滤整个反应体系,以乙酸乙酯(3
×
10ml)萃取,分离出有机相后,用无水na2so4干燥,过滤,旋转蒸发除去溶剂。残余物用石油醚/乙酸乙酯混合溶剂=5:1(v/v)柱层析纯化得到手性羟基化合物ⅲ,产物收率为75%(31.23mg),ee值达到78%。
[0100]
反应式如下:
[0101][0102]
硼加成产物氧化后产物ⅲ的核磁氢谱和碳谱如下所示。
[0103]1h nmr(400mhz,chloroform-d)δ=7.51(dd,j=7.6,1.5hz,1h),7.25-7.12(m,3h),5.35(dd,j=8.8,3.9hz,1h),4.39-4.05(m,2h),2.84-2.53(m,2h),2.35(s,3h),1.29(t,j=7.1hz,3h).
[0104]
13
c nmr(100mhz,chloroform-d)δ=172.77,140.39,134.29,130.47,127.62,126.45,125.23,66.93,61.02,42.07,19.09,14.22.
[0105]
hplc(dialcel chiralcel ad-h,nhexane/iproh=97/3,flow rate 0.5ml/min);tr=34.05min(s,major),tr=38.67min(r,minor)。
[0106]
[α]
28d
=
–
44.5
°
(c=0.90,chcl3).
[0107]
实施例4表明,在催化材料cell@cuti的催化条件下,2-烯-3-邻甲基苯基丙酸乙酯的转化率很高,硼加成产物的收率达到了75%,ee值达到78%。
[0108]
实施例5
[0109]
本实施例提供催化材料cell@cuti在α,β-不饱和酯i与联硼酸频那醇酯试剂的硼加成反应中的应用,包括以下步骤:
[0110]
1)将α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti(实施例1制备)和配体(r,s)-josiphos四种物质加入到0.2ml甲苯中预溶解,再加入1.8ml水在室温下搅拌3h,发生α,β-不饱和酯的不对称硼化反应,其中α,β-不饱和酯i 0.20mmol、联硼酸频那醇酯0.24mmol、催化材料cell@cuti(10.0mg)所含铜0.002mmol、配体(r,s)-josiphos 0.002mmol,本实施例α,β-不饱和酯i为2-烯-3-(2-苯基乙基)丙酸乙酯,其中r为2-苯基乙基,反应式如下:
[0111][0112]
2)反应结束后,反应液经过滤操作,所得沉淀物用水和乙醇反复交替洗涤、干燥,回收催化材料cell@cuti-1循环使用;滤液用乙酸乙酯萃取(3
×
10ml),得到含有产物的有机相,再经过无水na2so4干燥,过滤,旋蒸去除多余有机溶剂,所得粗产物用柱层析纯化得到硼加成产物ii(r为2-苯基乙基);
[0113]
随后通过氧化进一步转化为相应的羟基化合物ⅲ,用于测定对映体过量。通过比较羟基化合物ⅲ的旋光度与文献中的旋光度来确定立体化学。在步骤2)所得硼加成产物ii加入四水合硼酸钠244mg和5ml四氢呋喃水的混合溶剂,其中四氢呋喃和水的体积比为3:2。反应4h后,过滤整个反应体系,以乙酸乙酯(3
×
10ml)萃取,分离出有机相后,用无水na2so4干燥,过滤,旋转蒸发除去溶剂。残余物用石油醚/乙酸乙酯混合溶剂=5:1(v/v)柱层析纯化得到手性羟基化合物ⅲ,产物收率为74%(32.8mg),ee值达到77%。
[0114]
反应式如下:
[0115][0116]
硼加成产物氧化后产物ⅲ的核磁氢谱和碳谱如下所示。
[0117]1h nmr(400mhz,chloroform-d)δ=7.32-7.26(m,2h),7.21(dt,j=8.1,2.0hz,3h),4.17(q,j=7.1hz,2h),4.02(tt,j=8.7,3.8hz,1h),3.05(s,1h),2.83(ddd,j=14.7,9.7,5.4hz,1h),2.70(ddd,j=13.8,9.5,6.9hz,1h),2.58-2.37(m,2h),1.93-1.79(m,1h),1.73(dddd,j=13.8,9.7,6.9,4.2hz,1h),1.27(t,j=7.1hz,3h).
[0118]
13
c nmr(100mhz,chloroform-d)δ=173.14,141.77,128.51,128.45,125.93,67.18,60.82,41.26,38.13,31.80,14.22.
[0119]
hplc(dialcel chiralcel od-h,nhexane/iproh=95/5,flow rate 0.5ml/min);tr=24.6min(s,major),t=28.4min(r,minor)。
[0120]
[α]
28d
=
–
48.0
°
(c=0.90,chcl3).
[0121]
实施例5表明,在催化材料cell@cuti的催化条件下,2-烯-3-(2-苯基乙基)丙酸乙酯的转化率很高,硼加成产物的收率达到了74%,ee值达到77%。
[0122]
实施例6
[0123]
本实施例提供催化材料cell@cuti在α,β-不饱和酯i与联硼酸频那醇酯试剂的硼加成反应中的应用,包括以下步骤:
[0124]
1)将α,β-不饱和酯i、联硼酸频那醇酯、催化材料cell@cuti(实施例1制备)和配体(r,s)-josiphos四种物质加入到0.2ml甲苯中预溶解,再加入1.8ml水在室温下搅拌3h,发生α,β-不饱和酯的不对称硼化反应,其中α,β-不饱和酯i 0.20mmol、联硼酸频那醇酯0.24mmol、催化材料cell@cuti(10.0mg)所含铜0.002mmol、配体(r,s)-josiphos 0.002mmol,本实施例α,β-不饱和酯i为2-烯-3-苯基丙酸乙酯,其中r为苯基,反应式如下:
[0125][0126]
2)反应结束后,反应液经过滤操作,所得沉淀物用水和乙醇反复交替洗涤、干燥,回收催化材料cell@cuti循环使用;滤液用乙酸乙酯萃取(3
×
10ml),得到含有产物的有机相,再经过无水na2so4干燥,再次过滤,旋蒸去除多余有机溶剂,所得粗产物用柱层析纯化得到手性硼加成产物ii(r为苯基);
[0127]
随后通过氧化进一步转化为相应的羟基化合物ⅲ,用于测定对映体过量。通过比较羟基化合物ⅲ的旋光度与文献中的旋光度来确定立体化学。在步骤2)所得硼加成产物ii加入四水合硼酸钠244mg和5ml四氢呋喃水的混合溶剂,其中四氢呋喃和水的体积比为3:2。反应4h后,过滤整个反应体系,以乙酸乙酯(3
×
10ml)萃取,分离出有机相后,用无水na2so4干燥,过滤,旋转蒸发除去溶剂。残余物用石油醚/乙酸乙酯混合溶剂=5:1(v/v)柱层析纯化得到手性羟基化合物ⅲ,产物收率为79%(30.68mg),ee值达到76%。
[0128]
反应式如下:
[0129][0130]
硼加成产物氧化后产物ii的核磁氢谱和碳谱如下所示。
[0131]1h nmr(400mhz,chloroform-d)δ=7.44-7.26(m,5h),5.14(dd,j=8.8,4.0hz,1h),4.18(q,j=7.1hz,2h),2.95-2.51(m,2h),1.27(t,j=7.1hz,3h).
[0132]
13
c nmr(100mhz,chloroform-d)δ=172.53,142.46,128.58,127.84,125.69,70.32,60.96,43.32,14.19.
[0133]
hplc(dialcel chiralcel od-h,nhexane/iproh=90/10,flow rate 0.5ml/min);
tr=14.4min(s,major),tr=18.1min(r,minor)。
[0134]
[α]
28d
=
–
48.9
°
(c=0.84,chcl3).
[0135]
实施例6表明,在催化材料cell@cuti的催化条件下,2-烯-3-苯基丙酸乙酯的转化率很高,硼加成产物的收率达到了79%,ee值达到76%。
[0136]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。