1.涉及一种用于增强干性的组合物及其用途。
背景技术:
2.目前,为了用作细胞治疗药物,正在进行针对各种细胞的研究和研发,所述细胞根据分化部位,正使用全能性干细胞(胚胎干细胞、诱导性多能干细胞等)、多能干细胞或成体干细胞(骨髓/脂肪干细胞、脐带血/脐带干细胞、胎儿干细胞等)以及体细胞等。众所周知,其中,由于人胚胎干细胞从能够发育成人类生命体的胚胎制成,因此存在很多伦理问题,全能性干细胞则因其分化控制技术尚未完整,因此研发成细胞治疗药物还需要很长时间。另外,虽然利用体细胞的细胞治疗药物研发获得了诸多成果,但由于体细胞固有的低增殖性以及确保原料的困难,因而难以投入实际应用。因此,作为上述问题的解决方案,针对成体干细胞的研究受到关注。
3.在成体干细胞中,间充质干细胞的增殖能力比体细胞优异,并且是能够分化成骨、软骨、脂肪等的多能性干细胞,由于其在遗传上比胚胎干细胞等多能干细胞更稳定,因此研发为用于治疗软骨再生、心肌梗塞以及移植物抗宿主病等的细胞治疗药物。虽然间充质干细胞比体细胞显示出更优异的自我更新能力,但是与在体内时不同,在体外培养条件下需要具备能够维持细胞增殖性的最佳条件,并且存在要提供接近体内条件的营养、ph、温度、渗透压等环境条件。特别地,在体外培养时活性氧和氧化应激诱发老化,因而存在自体增殖和多能性损失的问题。对此,韩国注册专利第1980562号公开了用于提高干性成分的草酸盐。但是,尽管做出了这些努力,但实际上依然需要一种能够制备在体外培养时干性也得以维持和增强的干细胞的技术。
4.另一方面,已知唾液酸寡糖(sialyloligosaccharides)是人乳包括的典型的hmo成分,其作为构成大脑的核心成分对幼儿大脑功能的发育起着重要作用,并且具有用于改善肠道功能的益生元作用。但是,关于将唾液酸寡糖用于培养干细胞或增强干性的技术却一无所知。
5.在此背景下,本发明人为研发能够增强干细胞干性的技术而付出了诸多努力,最终证实唾液酸寡糖和干细胞干性之间明显的相关性后,完成了本技术。
技术实现要素:
技术问题
6.一方面提供一种用于增强干细胞干性的组合物,其包括唾液酸寡糖。
7.另一方面提供一种培养干细胞的方法,其包括在包括唾液酸寡糖的培养基中培养干细胞。
8.另一方面提供一种增强干细胞干性的方法,其包括在干细胞中添加唾液酸寡糖。
9.另一方面提供一种干性增强的干细胞,其通过所述培养干细胞的方法来获得。
10.另一方面提供一种用于治疗细胞的组合物,其包括作为活性成分的所述干性增强
的干细胞及其稀释液。
11.另一方面提供一种用于培养肝脏类器官的组合物,其包括唾液酸寡糖。
12.通过所附的权利要求和附图以及以下详细描述,本技术的其它目的和优点将变得进一步明确。对于本技术所属领域或相似技术领域的工作人员来说,本说明书未描述的内容是能够充分认知和推测的,因此省略对其的描述。技术方案
13.本发明人为通过维持干性并抑制干细胞的老化来使适合用作细胞治疗药物的干细胞的特性最大化而付出了诸多努力,最终证实在干细胞中处理唾液酸寡糖能够抑制干细胞老化、增加干细胞因子表达、增强干细胞增殖能力,从而干性得到明显增强,不仅如此,证实通过在肝脏类器官中处理唾液酸寡糖能够增加增殖和/或成熟度后,基于此完成了本发明。
[0014][0015]
一方面提供一种用于增强干细胞干性的组合物,所述干细胞包括唾液酸寡糖(sialyloligosaccharides)。
[0016]
本说明书中的术语“干细胞(stem cell)”是指,作为尚未分化的未分化细胞,具有全能性/多能性(pluri-potency或multi-potency)的多能细胞,即,能够通过自我复制(self-renewability)无限增殖,并受细胞所处环境影响而在根据需要给出适当的信号时,可以分化成各种细胞。
[0017]
所述干细胞可以是自体或同种异体干细胞,也可来源于包括人类和非人类哺乳类的任一类型的动物,所述干细胞可来源于成体或胚胎,但不限于此。
[0018]
所述干细胞包括诱导性多能干细胞、胚胎干细胞以及成体干细胞,具体地,可以是成体干细胞。所述成体干细胞可以是间充质干细胞、人类组织间充质基质细胞(mesenchymal stromal cell)、人类组织间充质干细胞、多能干细胞或羊膜上皮细胞,但不限于此。所述成体干细胞可以是来源于脐带、脐带血、滑膜、骨髓、脂肪、肌肉、神经、皮肤、羊膜和胎盘等的干细胞,但也不限于此。根据一具体实施方式,所述干细胞可以是人类骨髓来源间充质干细胞。
[0019]
本说明书中的术语“诱导性多能干细胞(ipsc:induced pluripotent stem cells)”是指通过人为的脱分化过程,从分化的细胞中诱导成具有多能性分化能力的细胞,也称为“脱分化干细胞”。所述人为的脱分化过程可以通过使用病毒性介导(其利用逆转录病毒和慢病毒)或非病毒性载体,导入非病毒性介导(其利用蛋白质和细胞提取物)的脱分化因子来进行,或者包括借助于干细胞提取物、化合物等的脱分化过程。诱导性多能干细胞具有与胚胎干细胞几乎相同的特性,具体地,表现出相似的细胞形状且基因和蛋白表达相似,在体外(in vitro)和体内(in vivo)具有全能性并形成畸胎瘤(teratoma),当插入到小鼠的囊胚(blastocyst)时形成嵌合体(chimera)小鼠,并可以进行基因的生殖系传递(germline transmission)。所述诱导性多能干细胞可以包括人、猴、猪、马、牛、羊、狗、猫、小鼠、兔等所有来源的诱导性多能干细胞。
[0020]
本说明书中的术语“胚胎干细胞(embryonic stem cell)”是从受精卵在母体子宫着床前的囊胚期胚胎中提取内细胞团(inner cell mass)后在体外进行培养,是指具有自我更新能力(self-renewal)的细胞,即,具有能够分化为个体所有组织细胞的多能性
(pluripotency)或全能性(totipotent)的细胞,广义上可以包括胚胎干细胞来源的胚状体(embryoid bodies)。所述胚胎干细胞可以包括人、猴、猪、马、牛、羊、狗、猫、小鼠、兔等所有来源的胚胎干细胞。
[0021]
本说明书中的术语“成体干细胞(adult stem cell)”是指,在发育过程进行后胚胎形成各器官的阶段或成体阶段出现的干细胞。成体干细胞的分化能力通常仅限为构成特定组织的细胞,在成年之后这种成体干细胞大部分留在器官中发挥补充正常或或病理学上发生的细胞损失的作用。这可以意味着通过将存在于组织中的干细胞分离出后在体外进行培养,从而使其具有多能性(multipotency)的细胞。所述成体干细胞可以包括人、猴、猪、马、牛、羊、狗、猫、小鼠、兔等所有来源的成体干细胞。
[0022]
本说明书中的术语“间充质干细胞”为从人或哺乳类的组织中分离出的未分化的干细胞,其可以来源于各种组织。特别地,其可以是脐带间充质干细胞、脐带血间充质干细胞、骨髓间充质干细胞、脂肪间充质干细胞、肌肉间充质干细胞、神经间充质干细胞、皮肤间充质干细胞细胞,羊膜间充质干细胞以及胎盘间充质干细胞,从各组织分离干细胞的技术已公开于所属领域。
[0023]
本说明书中的术语“唾液酸寡糖(sialyloligosaccharides)”指代,包括至少一个唾液酸部分的寡糖,所述寡糖(oligosaccharides)为葡萄糖(glucose)、果糖(fructose)以及半乳糖(galactose))等结合2个至8个糖的糖类,是水溶性的结晶物质。所述唾液酸寡糖可以包括,例如,3'-唾液酸乳糖(3'-sialyllactose)、6'-唾液酸乳糖(6'-sialyllactose)、3'-唾液酸乳糖胺(3'-sialyllactosamine)、6'-唾液酸乳糖胺(6'-sialyllactosamine)、3'-唾液酸-3-岩藻糖基乳糖(3'-sialyl-3-fucosyllactose)、唾液酸乳-n-四糖(sialyllacto-n-tetraose)、二唾液酸乳糖(disialyllactose)或它们的组合,例如,所述唾液酸寡糖可以是获得美国食品药品监督管理局(fda)批准的安全物质3'-唾液酸乳糖,但不限于此。
[0024]
另外,所述组合物可以另外包括人乳包括的寡糖,即,hmo(human milk oligosaccharide)。所述人乳来源寡糖可以包括,例如,乳-n-四糖(lacto-n-tetraose)、2'-岩藻糖基乳糖(2'-fucosyllactose)、3-岩藻糖基乳糖(3-fucosyllactose)、乳-n-新四糖(lacto-n-neotetraose)、ls-四糖b(ls-tetrasaccharide b)、ls-四糖c(ls-tetrasaccharide c)、二唾液酸乳-n-四糖(disialyllacto-n-tetraose)或它们的组合,但不限于此。
[0025]
所述唾液酸寡糖已知是抗菌和抗病毒作用优异的免疫活性物质,但关于干细胞的培养,具体地,关于干性维持和增强,其功能和活性完全未知。根据一具体实施方式,证实唾液酸寡糖,例如,唾液酸乳糖与干细胞的干性密切相关。具体地,证实唾液酸乳糖被处理的间充质干细胞增加sox2、oct4、nanog等干细胞性因子的表达并抑制细胞老化,提高细胞增殖能力。因此,唾液酸寡糖可用作维持或增强干细胞干性的活性物质。
[0026]
所述唾液酸寡糖可以根据所需细胞的类型以适当的浓度来包括,只要符合增强干细胞干性的目的。所述唾液酸寡糖可以以下比例来包括,例如,0.1μm至400μm,例如,0.1μm至350μm,例如,0.1μm至200μm,例如,0.1μm至150μm,例如,1μm至400μm,例如,1μm至350μm,例如,1μm至300μm,例如,1μm至250μm,例如,1μm至200μm,例如,1μm至150μm,例如,10μm至250μm,例如,30μm至250μm,例如,50μm至250μm,例如,50μm至200μm,例如,50μm至150μm。当
所述唾液酸寡糖的浓度超过或低于所述浓度范围时,可能引起体内副作用或者无法发挥干性维持或增强效果。
[0027]
本说明书中的术语“干性(stemness)”是指,对能够生成胚胎干细胞等所有细胞的能力,即,多能性,以及能够无限创造出与自身相似细胞的自我更新能力(self-renewal)的统称,是所属领域的通用术语。即,干性可以是指维持干细胞特性的能力。
[0028]
本说明书中的术语“增强干性”可以包括以下特征的表现,抑制干细胞的细胞老化,或提高干细胞的细胞增殖能力,或提高干细胞的功能性或增加干细胞的端粒酶活性,或增加干细胞性因子的表达,或维持未分化细胞的未分化状态的同时使其增殖,或提高干细胞中的蛋白质稳态,或增加细胞移动活性。
[0029]
所述术语“干细胞性因子”已知是在干细胞中较多表达,对干维持细胞的全能型,即,干细胞特性发挥重要作用的基因,例如,有sox2、oct4、nanog、klf4、c-myc、oct3/4、ssea-1、ssea-3、ssea-4、tra1-60、tra1-81、lin28、fbx15等,但不限于此。因此,当观察到所述干细胞性因子中的至少一个表达时,可认为是未分化干细胞,并且能够认为其表达的越多,干细胞的全能性就越高。
[0030]
所述术语“提高功能性”是指功能性的成熟,已知在干细胞表达并且对维持干细胞成熟的功能特性发挥重要作用的基因,例如,有cyp3a4、cyp3a7、alb、afp、ttr、ck19等,但不限于此。因此,在观察到提高所述干细胞功能的因子中至少一个的表达时,可认为能够提高干细胞的功能性,并且可认为其表达的越多,干细胞功能性的提高能力就越高。
[0031]
所述术语“增殖(proliferation)”是指细胞数量的增加,能够以与生长(growth)相同的含义来使用。特别地,所述术语“未分化增殖(undifferentiated proliferation)”是指,干细胞未分化成特定细胞并具有与原细胞相同的性质,即,增殖为具有多能性(有可能与术语“全能性”混用)的细胞。所述组合物能够以包括唾液酸寡糖的培养基组合物的形式来提供,以增强干细胞的干性。所述唾液酸寡糖可添加至用于培养干细胞的常规培养基来使用,以实现本说明书公开的关于增强干性的效果。根据一具体实施方式,证实将唾液酸寡糖添加至干细胞培养基时,抑制干细胞老化、提高细胞增殖能力以及干性显著增强。
[0032]
所述培养基组合物可以另外包括选自由硒、抗坏血酸、维生素e、儿茶酚、番茄红素、β-胡萝卜素、辅酶q-10(coq-10)、白藜芦醇(resveratrol)、t-bhq、奥替普拉(oltipraz)、桤木萃取物、epa(eicosapentaenoic acid、dha(docosahexaenoic acid)以及它们的组合所组成的组中的抗氧化剂。从所述唾液酸寡糖和所述含有抗氧化剂的培养基组合物中培养的干细胞,在形态或活性不变的情况下显示出优异的细胞增殖能力。
[0033]
包括在所述培养基组合物的唾液酸寡糖,或者选自由唾液酸寡糖、硒、抗坏血酸、维生素e、儿茶酚、番茄红素、β-胡萝卜素、辅酶q-10(coq-10)、白藜芦醇、t-bhq、奥替普拉、桤木萃取物、epa、dha以及它们的组合所组成的组中的抗氧化剂,可以与所属领域已知适用于干细胞培养的具有简单组成的常规培养基(basal medium)一同被含有。通常用于培养的基本培养基可以是选自由dmem(dulbecco's modified eagle's medium)、80%knockout dmem、mem(minimal essential medium)、bme(basal medium eagle)、rpmi 1640、f-10、f-12、dmem-f12、α-mem(α-minimal essential medium)、g-mem(glasgow's minimal essential medium)、imdm(iscove's modified dulbecco's medium)、maccoy's 5a培养基、amniomax medium以及chang's medium mesemcult-xf medium所组成的组中的基本培
medium)、mem(minimal essential medium)、bme(basal medium eagle)、rpmi1640、f-10、f-12、αmem(αminimal essential medium)、gmem(glasgow's minimal essential medium)、iscove's modified dulbecco's medium等,但不限于此。另外,所述培养基可以包括青霉素(penicillin)、链霉素(streptomycin)、庆大霉素(gentamycin)等抗生素。
[0042]
所述培养基可以有效浓度包括唾液酸寡糖。所述术语“有效浓度”是指足以增强干细胞干性的唾液酸寡糖的量,当低于或等于有效浓度时无法显现出活性,而当大于或等于有效浓度时可能显现出毒性,因此可以在有效浓度范围内使用唾液酸寡糖。所述唾液酸寡糖可以以下比例来包括,例如,0.1μm至400μm,例如,0.1μm至350μm,例如,0.1μm至300μm,例如,0.1μm至250μm,例如,0.1μm至200μm,例如,0.1μm至150μm,例如,1μm至400μm,例如,1μm至350μm,例如,1μm至300μm,例如,1μm至250μm,例如,1μm至400μm,例如,1μm至350μm,例如,1μm至300μm,例如,1μm至250μm,例如,1μm至200μm,例如,1μm至150μm,例如,10μm至250μm,例如,30μm至250μm,例如,50μm至250μm,例如,50μm至200μm,例如,50μm至150μm。当低于或等于所述浓度范围时,可能不显现出干细胞的维持或增强效果。
[0043]
另外,所述培养基可以另外包括人乳来源寡糖。所述人乳来源寡糖可以包括,例如,乳-n-四糖、2'-岩藻糖基乳糖、3-岩藻糖基乳糖、乳-n-新四糖、ls-四糖b、ls-四糖c、二唾液酸乳-n-四糖或它们的组合,但不限于此。
[0044]
所述方法可以包括传代培养干细胞。所述方法可以使干细胞维持未分化状态,具体地,可以使干细胞在传代培养期间或之后维持未分化状态。所述方法可以在例如,3至10或更多传代培养后维持干性。
[0045]
本说明书中的术语“传代培养”是指,为了以健康状态长期连续培养细胞,定期将部分细胞转移到新的培养容器后,更换培养基的同时持续传代培养细胞的方法。所述术语“传代(passage)”是指,最初的种子培养物在培养容器中生长至细胞在同一培养容器汇合(confluence)时,生长为多能性干细胞。在空间有限的培养容器中,随着细胞数量的增加,经过一定时间后增殖养分被消耗或污染物积累导致细胞的自然死亡,因此其用作增加健康细胞数量的方法,通常将更换一次培养基(培养容器)或分为细胞群后进行培养称为1代(1passage)。传代培养方法可以不受限制地使用所属领域已知的方法,但优选地可以通过机械分离或酶分离来进行。
[0046]
干细胞在进行重复培养或者受到更多外部刺激时,存在细胞的形态或大小会细微地发生变化,并且细胞的再生能力和活性(telomerase activity)降低的问题,即细胞老化。根据培养的培养基,细胞的再生能力和活性等特征存在差异,因此重要的是在一种即使进行重复培养,形态等细胞特性也无太大变化且再生能力或活性未下降的培养基中培养干细胞。即,重要的是在延迟或改善细胞老化,或者维持初始细胞状态的培养基组合物中培养干细胞。但是,根据现有的培养基中培养干细胞的方法,需要进行多次传代培养以获得较高收率的干细胞,因而需要花费大量的人力和时间,尤其是传代培养所需的部分培养基组分价格昂贵,因此在经济效益方面也不具有优势。另外,存在反复的传代培养使细胞的再生能力下降的问题。所述培养基组合物可提供一种细胞形态或活性不发生变化且能够提高细胞再生能力的培养基组合物。因此,提供将唾液酸寡糖作为活性成分而包括的培养基组合物,以维持和增强干性。
[0047]
所述维持干细胞的未分化状态可通过alp(alkaline phosphatase)、oct-4、sox2、
htert(human telomerase reverse transcriptase)、tdgf(teratocarcinoma-derived growth factor)或ssea-4等基因表达增加来进行确认,但不必然限于此。
[0048]
根据一具体实施方式,以传代培养后未处理唾液酸乳糖的间充质干细胞为例,确认到由于细胞老化因子p16和p53的表达增加而进行老化,但以处理唾液酸乳糖的间充质干细胞为例,确认到p16和p53的表达显著减少,从而抑制细胞老化。
[0049]
另外,根据一具体实施方式,以传代培养后未处理唾液酸乳糖的间充质干细胞为例,确认到由于细胞老化的标志物sa-β-gal的活性增加而进行老化,但以处理唾液酸乳糖的间充质干细胞为例,确认到sa-β-gal的活性显著减少,从而抑制细胞老化。
[0050]
所述培养干细胞的方法所提及的术语或要素中,与所述增强干性的组合物的描述所提及的术语或要素相同的,应理解为与所述组合物的描述所提及的术语或要素相同。
[0051]
另一方面提供一种增强干细胞干性的方法,其包括在干细胞中添加唾液酸寡糖。
[0052]
在所述增强干细胞干性的方法中,“唾液酸寡糖”和“干细胞”如上所述。
[0053]
所述在干细胞中添加唾液酸寡糖,可以在离体(ex vivo)或试管中(in vitro)进行。另外,所述在干细胞中添加唾液酸寡糖可以是指,将唾液酸寡糖添加至在培养基中培养的干细胞。
[0054]
所述在干细胞中添加唾液酸寡糖可以在普通血清培养基中进行,或者将在血清培养基中传代培养的干细胞转移至无血清培养基后进行。在无血清培养基中的培养可以在去除血清培养基中的培养液,并用磷酸盐缓冲溶液洗涤细胞后进行。
[0055]
所述方法可以另外包括添加人乳来源寡糖。所述添加人乳来源寡糖可以与所述添加唾液酸寡糖同时、另外或依次进行,所述人乳来源寡糖可以包括,例如,乳-n-四糖、2'-岩藻糖基乳糖、3-岩藻糖基乳糖、乳-n-新四糖、ls-四糖b、ls-四糖c、二唾液酸乳-n-四糖或它们的组合,但不限于此。
[0056]
所述术语“无血清培养基”是指,未含有血清的培养液和培养基,以培养动物组织或细胞例如,无血清培养基可以是dmem(dulbecco's modified eagle's medium)、edm(endothelial differentiation medium)、mem(minimal essential medium)、bme(basal medium eagle)、rpmi 1640、f-10、f-12、a-mem(a-minimal essential medium)、g-mem(glasgow'sminimal essential medium)或iscove's modified dulbecco's medium等。
[0057]
所述术语“血清”是指血液完全凝固后从血液游离的透明上清液。另外,培养动物细胞必须在合成培养基中添加血清,这时使用牛或马、人的血清,通常使用的是牛的血清。根据采血时间,可与胎牛血清(fetal bovine serum:fbs)、新生牛血清(newborn bovine serum)、小牛血清(calf serum)、牛血清(bovine serum)等进行区分。例如,可以是胎牛血清(fetal bovine serum,fbs)或小牛血清(bovine calf serum,bcs)等。
[0058]
根据所述增强干细胞干性的方法,通过唾液酸寡糖的处理,干细胞在试管中(in vitro)和体内(in vivo)的老化得到抑制,细胞增殖能力显著提高,即,由于干性显著增强,因此能够提供具有适合用作细胞治疗药物的干细胞特性的干细胞。
[0059]
所述增强干细胞干性的方法所提及的术语或要素中,与所述增强干性的组合物或培养干细胞的方法描述所提及的术语或要素相同的,应理解为与所述组合物或培养方法的描述所提及的术语或要素相同。
[0060]
另一方面提供一种干性增强的干细胞,其通过所述增强干性的方法来获得。
[0061]
另一方面提供一种细胞治疗药物组合物,其包括所述干性增强的干细胞或其稀释液。
[0062]
通过在干细胞中处理所述唾液酸寡糖,可以增强干细胞的干性。因此,通过包括处理唾液酸寡糖的增强干性的方法来获得的干细胞,其干性显著增强,因此可作为细胞治疗药物的活性成分而包括在其中,例如,将干细胞激活为适合移植的状态,或将其特性修饰为适合人体等。
[0063]
本说明书中的术语“细胞治疗药物”是通过从人类分离、培养以及特殊制造来制造,针对细胞和组织的用于治疗、诊断以及预防目的的药品,其指代为了修复细胞或组织的功能,通过在体外增殖、筛选存活的自体(autologous)、同种异体(allogenic)或异种(xenogenic)细胞或者利用其它方法来改变细胞的生物特性等一系列活动,用于治疗、诊断以及预防目的的药品。根据细胞分化程度,细胞治疗药物可大致分为体细胞治疗药物和干细胞治疗药物。根据一具体实施方式,所述细胞治疗药物组合物可以是将唾液酸寡糖被处理的干细胞作为活性成分而包括的干细胞治疗药物。
[0064]
本说明书中的术语“干细胞治疗药物”是一种在体外工程化细胞后重新将其注入体内,以达到治疗、诊断以及预防疾病目的的细胞治疗药物,与针对非特定人群的旨在缓和疾病症状的现有药物不同,其指代向患者注入经工程化和培养的干细胞,从而从根本上治疗疾病的针对性生物药品。所述干细胞治疗药物,根据细胞来源可分为胚胎早期发育阶段制成的胚胎干细胞治疗药物,在成人的各种组织有限存在的成体干细胞治疗药物,脱分化普通体细胞从而诱导成初始未分化状态的脱分化干细胞治疗药物,或胚胎干细胞、成体干细胞、脱分化干细胞来源的基于类器官的细胞治疗药物等;根据治疗方法可分为移植患者自身干细胞的自体干细胞治疗药物,移植他人干细胞的同种异体来源的细胞治疗药物,利用动物干细胞的异种干细胞治疗药物等。所述干细胞治疗药物在向患者直接注入细胞后,可修复损伤的细胞或组织,因此不会在体内引起毒性且再生和维持人体原有的功能,从而可以提供手术或药物疗法无法做到的根本性治疗方法。所述干细胞治疗药物通过针对受损组织和细胞的再生和修复(regeneration and rejuvenation)、置换(replacement)、修复(repair)3r策略,可用于治疗脑梗塞、心肌梗塞、退行性关节炎以及骨折等各种细胞损伤性疾病。
[0065]
所述干性增强的干细胞可以优选地呈细胞组合物的形式,其包括至少一种稀释剂,所述稀释剂保护和维持细胞并且在对所需的组织进行注射、输入、移植时便于使用。所述稀释剂可列举生理盐水、pbs(phosphate buffered saline)、hbss(hank's balanced salt solution)等缓冲溶液,血浆或血液成分等。
[0066]
所述细胞治疗药物组合物可通过各种途径施用于包括人在内的哺乳动物。施用方式为常规使用的所有方式,例如,除形式与临床施用时的肌肉或静脉注射剂相同的肠胃外施用之外,还可以直接施用于患病部位,或通过口服、经皮、皮下、静脉或肌肉等途径施用。
[0067]
所述细胞治疗药物组合物的施用剂量可根据个体的年龄、体重、性别、施用形式、健康状况以及患病程度所不同,并且也可以根据医生或药师的判断,隔一定时间一天一次至数次分开施用。例如,以人为例,细胞治疗药物的常规施用量可以是104cells/body至10
10
cells/body,优选为106cells/body至108cells/body,可以一次施用或分数次施用。所述施用量仅为一般情况下的示例,施用量可根据个体差异更多或更少。
[0068]
所述细胞治疗药物组合物可以对神经系统疾病、肌肉系统疾病、骨病或上皮相关疾病表现出预防或治疗效果。所述神经系统疾病可以包括退行性神经系统疾病,例如,包括帕金森病、痴呆症、阿尔茨海默病、亨廷顿氏病、肌萎缩侧索硬化、中风、记忆力下降、重症肌无力、行性核上性麻痹、多系统萎缩、特发性震颤、皮质基底节变性、弥漫性路易体病以及皮克病在内的各种神经体统疾病。所述肌肉系统疾病可以包括肌肉萎缩、脑瘫、进行性骨化纤维发育不良、皮肌炎、筋膜室综合征、重症肌无力、卢伽雷氏病、线粒体肌病、横纹肌溶解症、多发性肌炎、纤维肌痛、肌强直、酒精性肝炎、非酒精性脂肪肝、肝炎,肝硬化以及肌筋膜疼痛综合征等。所述骨病可以包括骨质疏松症(osteoporosis)、骨软化症(osteomalacia)、骨质减少(osteopenia)、骨萎缩(bone atrophy)、骨关节炎(osteoarthritis)、股骨头缺血性坏死(avascular necrosis of the femoral head)或牙周病(perodontal disease)等。所述上皮相关疾病可以包括顽固性角膜疾病等。所述细胞治疗药物除所述疾病之外,适用于所有可通过移植干细胞来治疗的疾病。
[0069]
本说明书中的术语“治疗”是指抑制、缓和或有利地改变与疾病相关临床状况的所有活动。另外,治疗可以是指未接受治疗时比预期存活率提高的存活率。除治疗手段之外,治疗可以同时包括预防手段。
[0070]
所述细胞治疗药物组合物可通过另外包括药学上可接受的载体来配置。本说明书中的术语“药学上可接受的载体”是指,不明显刺激生物体且不阻碍施用成分的生物活性和特性的载体或稀释剂。针对可适用所述细胞治疗药物组合物的药物组合物,药学上可接受的载体可不受限制地使用所属领域已知的载体,例如,缓冲剂、防腐剂、舒缓剂、增溶剂、等渗剂、稳定剂、基质、赋形剂、润滑剂等。
[0071]
所述细胞治疗药物组合物可以通过常用的各种剂型技术来制备。只要可以诱导向患病部位移动,细胞治疗药物组合物可以通过任何途径施用。根据具体情况,也可考虑加载于载剂的方法,所述载剂具有使干细胞向病变移动的手段。因此,所述细胞治疗药物组合物可以通过包括局部(包括颊侧、舌下、皮肤以及眼内施用)、肠胃外(包括皮下、皮内、肌肉内、点滴、静脉内、动脉内、关节内以及脑脊髓液内)或经皮施用的各种途径来施用,优选地,可直接施用于发病部位。
[0072]
在一实施方案中,干细胞可通过微量悬浮于适当的稀释剂来施用于个体,使用该稀释剂可以是为了保护和维持细胞,并且在注入靶组织时便于使用。所述稀释剂可以列举生理盐水、磷酸盐缓冲液、hbss等的缓冲溶液以及脑脊髓液等。另外,细胞治疗药物组合物可以借助任意装置来施用,以使活性物质移动至靶细胞。优选施用方式和制剂可以是注射剂。注射剂可利用生理盐水、林格氏液、汉克溶液或灭菌水溶液等水性溶剂,橄榄油等植物油,油酸乙酯等高级脂肪酸酯,以及乙醇、苯甲醇、丙二醇、聚乙二醇或甘油等非水性溶剂来制备,为渗透黏膜可以使用所属领域已知的适用于要通过的屏障的非穿透剂,用于防止变质的稳定剂可以另外包括药物载体,例如,抗坏血酸、亚硫酸氢钠、bha、生育酚、edta等,以及乳化剂、ph调节缓冲剂、硝酸苯汞、硫柳汞、苯扎氯铵、苯酚、甲酚、苯甲醇等抑制微生物生长的防腐剂等。
[0073]
本说明书中的术语“施用”是指通过某种适当的方法向患者引入所述细胞治疗药物组合物,细胞治疗药物组合物可以通过能够到达靶组织的口服或肠胃外的各种途径施用。可以腹膜内施用、静脉内施用、肌肉内施用、皮下施用、皮内施用、口服施用、局部施用、
鼻内施用、肺内施用、直肠内施用,但不限于此。
[0074]
所述细胞治疗药物组合物可以药学上的有效量来施用。本说明书中的术语“有效量”是指,延迟或完全停止要治疗的特定疾病的发病或进展而所需的量。适当的1天总使用量可以在正确的医学判断范围之内由处置医生来决定。为了所述细胞治疗药物组合物的目的,优选地,对特定患者的具体治疗有效量根据要实现的反应类型和程度,包括是否根据具体情况使用不同制剂在内的具体组合物、患者的年龄、体重、一般健康状况、性别和饮食、施用时间、施用途径,以及组合物的分泌率、治疗时间、与具体组合物一同使用或同时使用的药物在内的各种因子,药学领域已知的类似因子而不同地施用。
[0075]
所述干细胞或包括干细胞的细胞治疗药物组合物所提及的术语或要素中,与所述增强干性的组合物或培养干细胞的方法描述所提及的术语或要素相同的,应理解为与所述组合物或培养方法的描述所提及的术语或要素相同。
[0076][0077]
另一方面提供一种用于培养肝脏类器官的组合物,其包括唾液酸寡糖。
[0078]
另一方面提供一种制备成熟的肝脏类器官的方法/提高肝脏类器官成熟度的方法,其包括将唾液酸寡糖添加至肝脏类器官。
[0079]
所述用于培养肝脏类器官的组合物,或者制备成熟的肝脏类器官的方法/提高肝脏类器官成熟度的方法中所提及的术语或要素中,与所述增强干性的组合物或培养干细胞的方法描述所提及的术语或要素相同的,应理解为与所述组合物或培养方法的描述所提及的术语或要素相同。
[0080]
根据一具体实施方式,以在制备的肝脏类器官培养过程中处理唾液酸寡糖为例,证实肝脏类器官的增殖显著增加,并且cyp3a4/cyp3a7比例和alb/afp比例提高,从而对肝脏类器官的成熟度产生影响。
[0081]
所述术语“类器官(organoid)”是指,将从干细胞或器官来源细胞中分离出的细胞通过3d培养法重新聚集、重组而成的细胞聚集体,可以包括由悬浮细胞培养物形成的类器官或细胞簇。所述类器官也可命名为小型器官、器官类似物或类似器官。所述类器官具体包括构成器官或组织的各种类型中的至少一种细胞类型,并且应能够再现组织或器官的形态和功能。
[0082]
所述术语“类器官培养”包括能够生成或维持类器官的所有活动。例如,可以是能够使从干细胞或特定组织分离的细胞分化为具有特定功能的组织或器官细胞,和/或使类器官存活、生长或增殖。
[0083]
能够使用所述组合物的类器官可以来源于诱导性多能干细胞、胚胎干细胞以及成体干细胞,优选地,所述类器官可以是来源于诱导性多能干细胞或成体干细胞的肝脏类器官。
[0084]
所述唾液酸寡糖可以适当的浓度来包括,只要其满足培养肝脏类器官或提高肝脏类器官成熟度的目的。所述唾液酸寡糖可以以下比例来包括,例如,0.1μm至400μm,例如,0.1μm至350μm,例如,0.1μm至300μm,例如,0.1μm至250μm,例如,0.1μm至200μm,例如,0.1μm至150μm,例如,1μm至400μm,例如,1μm至350μm,例如,1μm至300μm,例如,1μm至250μm,例如,1μm至400μm,例如,1μm至350μm,例如,1μm至300μm,例如,1μm至250μm,例如,1μm至200μm,例如,1μm至150μm,例如,10μm至250μm,例如,30μm至250μm,例如,50μm至250μm,例如,50μm至
200μm,例如,50μm至150μm。有益效果
[0085]
通过根据一方面的组合物或方法中,可以使干细胞性因子的表达显著增加,抑制干细胞的老化,并显著提高干细胞的细胞增殖能力或干细胞的细胞功能。
[0086]
通过根据一方面的组合物或方法,能够消除现有体外培养干细胞时存在的自体增殖能力和多能性损失的问题,通过利用干性增强的干细胞,可以提高细胞治疗药物的治疗效率。
[0087]
根据一方面的组合物和方法中的干细胞,其干性得到显著增强,从而作为细胞治疗药物的活性成分而包括在其中。
[0088]
根据一方面的细胞治疗药物组合物包括干性显著增强的干细胞,从而能够提高细胞治疗药物的效率。
附图说明
[0089]
图1为通过cck-8assay确认唾液酸乳糖处理浓度对骨髓间充质干细胞存活率影响的结果,图1的a是处理3'-唾液酸乳糖的结果,图1的b是处理6'-唾液酸乳糖的结果,图1的c是处理3'-唾液酸乳糖和6'-唾液酸乳糖混合物的结果。
[0090]
图2为通过cck-8assay确认唾液酸乳糖处理浓度对脂肪间充质干细胞存活率影响的结果,图2的a是处理3'-唾液酸乳糖的结果,图2的b是处理6'-唾液酸乳糖的结果,图2的c是处理3'-唾液酸乳糖和6'-唾液酸乳糖混合物的结果。
[0091]
图3为通过cck-8assay确认唾液酸乳糖处理浓度对脐带血间充质干细胞存活率影响的结果,图3的a是处理3'-唾液酸乳糖的结果,图3的b是处理6'-唾液酸乳糖的结果,图3的c是处理3'-唾液酸乳糖和6'-唾液酸乳糖混合物的结果。
[0092]
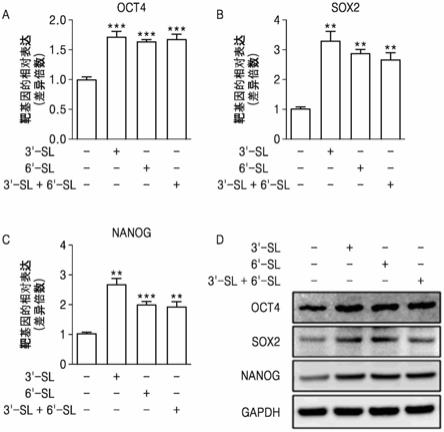
图4为唾液酸乳糖对骨髓间充质干细胞干性影响的确认结果,图4的a是oct4的mrna水平的确认结果,图4的b是sox2的mrna水平的确认结果,图4的c是nanog的mrna水平的确认结果,图4的d是oct4、sox2以及nanog的蛋白表达水平的确认结果。
[0093]
图5为唾液酸乳糖对脂肪间充质干细胞干性影响的确认结果,图5的a是oct4的mrna水平的确认结果,图5的b是sox2的mrna水平的确认结果,图5的c是nanog的mrna水平的确认结果,图5的d是oct4、sox2以及nanog的蛋白表达水平的确认结果。
[0094]
图6为唾液酸乳糖对脐带血间充质干细胞干性影响的确认结果,图6的a是oct4的mrna水平的确认结果,图6的b是sox2的mrna水平的确认结果,图6的c是nanog的mrna水平的确认结果,图6的d是oct4、sox2以及nanog的蛋白表达水平的确认结果。
[0095]
图7为3'-唾液酸乳糖对骨髓间充质干细胞老化影响的确认结果,图7的a是细胞老化因子p16和p53在mrna水平的表达变化的确认结果,图7的b是p16和p53在蛋白水平的表达变化的确认结果,图7的c是利用sa-β-gal分析细胞老化的结果。
[0096]
图8是唾液酸乳糖对骨髓间充质干细胞增殖影响的确认结果,是确认参与细胞周期进程和增殖的基因ccna2和cdk2表达变化的结果。
[0097]
图9是通过cck-8assay确认3'-唾液酸乳糖对骨髓来源干细胞传代存活率影响的结果。
[0098]
图10是唾液酸乳糖对诱导性多能干细胞来源肝脏类器官细胞存活率影响的确认
结果,是通过cck-8assay确认存活率的结果。
[0099]
图11是唾液酸乳糖对诱导性多能干细胞来源肝脏类器官细胞成熟度影响的确认结果,是比较cyp3a4和cyp3a7表达量比例的结果。
[0100]
图12是唾液酸乳糖对诱导性多能干细胞来源肝脏类器官细胞成熟度影响的确认结果,是比较cyp3a4和cyp3a7表达量比例的结果。
具体实施方式
[0101]
下面,通过实施例进一步详细描述本发明。但是,这些实施例仅用于示例性描述本发明,本发明的范围不限于此。
[0102][0103]
实施例1.干细胞培养
[0104]
本实施例的实验中使用了骨髓间充质干细胞(hbmscs)、脂肪组织间充质干细胞(hatmscs)、脐带血间充质(hcbmsc)以及诱导性多能干细胞来源的肝脏类器官。骨髓间充质干细胞、脂肪组织间充质干细胞、以及脐带血间充质干细胞的培养基使用了包括10%胎牛血清(fetal bovine serum,t&i,gangwon,korea)和1%抗生素(青霉素/链霉素gibco,grandisland,ny,usa)的dmem低葡萄糖培养基(dulbecco's modified eagle's medium,dmem low glucose,hyclone,logan,ut,usa)。另一方面,处理100μm的3'-唾液酸乳糖(3'-sialyllactose,genechem)、6'-唾液酸乳糖(6'-sialyllactose,genechem)以及3'-唾液酸乳糖和6'-唾液酸乳糖的混合物之后,每三天更换一次培养液。将三蒸水放入培养液后,针对对照组相同地进行实验。另外,肝脏类器官培养基使用了包括endothelial cell growth medium-2(lonza),2.5%fbs,100nm dexamethasone(sigma-aldrich)20ng/ml osm(r&d system),10ng/ml hgf(peprotech)的hepatocyte culture medium(lonza),每三天更换了一次培养液。
[0105][0106]
实施例2.确认根据处理唾液酸寡糖的干细胞的细胞存活率
[0107]
本实施例中欲确认唾液酸寡糖对干细胞细胞存活率的影响。具体地,在传代培养的干细胞中分别以0μm、50μm、100μm、200μm或400μm的浓度处理3'-唾液酸乳糖、6'-唾液酸乳糖以及它们的组合,然后通过cck-8检测(cell counting kit-8assay)确认了每个浓度的细胞存活率。具体地,人骨髓间充质干细胞、人脂肪组织间充质干细胞以及人脐带血间充质干细胞接种至96孔板。然后,以0μm、50μm、100μm、200μm或400μm的浓度,将3'-唾液酸乳糖(genechem)、6'-唾液酸乳糖(genechem)以及3'-唾液酸乳糖和6'-唾液酸乳糖的混合物,在不含胎牛血清(t&i)、包括1%抗生素(gibco)的dmem低葡萄糖培养基(hyclone)中处理后进行培养。然后,通过cck-8(dojindo laboratories,kumamoto,japan)检测确认了经培养的细胞的存活率。
[0108]
图1至图3是将3'-唾液酸乳糖、6'-唾液酸乳糖以及3'-唾液酸乳糖和6'-唾液酸乳糖的混合物按照浓度在骨髓间充质干细胞(图1)、脂肪组织间充质干细胞(图2)以及脐带血间充质干细胞(图3)进行处理后,确认每个干细胞对细胞存活率影响的结果。结果,虽然所有浓度都未对细胞存活率产生不利影响,但证实以100μm浓度处理唾液酸乳糖时的细胞存活率显著提高。因此,在之后的实验中都以100μm浓度处理唾液酸乳糖来进行了实验。
[0109][0110]
实施例3.确认根据处理唾液酸寡糖的干性增加
[0111]
本实施例中欲确认唾液酸寡糖对干细胞干性的影响。具体地,在间充质干细胞分别处理3'-唾液酸乳糖、6'-唾液酸乳糖以及它们的组合后,分别用实时荧光定量逆转录聚合酶链反应(qrt-pcr:quantitative reverse transcription-polymerase chain reaction)和蛋白质印迹法测量了所述间充质干细胞的干性标志物oct4、sox2以及nanog的mrna和蛋白水平的表达变化。具体地,通过所述实施例1的方法培养细胞,从收集的细胞中分离出总rna,然后利用购自bioneer(daejeon,korea)的oct4引物、sox2引物(bioneer,p200205)以及nanog引物,通过qrt-pcr确认分离的总rna的mrna表达变化。使用的oct4和nanog引物的序列示于下表1。
[0112]
【表1】引物名称引物序列(5'-》3')序列号oct4 forwardgcaagccctcatttcacca1oct4 reversegcccatcacctccaccac2nanog forwardtttgtgggcctgaagaaaact3nanog reverseagggctgtcctgaataagcag4
[0113]
图4至图6是唾液酸乳糖对干细胞干性影响的确认结果。结果,相比于在没有唾液酸乳糖的情况下培养的干细胞,证实处理3'-唾液酸乳糖、6'-唾液酸乳糖以及3'-唾液酸乳糖和6'-唾液酸乳糖混合物后培养的骨髓间充质干细胞(图4)、脂肪组织间充质干细胞(图5)以及脐带血间充质干细胞(图6),在能够确认干性的标记基因oct4、sox2以及nanog的mrna和蛋白质水平上的表达均显著增加。
[0114]
通过所述实验结果证实,在干细胞的培养前、培养时或培养后的过程中处理唾液酸寡糖能够显著增强干细胞干性。
[0115][0116]
实施例4.确认根据处理3'-sialyllactose的干细胞老化的减少
[0117]
本实施例中欲确认唾液酸寡糖对干细胞老化的影响。具体地,用3'-唾液酸乳糖处理骨髓间充质干细胞,分别通过qrt-pcr和蛋白质印迹法测量传代培养后细胞衰老因子p16和p53的mrna和蛋白水平的表达变化。具体地,通过所述实施例1的方法培养细胞,从收集的细胞中分离出总rna,然后利用bioneer(daejeon,korea)验证的p16引物(bioneer,p260189)和p53引物(bioneer,p250999),通过qrt-pcr确认分离的总rna的mrna表达变化。
[0118]
图7为3'-唾液酸乳糖对干细胞老化影响的确认结果。结果,未处理3'-唾液酸乳糖而传代培养的骨髓间充质干细胞,随着老化的进行p16和p53的mrna和蛋白水平的表达增加,但是处理3'-唾液酸乳糖后传代培养的干细胞在p16和p53的mrna和蛋白水平显示出非常低的表达,从而证实p16和p53的表达减少。
[0119]
另外,为确认处理3'-唾液酸乳糖(genechem)后干细胞的老化程度,对用100μm的3'-唾液酸乳糖处理的10代骨髓间充质干细胞(hbmscs)进行了老化相关的β-半乳糖苷酶染色。具体地,将细胞固定于福尔马林后用pbs洗涤,添加β-半乳糖苷酶染色溶液(β-gal staining solution,1mg/ml x-gal,40mm柠檬酸-磷酸钠缓冲液,150mm nacl,2mm mgcl2,5mm亚铁氰化钾,以及5mm亚铁氰化钾;ph 6.0;sigma-aldrich,st.louis,usa)后在37℃反
应。然后,利用eclipse ts100;nikon usa,melville,ny,usa,确认了老化的细胞(蓝色,阳性)和未显示老化活性细胞(阴性)的老化活性程度。
[0120]
利用sa-β-gal进行细胞老化分析结果显示,未处理3'-唾液酸乳糖而传代培养的骨髓间充质干细胞,随着老化进行sa-β-gal的活性增加,处理3'-唾液酸乳糖后传代培养的干细胞显示出低活性,从而证实sa-β-gal的活性减少。
[0121]
通过所述实验结果证实,在干细胞的培养前、培养时或培养后的过程中处理唾液酸寡糖能够显著减少干细胞的老化。
[0122][0123]
实施例5.确认根据处理3'-sialyllactose的干细胞增殖的提高
[0124]
本实施例中欲确认唾液酸寡糖对干细胞增殖的影响。具体地,在具有低增殖能力的骨髓间充质干细胞处理3'-唾液酸乳糖,确认了参与细胞周期进程和增殖的基因细胞周期蛋白a2(ccna2:cyclin a2)和周期蛋白依赖性激酶2(cdk2:cyclin-dependent kinase 2)的表达变化。具体地,通过所述实施例1的方法培养细胞,从收集的细胞中分离出总rna,然后利用bioneer(daejeon,korea)验证的ccna引物(bioneer,p212796)和cdk2引物(bioneer,p136765),通过qrt-pcr确认分离的总rna的mrna表达变化。
[0125]
图8为3'-唾液酸乳糖对骨髓间充质干细胞增殖影响的确认结果。结果,证实未处理3'-唾液酸乳糖的干细胞随着老化进行,ccna2和cdk2的表达减少,但是处理3'-唾液酸乳糖的干细胞,ccna2和cdk2的表达显著增加。
[0126]
通过所述实验结果证实,在干细胞的培养前、培养时或培养后的过程中处理唾液酸寡糖能够显著增加干细胞的增殖。
[0127][0128]
实施例6.确认根据处理3'-sialyllactose的每一代干细胞存活率提高
[0129]
本实施例中欲确认唾液酸寡糖对根据干细胞的细胞传代培养的存活率的影响。具体地,在4、7、10以及12传代培养的骨髓间充质干细胞中,以100μm的浓度处理3'-唾液酸乳糖,然后通过cck-8检测(cell counting kit-8assay)确认了细胞存活率。具体地,将人骨髓间充质干细胞接种至96孔板。然后,以100μm的浓度,将3'-唾液酸乳糖(genechem)在不含胎牛血清(t&i)、包括1%抗生素(gibco)的dmem低葡萄糖培养基(hyclone)中处理后进行培养。通过cck-8检测确认了培养细胞的存活率。
[0130]
图9是确认3'-唾液酸乳糖对根据传代数的干细胞存活率影响的结果。结果,证实处理3'-唾液酸乳糖后培养干细胞时的细胞存活率显著增加。
[0131]
通过所述实验结果证实,虽然自体增殖能力随着干细胞的连续传代培养下降,但是唾液酸寡糖的处理能够显著抑制随传代培养的增殖能力下降。
[0132][0133]
实施例7.确认根据处理sialyllactose的类器官存活率提高
[0134]
本实施例中欲确认唾液酸寡糖对诱导性多能干细胞来源肝脏类器官存活率的影响。具体地,传代培养肝脏类器官后在hepatic medium(hm)中稳定一天,以0μm、0.1μm、1μm、10μm以及100μm的浓度处理3'-唾液酸乳糖和6'-唾液酸乳糖六天,然后在经过六天后的第七天通过cck检测确认了细胞存活率。
[0135]
图10是唾液酸乳糖对诱导性多能干细胞来源肝脏类器官细胞存活率影响的确认
结果。结果,证实当以10μm、100μm的浓度处理3'-唾液酸乳糖,以0.1μm、1μm、10μm、100μm的浓度处理6'-唾液酸乳糖时,肝脏类器官内的细胞存活率显著增加。
[0136]
通过所述实验结果证实,在培养诱导性多能干细胞来源肝脏类器官的过程中,唾液酸寡糖的处理能够显著增加肝脏类器官的增殖。
[0137][0138]
实施例8.确认根据处理sialyllactose的类器官成熟度提高
[0139]
本实施例中欲确认唾液酸寡糖对诱导性多能干细胞来源肝脏类器官成熟度的影响。具体地,传代培养肝脏类器官后在hepatic medium(hm)中稳定一天,以0μm、0.1μm、1μm、10μm以及100μm的浓度处理3'-唾液酸乳糖和6'-唾液酸乳糖六天,然后在经过六天后的第七天从肝脏类器官中分离总rna,分别用实时荧光定量逆转录聚合酶链反应(qrt-pcr:quantitative reverse transcription-polymerase chain reaction)测量代谢成熟度标志物cyp3a4、cyp2a7、alb、afp的mrna水平的表达变化,然后通过比较其表达比例来确认代谢成熟度。
[0140]
图11和图12是唾液酸乳糖对诱导性多能干细胞来源肝脏类器官细胞成熟度影响的确认结果。结果,证实当以1μm、10μm的浓度处理3'-唾液酸乳糖时的cyp3a4/cyp3a7比例,以及当以10μm、100μm的浓度处理3'-唾液酸乳糖时的alb/afp比例显著增加,并且证实以0.1μm、100μm的浓度处理6'-唾液酸乳糖时的alb/afp比例显著增加。
[0141]
通过所述实验结果证实,在培养诱导性多能干细胞来源肝脏类器官的过程中,唾液酸寡糖的处理能够显著增加肝脏类器官的代谢成熟度。
[0142][0143]
上述对本发明的描述是为了示例性描述,本发明所属领域的技术人员能够理解,在不改变本发明的技术构思或必要特征的情况下,可以容易地改变为其它具体形式。因此,应理解上述实施例在所有方面都具有示例性,而非限制性。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
