1.本发明涉及复硝酚钠检测技术领域,具体地说是一种快速检测复硝酚钠的方法。
背景技术:
2.复硝酚钠(sodium nitrophenolate)是几种含硝基苯酚钠盐的复合型植物生长调节剂,包括对硝基酚钠、邻硝基酚钠和5-硝基邻甲氧基苯酚钠。复硝酚钠具有显著的增产效果,在农业上应用广泛。复硝酚钠还应用在畜牧上,在提高肉、蛋产量和质量的同时,还能增强动物的免疫力,预防多种疾病。但复硝酚钠的广泛使用,对环境生物的生长、发育和繁殖构成威胁,并且对人体健康具有有潜在危害。
3.2019年,中华人民共和国农业农村部公告第250号明确规定复硝酚钠为禁用兽药。2021年公布的《gb 2763-2021食品安全国家标准食品中农药最大残留限量》规定了复硝酚钠在几种作物中的临时限量。目前,已经发展了几种复硝酚钠的样品预处理方法,对食品中的复硝酚钠进行分析(china feed,2013,2,42-44;acta scientiarum naturalium universitatis,2013,6,104-109;chemical analysis and meterage,2015,1,68-70)。但是,现有方法采用单一有机溶剂提取,容易受基质干扰,并且适用的基质范围有限,不同基质缺乏统一的样品预处理方法,这会给复硝酚钠的检测造成很大麻烦,因此其需要进一步改进。
技术实现要素:
4.本发明之目的是弥补上述之不足,向社会公开简便高效、精密度高、适用范围广的一种快速检测复硝酚钠的方法。
5.本发明的技术方案是这样实现的:
6.一种快速检测复硝酚钠的方法,包括以下步骤:
7.步骤一、将1g待测样品与25ml提取液混合均匀,然后震荡提取,离心,取下层溶液过滤,得到待净化液,所述的提取液中包含有正己烷和乙腈;
8.步骤二、将得到的待净化液通过prime hlb固相萃取小柱进行富集;接着采用乙腈水溶液洗脱,收集洗脱液,混匀过滤,得到净化液;
9.步骤三、采用液相色谱-质谱串联系统对制得的净化液进行检测。
10.进一步优化本技术方案的措施是:
11.作为改进,所述的提取液中,正己烷为10ml,乙腈和磷酸水溶液为15ml;乙腈和磷酸水溶液按照体积比1:4-19混合,磷酸水溶液的ph值为1-4。所述的磷酸水溶液可用甲酸水溶液或者乙酸水溶液替代。
12.作为改进,所述的步骤一中,震荡提取的条件为震荡频率600-720rpm,提取10min-30min。
13.作为改进,所述的步骤一中,离心的条件为6000rpm-10000rpm,离心5min-15min。
14.作为改进,所述的步骤二中,洗脱用的乙腈水溶液,乙腈的体积为40%-70%
15.作为改进,所述的步骤三中,采用液相色谱-质谱串联系统对制得的净化液进行检测的具体过程为:采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。
16.本发明与现有技术相比的优点是:
17.针对复硝酚钠为强电解质、在水溶液中呈碱性的特点,在提取溶液中使用乙腈和磷酸水溶液,形成强静电相互作用,同时可以减少样品基质的干扰,从而提高提取效率;另外,在提取液中加入正己烷,有助于降低基质中油脂、蛋白质等的干扰,降低样品提取液的复杂度,利于后续的检测;接着采用prime hlb固相萃取小柱对复硝酚钠进行净化和富集。本发明的检测方法可以应用于各种动植物源性食品,包括脂肪含量和蛋白含量较高的动植物源性食品,简便高效,精密度高。
附图说明
18.图1是本发明检测加标为10.0μg/kg的阴性鸡肉的谱图。
19.图1中,1为对硝基酚钠,2为5-硝基邻甲氧基苯酚钠,3为邻硝基酚钠。纵坐标为强度,横坐标为时间(min)。
具体实施方式
20.下面结合附图进一步详细描述本发明:
21.一种快速检测复硝酚钠的方法,包括以下步骤:
22.步骤一、将待测样品与提取液混合均匀,然后震荡(震荡提取的条件为震荡频率600-720rpm,时间10min-30min)提取;离心(离心的条件为转速6000rpm-10000rpm,时间5min-15min),取下层溶液过滤,得到待净化液。所述的提取液中,正己烷为10ml,乙腈和磷酸水溶液为15ml;乙腈和磷酸水溶液按照体积比1:4-19混合,磷酸水溶液的ph值为1-4。
23.步骤二、将得到的待净化液通过prime hlb固相萃取小柱进行富集;接着采用乙腈水溶液洗脱,收集洗脱液,混匀过滤,得到净化液。上述的乙腈水溶液,乙腈的体积为40%-70%。
24.步骤三、采用液相色谱-质谱串联系统对制得的净化液进行检测,其具体过程为:采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最
后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。
25.提取液的配置过程:用磷酸将水的ph调到1-4,得到磷酸水溶液;然后乙腈和磷酸水溶液按照体积比1:4-19混合;然后取15ml乙腈和磷酸水溶液,加入10ml正己烷,就得到了提取液。上述的磷酸水溶液可用甲酸水溶液或者乙酸水溶液替代,优选为磷酸水溶液。
26.下面通过具体的实施例来进一步阐述本发明:
27.实施例1
28.称取均质后的鸡肉1.00g(精确至0.01g)于50ml聚丙烯离心管中,对添加了10.0μg/kg、20.0μg/kg、50.0μg/kg复硝酚钠标准工作液的阴性样品进行实验。加入25ml提取液(正己烷为10ml,乙腈和磷酸水溶液为15ml,乙腈:磷酸水溶液=1:4,ph值为4),涡旋混匀,震荡30min(600rpm)。9000r/min离心5min后,将溶液通过滤纸过滤到另一洁净离心管中,得到上清液,待净化。
29.将全部待净化的上清液通过prime hlb固相萃取小柱进行富集,接着用乙腈水溶液(乙腈的体积为40%)洗脱,收集洗脱液,涡旋混匀,通过0.22μm微孔滤膜得到净化液。
30.采用液相色谱-质谱串联系统对上述得到的净化液进行检测。对所获得的复硝酚钠进行反向分离后,采用质谱采集数据分析。采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。利用数据处理软件对质谱采集的数据进行分析,得到结果如图1所示(图1中,1为对硝基酚钠,2为5-硝基邻甲氧基苯酚钠,3为邻硝基酚钠)。
31.将得到的数据信息进行统计分析,结果如表1所示。
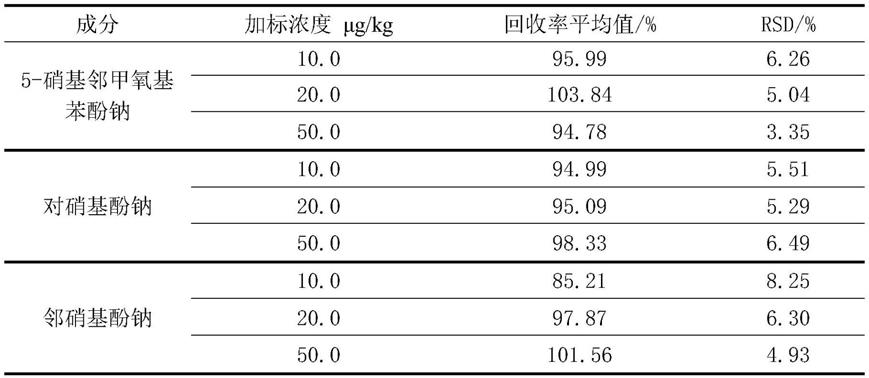
32.表1
[0033][0034]
从表1中可以看出,鸡肉中5-硝基邻甲氧基苯酚钠、对硝基酚钠和邻硝基酚钠的加标回收率平均值为85%-104%,rsd小于9%,检测回收率和精密度达到检测要求。
[0035]
实施例2
[0036]
称取均质后的小麦粉1.00g(精确至0.01g)于50ml聚丙烯离心管中,对添加了10.0μg/kg、20.0μg/kg、50.0μg/kg复硝酚钠标准工作液的阴性样品进行实验。加入25ml提取液(正己烷为10ml,乙腈和磷酸水溶液为15ml,乙腈:磷酸水溶液=1:9,ph值为2),涡旋混匀,震荡20min(650rpm)。7000r/min离心10min后,将溶液通过滤纸过滤到另一洁净离心管中,得到上清液,待净化。
[0037]
将全部待净化的上清液通过prime hlb固相萃取小柱进行富集,接着用乙腈水溶液(乙腈的体积为60%)洗脱,收集洗脱液,涡旋混匀,通过0.22μm微孔滤膜得到净化液。
[0038]
采用液相色谱-质谱串联系统对上述得到的净化液进行检测。对所获得的复硝酚钠进行反向分离后,采用质谱采集数据分析。采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。利用数据处理软件对质谱采集的数据进行分析。
[0039]
将得到的数据信息进行统计分析,结果如表2所示。
[0040]
表2
[0041][0042]
从表2中可以看出,小麦粉中5-硝基邻甲氧基苯酚钠、对硝基酚钠和邻硝基酚钠的加标回收率平均值为85%-109%,rsd小于7%,检测回收率和精密度达到检测要求。
[0043]
实施例3
[0044]
称取均质后的马铃薯1.00g(精确至0.01g)于50ml聚丙烯离心管中,对添加了10.0μg/kg、20.0μg/kg、50.0μg/kg复硝酚钠标准工作液的阴性样品进行实验。加入25ml提取液(正己烷为10ml,乙腈和甲酸水溶液为15ml,乙腈:甲酸水溶液=1:19,ph值为1),涡旋混匀,震荡10min(720rpm)。6000r/min离心15min后,将溶液通过滤纸过滤到另一洁净离心管中,得到上清液,待净化。
[0045]
将全部待净化的上清液通过prime hlb固相萃取小柱进行富集,接着用乙腈水溶液(乙腈的体积为50%)洗脱,收集洗脱液,涡旋混匀,通过0.22μm微孔滤膜得到净化液。
[0046]
采用液相色谱-质谱串联系统对上述得到的净化液进行检测。对所获得的复硝酚钠进行反向分离后,采用质谱采集数据分析。采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。利用数据处理软件对质谱采集的数据进行分析。
[0047]
将得到的数据信息进行统计分析,结果如表3所示。
[0048]
表3
[0049][0050]
从表3中可以看出,马铃薯中5-硝基邻甲氧基苯酚钠、对硝基酚钠和邻硝基酚钠的加标回收率平均值为89%-104%,rsd小于9%,检测回收率和精密度达到检测要求。
[0051]
实施例4
[0052]
称取均质后的橙子1.00g(精确至0.01g)于50ml聚丙烯离心管中,对添加了10.0μg/kg、20.0μg/kg、50.0μg/kg复硝酚钠标准工作液的阴性样品进行实验。加入25ml提取液(正己烷为10ml,乙腈和乙酸水溶液为15ml,乙腈:乙酸水溶液=1:4,ph值为3),涡旋混匀,震荡10min(720rpm)。7000r/min离心8min后,将溶液通过滤纸过滤到另一洁净离心管中,得到上清液,待净化。
[0053]
将全部待净化的上清液通过prime hlb固相萃取小柱进行富集,接着用乙腈水溶液(乙腈的体积为70%)洗脱,收集洗脱液,涡旋混匀,通过0.22μm微孔滤膜得到净化液。
[0054]
采用液相色谱-质谱串联系统对上述得到的净化液进行检测。对所获得的复硝酚钠进行反向分离后,采用质谱采集数据分析。采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。利用数据处理软件对质谱采集的数据进行分析。
[0055]
将得到的数据信息进行统计分析,结果如表4所示。
[0056]
表4
[0057][0058][0059]
从表4中可以看出,橙子中5-硝基邻甲氧基苯酚钠、对硝基酚钠和邻硝基酚钠的加标回收率平均值为86%-107%,rsd小于6%,检测回收率和精密度达到检测要求。
[0060]
实施例5
[0061]
称取均质后的奶粉1.00g(精确至0.01g)于50ml聚丙烯离心管中,对添加了10.0μg/kg、20.0μg/kg、50.0μg/kg复硝酚钠标准工作液的阴性样品进行实验。加入25ml提取液(正己烷为10ml,乙腈和磷酸水溶液为15ml,乙腈:磷酸水溶液=1:19,ph值为4),涡旋混匀,震荡10min(600rpm)。9000r/min离心5min后,将溶液通过滤纸过滤到另一洁净离心管中,得到上清液,待净化。
[0062]
将全部待净化的上清液通过prime hlb固相萃取小柱进行富集,接着用乙腈水溶液(乙腈的体积为40%)洗脱,收集洗脱液,涡旋混匀,通过0.22μm微孔滤膜得到净化液。
[0063]
采用液相色谱-质谱串联系统对上述得到的净化液进行检测。对所获得的复硝酚钠进行反向分离后,采用质谱采集数据分析。采用两种流动相:流动相a为水,流动相b为乙腈;采用如下分离梯度进行反相分离:15%流动相b,平衡0.5min;15%-30%流动相b,分离2.5min;之后才用100%流动相b,冲洗1min;最后采用15%流动相b,平衡1.5min;质谱采用负离子多反应监测模式采集数据,apci离子源温度200℃,针电流-3.0ma,气帘气流速40l/min,碰撞气流速7l/min,喷雾气流速40l/min。对硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;对硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。邻硝基酚钠定量离子对138.0/92.0m/z,去簇电压-40v,碰撞能量-28v,驻留时间100ms;邻硝基酚钠定性离子对138.0/108.0m/z,去簇电压-40v,碰撞能量-24v,驻留时间100ms。5-硝基邻甲氧基苯酚钠定量离子对168.0/95.0m/z,去簇电压-40v,碰撞能量-33v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/123.0m/z,去簇电压-40v,碰撞能量-26v,驻留时间100ms;5-硝基邻甲氧基苯酚钠定性离子对168.0/153.0m/z,去簇电压-40v,碰撞能量-19v,驻留时间100ms。利用数据处理软件对质谱采集的数据进行分析。
[0064]
将得到的数据信息进行统计分析,结果如表5所示。
[0065]
表5
[0066]
[0067][0068]
从表5中可以看出,奶粉中5-硝基邻甲氧基苯酚钠、对硝基酚钠和邻硝基酚钠的加标回收率平均值为91%-108%,rsd小于9%,检测回收率和精密度达到检测要求。
[0069]
本发明的最佳实施例已被阐明,由本领域普通技术人员做出的各种变化或改型都不会脱离本发明的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。