1.本发明涉及向狗施用益生菌组合物来减少内毒素血症并且改善消化过程的方法以及相关方法,该益生菌组合物包含枯草芽孢杆菌(bacillus subtilis)、地衣芽孢杆菌(bacillus licheniformis)和乳酸片球菌(pediococcus acidilactici)。
背景技术:
2.在许多物种(包括驯养哺乳动物、伴侣动物和宠物)中,肠道微生物群和宿主之间的相互作用在众多生理过程的调节中起重要作用。
3.益生菌组合物含有活微生物,这些活微生物在适量施用时能够为宿主提供有益作用。实现这些有益作用的机制包括降低肠通透性,增加杯状细胞的黏蛋白分泌,增加阻止病原体定殖的防御素的产生,增加短链脂肪酸产生,刺激iga分泌,降低腔道ph以及增加免疫细胞对共生微生物的耐受性,同时维持对病原体产生应答的能力(gallo等人,“modulation of microbiota as treatment for intestinal inflammatory disorders:an uptodate[作为肠炎性障碍的治疗手段的微生物群的调节:最新]”,world j.gastroenterol.[世界胃肠病学杂志]22:7186-7202(2016);barko等人,“the gastrointestinal microbiome:a review[胃肠微生物组:综述]”,j.vet.internal med.[兽医内科学杂志],32:9-25(2018))。还认为通过附着到胃肠(gi)道的粘液层并且刺激免疫功能,非活微生物能够赋予有益作用(barko等人,2018)。
[0004]
益生菌组合物通过支持有益肠道微生物区系的增殖而使其宿主受益。益生菌能够对其宿主产生有益作用,而不永久改变微生物组,这可能是由于在肠中短暂定殖(ceapa等人,“influence of fermented mild products,prebiotics and probiotics on microbiota composition and health[发酵的温和产物、益生元和益生菌对微生物群组成和健康的影响]”,best pract.res.clin.gastroenterol.[临床胃肠病学最佳实践和研究]27:139-155(2013);barko等人,2018)。
[0005]
此外,益生菌可以调节在肠细胞旁途径中充当屏障的紧密连接蛋白的频率。通过增强肠屏障功能,益生菌充当预防剂以抵御病原体的不利影响,从而促进对消化和免疫健康的积极作用。另外,似乎益生菌的有益作用可以是菌株特异性的,大多数益生菌研究在普通人群的不同特殊群组(即糖尿病、肥胖)中调查了双岐杆菌属(bifidobacterium)和乳杆菌属(lactobacillus)菌株。
[0006]
一些人认为芽孢杆菌属(bacillus)的成员比产乳酸细菌具有更高的益生菌潜力,因为它们在gi道中具有高水平的生存力并且能够繁殖且数量增加,即使在低ph的不利环境条件中也是如此。然而,其他研究者认为,细菌并非必须是活的才能发挥益生菌作用(biourge等人,“the use of probiotics in the diet of dogs[益生菌在狗的饮食中的用途]”,j.nutrition[营养学杂志],128(12期增刊):2730s-2732s(1998);schmitz和suchodolski,“understanding the canine intestinal microbiota and its modification by pro-,pre-,and synbiotics-what is the evidence?[了解犬的肠微生
物群及益生菌、益生元和合生素对它的改善——证据是什么?]”vet.med.sci.[兽医科学杂志],2:71-94(2016))。
[0007]
目前,认为益生菌是患有肠道障碍(如肠漏)的狗的潜在替代治疗。内毒素血症是所有哺乳动物中都存在的病症。其特征为血清内毒素水平升高。它可以影响gi通透性、gi微生物群或二者(mcfarlin等人,2015)。在人类医学中,已知在进餐后约5小时出现这种升高,并且它影响大约33%的人群(kirshnan,“metabolic endotoxemia,a driving force behind chronic illness[代谢性内毒素血症,慢性病背后的驱动力]”,aapi’s nutrition guide to optimal health using principles of functional medicine&nutritional genomics[aapi的最佳健康营养指南,使用功能医学和营养基因组学原理],第iii部分:269-286(2017))。在狗的情况下,在静脉内输注低剂量内毒素后,报告了轻度内毒素血症水平(bartko等人,“selective glucocorticoid receptor modulation inhibits cytokine responses in a canine model of mild endotoxemia[在轻度内毒素血症的犬模型中,选择性糖皮质激素受体调节抑制细胞因子应答],pharmacolog.res.[药理学研究]125:215-223(2017);devries等人,“establishment of a low dose canine endotoxemia model to test anti-inflammatory drugs:effects of prednisolone[低剂量犬内毒素血症模型的建立,用来测试抗炎药物:泼尼松龙的效果]”,intl.j.immunopathol.and pharmacol.[国际免疫病理学与药理学杂志],26(4):861-869(2013)),但是并未表征天然存在的内毒素血症。已经在人类中研究了实验诱导的内毒素血症,其中利用推注大肠杆菌(escherichia coli)内毒素(deventer等人,“experimental endotoxemia in humans:analysis of cytokine release and coagulation,fibrinolytic,and complement pathways[人类中的实验内毒素血症:细胞因子释放和凝血、溶纤维蛋白药和补体途径的分析]”,blood[血液],76(12):2520-2526(1990)),或通过进食高脂餐(mcfarlin等人,“oral spore-based probiotic supplementation was associated with reduced incidence of post-prandial dietary endotoxin,triglycerides,and disease risk biomarkers[口服补充基于孢子的益生菌与餐后饮食内毒素、甘油三酯和疾病风险生物标志物的出现率降低相关]”,world j.gastrointest.pathophysiol.[世界胃肠病理生理学杂志],8:117-126(2017))。
技术实现要素:
[0008]
在一个实施例中,本发明涉及减少狗的内毒素血症的方法,该方法包括以下步骤:提供包含枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌的益生菌组合物,以及以有效减少该狗的内毒素血症的量向该狗施用该益生菌组合物。在一个实施例中,本发明还涉及改善狗的消化和消化过程,和/或治疗狗的消化障碍。
[0009]
在一个实施例中,本发明包括枯草芽孢杆菌hu58和/或地衣芽孢杆菌sl-307。在一个实施例中,益生菌组合物的离散剂量单位的总cfu可以是约10亿至约100亿cfu,包括例如约25亿至约40亿cfu。在一个实施例中,本发明的方法可以永久性抑或暂时性用于健康的狗或者用于患有胃肠障碍的狗。
附图说明
[0010]
图1是显示根据本发明的受试者的入选和处置的组合图。
[0011]
图2是显示在本发明的益生菌组合物施用之前和之后在健康的狗中干物质、粗蛋白、粗脂肪、粗纤维素和nfe的平均消化率参数的图。
[0012]
图3是显示在根据本发明的益生菌组合物施用之前和之后在健康的狗中与内毒素血症有关的平均值和趋势线的图。
[0013]
图4是显示在本发明的益生菌组合物施用之前和之后在健康的狗中平均cd14值的图。
[0014]
图5是显示在本发明的益生菌组合物施用之前和之后在健康的狗中平均il-1b值的图。
[0015]
图6是显示在本发明的益生菌组合物施用之前和之后在患有生态失调(dysbiosis)的狗中内毒素血症的平均值和趋势线的图。
[0016]
图7是显示在本发明的益生菌组合物施用之前和之后在患有生态失调的狗中平均cd14值的图。
[0017]
图8是显示在本发明的益生菌组合物施用之前和之后在患有生态失调的狗中平均il-1b值的图。
[0018]
图9是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中红细胞比容动力学的图。
[0019]
图10是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中血红蛋白动力学的图。
[0020]
图11是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中红细胞动力学的图。
[0021]
图12是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中平均红细胞体积动力学的图。
[0022]
图13是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中平均红细胞血红蛋白动力学的图。
[0023]
图14是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中平均红细胞血红蛋白浓度动力学的图。
[0024]
图15是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中白细胞动力学的图。
[0025]
图16是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中嗜中性粒细胞动力学的图。
[0026]
图17是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中嗜酸性粒细胞动力学的图。
[0027]
图18是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中单核细胞动力学的图。
[0028]
图19是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中淋巴细胞动力学的图。
[0029]
图20是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失
调的狗中丙氨酸氨基转移酶动力学的图。
[0030]
图21是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中白蛋白动力学的图。
[0031]
图22是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中碱性磷酸酶动力学的图。
[0032]
图23是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中淀粉酶动力学的图。
[0033]
图24是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中肌酸酐动力学的图。
[0034]
图25是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中球蛋白动力学的图。
[0035]
图26是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中葡萄糖动力学的图。
[0036]
图27是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中总胆红素动力学的图。
[0037]
图28是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中总蛋白动力学的图。
[0038]
图29是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中血尿素氮动力学的图。
[0039]
图30是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中血钙动力学的图。
[0040]
图31是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中磷动力学的图。
[0041]
图32是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中钾动力学的图。
[0042]
图33是显示在本发明的益生菌组合物施用之前和之后在健康的狗和患有生态失调的狗中钠动力学的图。
[0043]
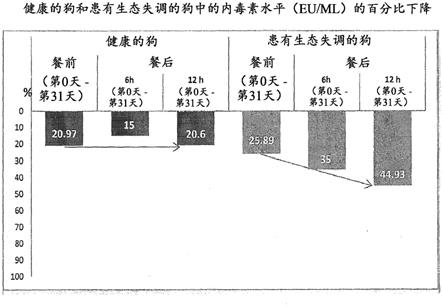
图34是显示在本发明的益生菌组合物施用之前(第0天)和之后(第31天)在健康的狗和患有生态失调的狗中内毒素血症水平(eu/ml)的变化的图。
[0044]
图35是显示根据本发明在健康的狗和患有生态失调的狗中在餐前(before/ante-)和餐后(after/post-)从第0天至第31天的内毒素水平的百分比下降的图。
具体实施方式
[0045]
本发明涉及向狗施用益生菌组合物的方法,该益生菌组合物包含枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌。
[0046]
以下定义和讨论旨在引导理解,但不旨在关于本技术的其他披露内容进行限制。所提及的在本发明组合物中的百分比(%)是给定组分的重量相对于所讨论组合物的总重量的%,也表示为“w/w”,除非另有说明。
[0047]
如本文所用,本说明书和权利要求中所用的动词“包含”及其变化形式以其非限制
性含义使用,意指包括该词之后的项目,但不排除未具体提及的项目。此外,不定冠词“一个/种(a或an)”对要素的提及不排除存在多于一个/种要素的可能性,除非上下文明确要求存在一个且仅一个要素。因此,不定冠词“一个/种(a或an)”通常意指“至少一个/种”。
[0048]
如本文所用,“有效量”或“对
……
有效的量”定义为在必要的剂量下和时间段内有效实现所需生物结果(例如减少、预防或治疗疾病或病症和/或诱导特定的有益作用)的量。本披露内容的组合物的有效量可根据例如个体的年龄、性别和体重等因素而变化。可以调整剂量方案以提供最佳应答。可每日施用几个分开的剂量,或者可如个体情况的紧急程度所示按比例减少剂量。根据本发明,可以按有效量的枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌施用单个每日剂量。如将容易理解的,根据本披露内容的组合物可以按单份或全天间隔的多份施用。如本领域技术人员将理解的,份量不必限于每日施用,并且可以按每两天或每三天或其他方便有效的方式进行。根据情况的紧急程度,在给定日期的施用可以是按单份或全天间隔的多份进行。
[0049]
根据本发明,根据本发明的“受试者”、“患者”或其他个体是狗。
[0050]
本发明的“益生菌组合物”包含枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌。本发明的益生菌组合物可以包含以下、基本上由以下组成、或由以下组成:枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌。在一个实施例中,本发明的益生菌组合物是一种经包封的饮食补充剂,每个胶囊包含总共40亿cfu枯草芽孢杆菌hu58、地衣芽孢杆菌sl-307和乳酸片球菌以及180mg脱脂草饲牛肝提取物。hu58(“probiotene
tm”)是枯草芽孢杆菌菌株,其制剂由印度孟买的维里迪斯生物制药私人有限公司(viridis biopharma pvt.ltd.)制造。枯草芽孢杆菌hu58已保藏在美国国家生物技术研究中心(national center for biotechnology research),保藏号为ef101709。芽孢杆菌属遗传保藏中心(bacillus genetic stock center,“bgsc”)为芽孢杆菌属hu58指定的编号为3a34,而ncimb有限公司指定的菌株编号为30283。在本发明的益生菌组合物中还使用了地衣芽孢杆菌菌株。在本发明的益生菌组合物中还使用了乳酸片球菌菌株。在一个实施例中,本发明的益生菌组合物包含约20亿cfu hu58、约5亿至10亿cfu乳酸片球菌以及1亿cfu地衣芽孢杆菌,每天一次以胶囊形式口服施用;在一个实施例中,这样的组合物是在一个实施例中,本发明的胶囊由纤维素制成。在不同的实施例中,本披露内容披露了益生菌组合物以及产生和使用这些益生菌组合物的方法。在其他实施例中,本发明的益生菌组合物支持狗的消化健康、减少狗的内毒素血症和/或治疗狗的消化障碍。
[0051]
已基于对研究参与者补充包含一种或多种定殖型益生菌材料菌株的组合物经实验验证了这些作用,这些菌株可以是基于孢子的益生细菌菌株。
[0052]
可以按菌落形成单位(“cfu”)测量本发明的益生菌组合物。有效剂量通常是数亿的cfu或更高。如果益生菌被用于帮助消化,则益生菌应随餐服用,否则如果在两餐之间服用,特别是如果与有助于稀释胃酸并使益生菌更快地进入消化道的液体一起服用,则益生菌可能会存活。可以短期或长期给予益生菌。
[0053]
在一些实施例中,益生菌微生物在组合物中的浓度可以是至少约1
·
109cfu/g、至少约2
·
109cfu/g、至少约3
·
109cfu/g、至少约4
·
109cfu/g、至少约5
·
109cfu/g、至少约6
·
109cfu/g、至少约7
·
109cfu/g、至少约8
·
109cfu/g、至少约9
·
109cfu/g、至少约1
·
10
10
cfu/g、至少约2
·
10
10
cfu/g、至少约3
·
10
10
cfu/g、至少约4
·
10
10
cfu/g、至少约5
·
10
10
cfu/g、至少约6
·
10
10
cfu/g、至少约7
·
10
10
cfu/g、至少约8
·
10
10
cfu/g、至少约9
·
10
10
cfu/g、或至少约1
·
10
11
cfu/g,以及其中的任何范围。
[0054]
在一个实施例中,基于孢子的益生菌组合物可以包含在原位暴露于胃酸后存活率在以下任何范围内的孢子:约75%至约99%、约80%至约95%、约85%至约90%、以及大于约90%。基于孢子的益生菌组合物可以包含在以下任何范围内的许多孢子:约10亿至约100亿个孢子、约15亿个孢子至约95亿个孢子、约25亿个孢子至约80亿个孢子、约30亿个孢子至约70亿个孢子、约35亿个孢子至约60亿个孢子、约40亿个孢子至约50亿个孢子、和约40亿个孢子。
[0055]
在一个实施例中,基于孢子的益生菌组合物可包括液体、糖果制品、粉剂或丸剂形式,或者可以添加到食物产品中或配制为饮食补充剂。例如,在一个实施例中,益生菌组合物可以呈粉剂形式并且添加至狗粮中。在一个实施方式中,每克散装干燥原粉中存在约1
·
10
10
cfu微生物,其中每克含有约60%或更少的细菌质量和约40%的载体系统。在其他实施方式中,每克含有约70%或更少的细菌质量和约30%的载体系统、约80%或更少的细菌质量和约20%的载体系统、约90%或更少的细菌质量和约10%的载体系统、约50%或更少的细菌质量和约50%的载体系统、约40%或更少的细菌质量和约60%的载体系统、约30%或更少的细菌质量和约70%的载体系统、约20%或更少的细菌质量和约80%的载体系统、或约10%或更少的细菌质量和约90%的载体系统。
[0056]
本文披露的方法和组合物的实施方式可包括基于孢子的益生菌。基于孢子的益生菌由内体组成,这些内体对酸性ph高度耐受,在室温下是稳定的,并且与传统的益生菌补充剂相比向小肠递送更大量的高生存力细菌。传统的微囊化使用活微生物,然后将这些微生物微囊化以力求对其进行保护;然而,这是一个固有地导致微生物最终死亡从而降低微生物功效的过程。使用经天然微囊化以形成内体的基于孢子的微生物可能是优选的,因为这些微生物处于休眠状态并且不经历功效随时间的下降。
[0057]
这些基于孢子的微生物也特别具有热稳定性并且可以经受uv巴氏杀菌,因此它们也能够在热暴露或uv巴氏杀菌之前添加到食物产品或饮料中,而不经历功效随时间的下降。
[0058]
微囊化
[0059]
在某些实施方式中,在添加至益生菌组合物之前将益生菌微生物进行微囊化。微囊化是通过包衣包围微小颗粒或液滴以得到具有许多有用特性的小胶囊的工艺。在相对简单的形式中,微胶囊是周围具有均匀的壁的小球体。微胶囊内部的材料称为核心、内相或填充物,而壁有时称为壳、包衣或膜。大多数微胶囊的直径在几微米到几毫米之间。
[0060]“微囊化”的定义已经扩大,并且包括大多数食品。每类食品成分均已被包封;香料是最常见的。微囊化技术取决于待包封材料的物理和化学特性。参见例如,l.s.jackson和k.lee,microencapsulation and the food industry[微囊化和食品工业],lebensmittel-wissenschaft technologie[食品科学技术](1991年1月1日),出于描述微囊化的目的,将其通过引用并入本文。
[0061]
然而,许多微胶囊与这些简单的球体几乎没有相似之处。核心可以是晶体、锯齿状吸附剂颗粒、乳液、皮克林乳液(pickering emulsion)、固体悬浮液或较小微胶囊的悬浮
液。微胶囊甚至可以具有多个壁。可以使用各种技术来生产微胶囊,并且本领域普通技术人员将理解各种此类技术中的每一种。可用于生产微胶囊的这些技术包括但不限于如下所述的锅包衣、空气悬浮包衣、离心挤出、振动喷嘴、喷雾干燥、离子型凝胶化、界面缩聚、界面交联、原位聚合和基质聚合。
[0062]
锅包衣
[0063]
广泛用于制药工业的锅包衣工艺是用于形成小的包衣颗粒或片剂的最古老的工业程序之一。使颗粒在锅或其他装置中翻滚,同时缓慢施加包衣材料。
[0064]
空气悬浮包衣
[0065]
空气悬浮包衣由威斯康星大学(university of wisconsin)的dale eavin wurster教授于1959年首次描述,与锅包衣相比,它提供了改善的控制和灵活性。在该工艺中,将固体颗粒状核心材料分散到支撑气流中,并用挥发性溶剂中的聚合物包衣这些悬浮颗粒,从而在其上留下非常薄的聚合物层。重复该过程几百次,直到获得所需的参数(如包衣厚度等)。支撑颗粒的气流也有助于对它们进行干燥,并且干燥速率与气流温度成正比,可改变气流温度以进一步影响包衣的特性。
[0066]
颗粒在包衣区部分中的再循环受腔室设计及其操作参数影响。包衣腔室被布置成使得颗粒向上通过包衣区,然后分散到移动较慢的空气中并沉回到包衣腔室的底部,重复通过包衣区直到获得所需的包衣厚度。
[0067]
离心挤出
[0068]
使用含有同心喷嘴的旋转挤出头来包封液体。在该工艺中,核心液体射流被壁溶液或熔体的外壳包围。当射流移动通过空气时,由于瑞利不稳定性(rayleigh instability),射流破裂成核心液滴,每个液滴皆包覆有壁溶液。当液滴在飞行中时,熔融壁可能变硬或溶剂可能从壁溶液中蒸发。由于大多数液滴在平均直径的 10%以内,它们落在喷雾喷嘴周围的窄环中。因此,如果需要,胶囊可以在形成后通过将它们捕获在环形硬化浴中而变硬。该工艺非常适合形成直径400-2,000μm的颗粒。由于液滴是通过液体射流的破裂形成的,该工艺仅适用于液体或浆液。可以实现高生产率,即每个喷嘴每小时每个头可以生产高达22.5kg(50lb)的微胶囊。含有16个喷嘴的头可供使用。
[0069]
振动喷嘴
[0070]
可以使用通过喷嘴的层流和喷嘴或液体的附加振动来进行核心-壳包封或微粒化(基质包封)。振动必须在瑞利不稳定性的共振中进行,并产生非常均匀的液滴。液体可由具有限定黏度(0-10,000mpa
·
s已被证明有效)的任何液体组成,例如溶液、乳液、悬浮液、熔体等。固化可以根据所使用的凝胶化系统使用内部凝胶化(例如,溶胶-凝胶处理、熔融)或外部凝胶化(另外的黏合剂系统,例如,在浆液中)进行。该工艺非常适用于产生20-10,000μm之间的液滴,更小和更大液滴的应用是已知的。这些装置在工业和研究中主要以1-20,000kg/小时(2-44,000lb/h)的容量,在20℃-1500℃(68
°
f-2732
°
f)(室温直至熔融硅)的工作温度下使用。具有一个直到几十万个喷嘴的喷嘴头可供使用。
[0071]
喷雾干燥
[0072]
当活性材料溶解或悬浮在熔体或聚合物溶液中并被捕获在干燥颗粒中时,喷雾干燥用作微囊化技术。主要优点是由于在干燥器中接触时间短而能够处理不稳定材料;此外,该操作是经济的。在现代喷雾干燥器中,待喷雾溶液的黏度可高达300mpa
·
s。通过将该技
术与使用超临界二氧化碳相结合,可以包封敏感材料(如蛋白质)。
[0073]
离子型凝胶化
[0074]
凝聚-相分离工艺由在连续搅拌下进行的三个步骤组成:(1)形成3个不混溶的化学相:液体制造媒介物相、核心材料相和包衣材料相。(2)包衣的沉积:将核心材料分散在包衣聚合物溶液中。将包衣聚合物材料包被在核心周围。通过在核心材料和媒介物相之间形成的界面处吸附的聚合物而在核心周围沉积液体聚合物包衣。(3)包衣的硬化:包衣材料在媒介物相中是不混溶的,并且其形式上变硬。硬化技术包括热、交联或去溶剂化(dissolvation)。
[0075]
界面缩聚
[0076]
在界面缩聚中,缩聚中的两种反应物在界面处相遇并迅速反应。该方法的基础是酰氯与含有活性氢原子的化合物(如胺或醇、聚酯、聚脲或聚氨酯)之间的经典肖顿-鲍曼(schotten-baumann)反应。在合适的条件下,柔性薄壁在界面处迅速形成。将农药和二酰氯的溶液在水中乳化,并添加含有胺和多官能异氰酸酯的水溶液。存在碱以中和反应过程中形成的酸。缩合的聚合物壁在乳液液滴的界面处瞬间形成。
[0077]
界面交联
[0078]
界面交联源自界面缩聚,并且开发界面交联是为了避免使用毒性二胺,用于药物或化妆品应用。在该方法中,含有活性氢原子的小双官能单体被生物来源的聚合物(如蛋白质)替代。当在乳液界面进行反应时,酰氯与蛋白质的各种官能团反应,从而形成膜。该方法非常通用,并且微胶囊的特性(尺寸、孔隙率、可降解性、机械阻力)可以变化。设想了人工微胶囊在微氟通道中的流动。
[0079]
原位聚合
[0080]
在一些微囊化工艺中,在颗粒表面上进行单一单体的直接聚合。在一种工艺中,例如,将纤维素纤维包封在聚乙烯中,同时浸入无水甲苯中。常用沉积速率为约0.5μm/min。包衣厚度范围为0.2-75μm(0.0079-3.0密耳)。包衣是均匀的,即使在尖锐的突起上也是如此。蛋白质微胶囊具有生物相容性和生物可降解性,并且蛋白质骨架的存在使得膜比通过界面缩聚获得的那些膜更具有抗性和弹性。
[0081]
基质聚合
[0082]
在许多工艺中,在颗粒形成过程中将核心材料包埋在聚合物基质中。这种类型的简单方法是喷雾干燥,在该方法中通过从基质材料中蒸发溶剂来形成颗粒。然而,基质的固化也可由化学变化引起。
[0083]
在一个实施例中,“施用(administering、administration等)”是指向受试者提供本发明的益生菌组合物,使得枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌可以到达受试者的胃肠道,并且直接和/或例如通过产生且释放代谢物或其他活性化学物质作用于gi道的组织和/或细胞和/或gi道中(如细菌),从而减少内毒素血症、改善消化过程和/或治疗胃肠障碍。在一个实施例中,受试者是健康的狗或患有gi道障碍的狗。根据本发明,向受试者施用可以是口服,例如以饮食补充剂形式、以固体剂型(如胶囊)或以液体剂型和/或经由其他途径(例如作为栓剂经直肠)施用。在一个实施例中,本发明的益生菌组合物(如)是在餐前、随餐或餐后口服的。“同时施用”是指将本发明的益生菌例如与抗
生素或可能不利于肠道健康的其他物质、或例如与有益于肠道健康的另一物质同时(包括同一天)施用。
[0084]
在一个实施例中,根据本发明的“饮食补充剂”是指本发明的益生菌组合物,它是作为受试者饮食的补充口服施用,而非天然或常规食品。在一个实施例中,饮食补充剂包含有效量的枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌,使得这些物质在施用至狗时进入狗的消化道并且在狗的消化道中以及身体其他地方适当地发挥作用,从而减少内毒素血症、改善消化过程和/或治疗胃肠障碍。
[0085]
在一个实施例中,饮食补充剂或其他形式的本发明的益生菌组合物是每日施用,持续1天、1-7天、1-14天、1-30天、1-31天、1-32天、1-60天,或持续另一段时间。在一个实施例中,可以长期服用益生菌组合物,例如每日或每周,持续几个月或一年或数年。
[0086]
在一个实施例中,可以施用本发明的益生菌组合物来治疗受试者的肠生态失调、内毒素血症或gi道的其他障碍。
[0087]
在一个实施例中,可以施用本发明的益生菌组合物来预防受试者的肠生态失调、内毒素血症或gi道的其他障碍。
[0088]
在一个实施例中,可以施用本发明的益生菌组合物来改善受试者的gi道的健康和消化。
[0089]
结合以下实例和实施例,可以进一步理解本发明。本技术通篇描述的实例和实施例是出于说明本发明而提供,而并不旨在作为限制。实例
[0090]
在此实例中,根据本发明的基于孢子的益生菌组合物(含有枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌)在施用30天后减少了狗的内毒素血症。此外,鉴定了在临床上健康的狗和患有明显生态失调的那些狗中天然餐后内毒素血症水平的模式。
[0091]
研究设计
[0092]
年龄在4个月和7岁之间的总共18只成年狗入选了研究。每日一次伴随进餐向狗施用包含枯草芽孢杆菌、地衣芽孢杆菌和乳酸片球菌的益生菌组合物,持续30天(参见表1)。
[0093]
在第-5天至第0天,开始从健康的狗采集粪便。
[0094]
在研究的第0天,对狗进行临床检查,并且采集粪便和血液样品。为了检测内毒素血症,采集餐前和餐后(6小时和12小时)血液样品。由兽医进行临床检查,目的是评估每只狗的总体健康状况。检查包括收集体温、心率和呼吸速率数据。
[0095]
在第1天至第30天,根据制造商的建议向动物施用益生菌组合物。在第31天,如上文所描述对所有狗进行临床检查,并且采集生物样品(粪便和血液)用于临床辅助(paraclinical)检查。为了检测内毒素血症,采集餐前和餐后(6小时和12小时)血液样品。
[0096]
在第31天至第36天,将从健康的狗采集的粪便至少用于消化率研究。表1研究时间表
[0097]
研究群体
[0098]
此研究使用真实世界的临床病例,如图1中所示。图1显示了患者处置。使用下文描述的研究排除/纳入标准来仔细地筛选患者。合格的狗入选研究。在入选研究的18只狗中,总共11只狗完成了整个研究期:5(五)只健康的狗(表2)和6(六)只患有生态失调的狗(表3)。在研究全程中,这些狗并没有经历任何生活方式或营养的改变。
[0099]
健康的狗的纳入标准包括不存在gi表现(腹泻、呕吐),在过去6个月没有抗生素治疗史,临床上健康并且每天正常进食1餐。如果这些狗患有急性肝病或肾病、有肠内寄生、或在过去6个月有过抗生素治疗,则从健康的狗的组中排除这些狗。
[0100]
对于患有肠生态失调的狗,纳入标准是目前在进行抗生素治疗(最少持续2周),或存在gi表现(腹泻、呕吐),并且每天正常进食一餐。如果这些狗患有急性肝病或肾病或如果它们有肠内寄生,则排除这些狗。表2健康的狗*提前终止;已接受益生菌给药;保留在研究中,仅用于粪便评分和消化率研究表3患有肠生态失调的狗
[0100]
治疗
[0101]
测试的益生菌产品包含两种细菌菌株:枯草芽孢杆菌hu58和乳酸片球菌(fidospore
tm
)。以胶囊形式给予益生菌。伴随每日饮食,每日施用一个胶囊,持续30天。将肝粉用于改善益生菌产品的味道,并且确保它被摄取。
[0102]
临床调查
[0103]
为了评估进入研究的狗的健康状况并且获得基线临床数据,给予每只狗临床评估。对狗进行总体临床检查,包括收集与临床参数有关的数据。在此研究中,认为默克兽医手册(merck veterinary manual)(2016)中狗的正常范围值是正常临床值。
[0104]
粪便评分
[0105]
在益生菌治疗期间,要求狗主人完成由普瑞纳公司(purina)制定的optidigest临床表(www.purina.com;原始表可在https://www.purina.ro/produse/proplan-optidigest上获得)。临床表分为三个部分:粪便稠度、粪便量和气味、以及肠道紊乱(gut rambling)和气胀。
[0106]
粪便稠度部分使用粪便评分量表在一整天中评估了狗的粪便。该量表描述如下:1-非常硬并且干燥,2-结实但是不硬,3-圆木状,4-非常潮湿,5-非常潮湿但具有明显的形状,6-具有纹理但没有限定的形状,7-水状无纹理,平的。
[0107]
粪便量和气味部分也是在一整天中记录的。将粪便量分级为1-少量,2-正常量,3-大量,4-非常大的量。将气味记录为1-非常小的气味,2-低气味,3-适度难闻的气味,4-难闻的气味,5-非常难闻的气味。
[0108]
在日间评估了肠道紊乱和气胀部分并且记录了它们是否存在。
[0109]
在研究的第1天、第7天、第15天和第30天填写所有这些数据。
[0110]
消化率
[0111]
使用消化率系数(d.c.)来测量饲料的消化率,它代表饲料或饲料营养素未在粪便中回收的部分,即动物已吸收的部分。将方程i用于确定表观消化率系数(adc%):
从此原理出发,确定了以下项的水平:干物质(dm),粗蛋白-凯氏定氮法(kjeldahl method)(cp),粗脂肪-索格利特法(soxhlet method)(cf),粗纤维素-温德法(weende method)(cc),无氮提取物(nfe)。
[0112]
仅在健康的狗中确定消化率。生物样品是粪便和食物样品。在治疗开始之前的5天以及在施用益生菌组合物结束之后的5天采集粪便。
[0113]
临床辅助调查
[0114]
寄生虫学
[0115]
在施用益生菌之前和之后,对本研究中入选的11只狗进行粪便学检查。使用了漂浮(威利斯法(willis method))和沉降的技术。目的是查看益生菌作用是否没有因存在体内寄生虫而被错误判断。
[0116]
血液学参数
[0117]
将血液采集到具有抗凝血剂(edta)的血液管中。通过装置abacus junior vet分析血液学样品(表4)。将获得的所有数据与来自默克兽医手册(2016)的参考进行比较。
[0118]
在益生菌组合物施用之前(第0天)和之后(第31天)进行这些评估(表5)。表4血液学参数和它们的方法表5血液样品调查(健康的狗和患有生态失调的狗)
*仅针对3只狗
[0119]
生化参数
[0120]
使用了vet scan化学分析仪与提供以下项的定量测定的综合测试:在肝素化全血、肝素化血浆或血清中的丙氨酸氨基转移酶(alt)、白蛋白(alb)、碱性磷酸酶(alp)、淀粉酶(amy)、总钙(ca
)、肌酸酐(cre)、球蛋白(glob)、葡萄糖(glu)、磷(phos)、钾(k )、钠(na )、总胆红素(tbil)、总蛋白(tp)和尿素氮(bun)。将获得的所有数据与来自默克兽医手册(2016)的参考进行比较。
[0121]
在益生菌组合物施用之前(第0天)和之后(第31天)进行这些评估(表5)。
[0122]
内毒素血症的确定
[0123]
为了测定内毒素血症,我们使用了toxinsensor
tm
显色lal内毒素测定试剂盒(金斯瑞公司(genscript),皮斯卡塔韦,新泽西州(美国))。此方法利用改良的鲎变形细胞溶解物和合成的生色底物通过显色来检测内毒素。可以使用分光光度计(545nm滤波器)测量终产物,并且可以通过与标准曲线比较来确定内毒素水平。该试剂盒具有0.01eu/ml的最低内毒素检测极限和0.01至1eu/ml的可测量浓度范围。
[0124]
对所有狗(健康的和患有生态失调的)进行内毒素血症评估。研究方案包括餐前和餐后(6小时和12小时)血清每日益生菌施用中的内毒素血症评估(表5)。使用如下的血清评估内毒素血症:未稀释的血清、1:1稀释的血清、1:2稀释的血清。在益生菌组合物施用之前(第0天)和之后(第31天)进行这些评估(表5)。根据标准曲线(r2=0.9808)计算1:2稀释的血清的结果。
[0125]
免疫/炎性参数
[0126]
为了调查免疫/炎性参数,我们使用了:犬il-1β(白介素1β)elisa试剂盒-根据标准曲线(r2=0.9527)计算结果。nori犬cd14 elisa试剂盒-根据标准曲线(r2=0.991)计算结果。犬il-6(白介素6)elisa试剂盒-对于此参数,od值不在标准曲线内并且无法解释结果。对所有狗(健康的和患有生态失调的)进行il1b(白介素-1-β,在针对感染和损伤的宿主防御应答中重要的促炎细胞因子)和cd14(激活固有免疫细胞的关键分子)的评估。调查方案与内毒素血症的方案是相同的。对于患有生态失调的狗,调查方案包括餐前和餐后(6小时和12小时)动力学中此参数的评估。在益生菌组合物施用之前(第0天)和之后(第
31天)进行这些评估(表5)。
[0127]
对于健康的狗的组,由于一些血液样品的溶血和方案的修改,我们仅对益生菌组合物施用之前(第0天)和之后(第31天)的结果具有完整的动力学,而没有这些日期餐前和餐后6或12小时的结果(表5)。
[0128]
统计学分析
[0129]
使用条件方差分析(anova)和以下条件(方程ii)分析数据:(健康的狗或患有生态失调的狗)
×
(实验时间(第0天和第31天))
×
(进餐时间(餐前、餐后6小时、餐后12小时))。方程ii将显著性设置为p《0.05,使用施图登特-纽曼-科伊尔斯(student-newman-keuls)多重比较检验来确定显著性。通过趋势线和r2的表述,使用线性回归确定研究参数的变化。结果
[0130]
临床检查
[0131]
在开始益生菌治疗之前(第0天)和在研究结束时(第31天),对所研究的所有狗进行总体临床检查。
[0132]
在临床检查期间,所有狗都不存在显著的治疗需求。所研究的所有狗都具有正常体温,范围是37.9℃至39.9℃。心率并不指示具有显著临床重要性的任何问题。所有研究的狗都存在高于正常值的呼吸速率。狗的呼吸速率的正常静止值是每分钟18至34次呼吸。提高的呼吸速率并不是警报,并且可以解释为兴奋、应激和/或检查室中温度高。
[0133]
用本发明的益生菌组合物进行治疗并不改变健康的狗的临床表现。在健康的狗中没有观察到如腹泻或呕吐等症状。益生菌治疗改善了狗的皮毛外观,并且诱导了皮肤损害的改善。
[0134]
对于患有生态失调的狗,初始临床检查揭示了腹泻、呕吐和/或皮肤损害;取决于研究中纳入的合格的每只狗的症状,临床症状而有所不同。在用本发明的益生菌组合物完成30天的治疗后,我们观察到消化症状的减少,并且在一些病例中,消化问题消失。在这些狗的整体状况方面观察到改善,改善的细节取决于每只狗的原始诊断。在狗10-y中(参见表3),在用本发明的益生菌组合物完成30天的治疗时观察到健康状态的改善,并且主人要求再继续治疗30天。
[0135]
粪便评分
[0136]
在用本发明的益生菌组合物进行治疗期间,要求狗主人填写由普瑞纳公司制定的optidigest临床表。如上文所讨论,该临床表分为三个部分:粪便稠度、粪便量和气味、以及肠道紊乱和气胀。
[0137]
在大多数狗中,用本发明的益生菌组合物进行治疗略微改善了粪便稠度和粪便量。根据optidigest表结果,用本发明的益生菌组合物进行治疗并未改善粪便的气味。在用本发明的益生菌组合物进行治疗之前、期间、或之后,肠道紊乱并不存在于任何狗中。然而,仅在治疗之前存在气胀的狗中,气胀似乎得到改善(参见表6、表7)。表6健康的狗的粪便评分
表7患有生态失调的狗的粪便评分
[0138]
消化率
[0139]
通过测量表观消化率系数研究了饲料的消化率,显示出所有研究的组分(干物质、粗脂肪、粗纤维素和nfe)的消化率的重要改善,但粗蛋白除外,其中在一个病例(狗02-h)中值是降低的(参见表8,图2)。对于干物质、粗蛋白和nfe,消化率的提高是统计上重要的(p<0.001)。表8消化率的演化(%)-健康的狗
***
p<0.001-极显著
[0140]
血液学
[0141]
狗的血液学参数是相当多样的,但始终在狗的正常值范围内。然而,我们观察到血红蛋白(hb)、平均红细胞血红蛋白(mch)和平均红细胞血红蛋白浓度(mchc)的略微增加(参见表9和10)。
[0142]
在用本发明的益生菌组合物进行治疗之前和之后的白细胞值呈现了多样的结果,但仍在狗的正常值范围内。在治疗后,在大多数狗中,嗜酸性粒细胞值趋向于略微增加。嗜中性粒细胞、嗜碱性粒细胞、单核细胞和淋巴细胞视个体的狗增加或减少(参见表11和12)。个体变异和平均变异并不被认为具有病理学内涵。
[0143]
在患有生态失调的狗中观察到具体情况,其中嗜酸性粒细胞平均值有小的增加趋势。在施用后具有嗜酸粒细胞增多(30%)的14-m患者显示此情况。此值与钩虫病的诊断相关,由于寄生虫(犬钩虫(ancylostoma coninum))的生物周期,施用之前并未证明钩虫病。表9红细胞参数的演化-健康的狗表10红细胞参数的演化-患有生态失调的狗表11白细胞参数的演化-健康的狗表12白细胞参数的演化-患有生态失调的狗
[0144]
生物化学
[0145]
对生化参数的调查指示不同系统和器官的健康,并且还指示益生菌组合物如何对狗产生作用(表13)。表13调查的生化参数
[0146]
表14、15、16和17呈现了在用本发明的益生菌组合物进行治疗之前和之后所有病例的生化参数结果。
[0147]
狗的生化参数是多样的,但始终在狗的正常值范围内。生化结果与施用之前和之后记录的临床观察结果相关。
[0148]
在健康的狗的组中07-i患者显示出施用之前高水平的alt和钾。此增加与其他生化参数、血液学参数或临床参数的改变无关,所以该狗保留在研究中。施用之后的alt水平在物种的生理学极限内,并且钾继续以更高水平存在。表14生化参数的演化-健康的狗表15生化参数的演化-患有生态失调的狗
表16电离图的演化-健康的狗表17电离图的演化-患有生态失调的狗
[0149]
内毒素血症
[0150]
a.健康的狗
[0151]
观察到在益生菌组合物施用之前,餐后6小时的平均内毒素水平与餐前平均水平相比有所升高(餐前,0.465
±
0.113eu/ml;餐后6小时,0.473
±
0.172eu/ml)。在完成30天的益生菌施用后,观察到相同的动力学,其中内毒素水平从0.3677
±
0.2266eu/ml(餐前)升高至0.388
±
0.233eu/ml(餐后6小时)(参见表19,显示了在健康的狗和患有生态失调的狗中内毒素血症水平的变化;和图34,显示了在健康的狗和患有生态失调的狗中内毒素血症水平(eu/ml)的变化(益生菌治疗之前和之后))。由于个体的狗之间的高水平变异,这些差异在统计学上并不显著。
[0152]
重要的是,在施用益生菌组合物30天后,内毒素水平下降(参见表18和图3)。图35显示了在健康的狗中,从第0天至第31天,内毒素水平(eu/ml)的平均百分比下降(益生菌治疗之前和之后),并且如下:餐前:20.97%;餐后6小时:15%;餐后12小时:20.6%。与内毒素水平下降的趋势直接关联的是cd14的演化(表20;图4)。两个参数的相关系数(r=0.8452,r2=0.744)指示了统计显著性(p=0.05)。表18内毒素血症的演化(fu/ml)-健康的狗
表19内毒素血症水平的变化(eu/ml)表20cd14的演化(pg/ml)-健康的狗
[0153]
关于il1b水平的演化,此参数的值保持相对恒定(表21,图5)。表21il1b的演化(ng/ml)-健康的狗
[0154]
b.患有生态失调的狗
[0155]
在用本发明的益生菌组合物完成治疗后,内毒素血症水平下降(参见表22,图6、图34)。在益生菌施用后观察到的内毒素血症的下降趋势具有显著递增的动力学(r2=0.9536)(图6、图34)。这指示了肠状况的显著改善,这与在狗中看到的相较于这些狗的原始诊断的临床改善相关。
[0156]
观察到的最重要的变化是在完成本发明的益生菌组合物的30天施用后,在患有生态失调的狗中内毒素水平的下降(图35)。从第0天至第31天的百分比下降如下:餐前:25.89%,餐后6小时:35%,餐后12小时:44.93%。表22内毒素血症的演化(eu/ml)-患有生态失调的狗表23cd14的演化(pg/ml)-患有生态失调的狗表24il1b的演化(ng/ml)-患有生态失调的狗从cd 14的演化的角度来看,内毒素血症减少的趋势与内毒素水平直接相关(表23,图7)。施用之前和之后的值(餐前)之间的相关性是统计学上显著的(p=0.05),其中相关系数是r=0.08445和r2=0.744。在研究期间,il1b水平保持相对恒定(表24,图8)。
[0157]
图9-33显示了在健康的狗和患有生态失调的狗中血液学参数和生化参数的施用之前和之后的动力学。讨论
[0158]
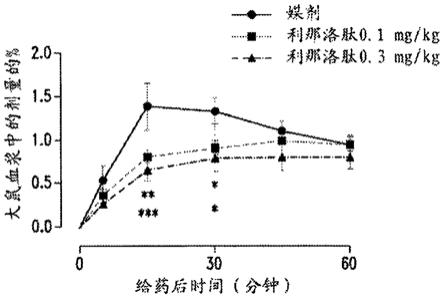
内毒素血症是影响肠道正常发挥功能的病症。在兽医学中,尚未充分研究代谢性内毒素血症。目前可用的数据通常是从人类医学外推的,或获自使用狗作为产品测试的犬模型的研究。从此类研究中,我们已获知少量内毒素(0.1g/kg)能够在狗中产生轻度内毒素血症(bartko等人,2017)。另一研究尝试通过以单次推注方式静脉内注射0.03、0.1或1.0ug/kg体重脂多糖(这会导致轻度内毒素血症)建立犬内毒素血症模型(f.de vries等人,2013)。
[0159]
在人类中,已知进餐后大约5小时出现内毒素水平升高(kirshnan,2017)。与餐后内毒素血症有关的来自人类研究的发现不能外推至狗,这是由于消化过程(即完成食物消化所使用的酶和需要的时间)在个体和品种之间不同。此外,狗和人类的饮食之间的差异相当大,这是鉴于狗是食肉动物而人类是杂食动物。
[0160]
饲喂给狗的饮食类型对它们经历的天然内毒素血症水平具有主要影响。在我们的研究中,患者01-k(健康的狗的组)遵循基于生食的饮食,而健康的狗的组中的另四只狗仅食用干狗粮。因为饮食的突然改变会造成gi失衡,如腹泻或甚至呕吐,因此在我们的研究中,我们并未改变狗的饮食。入选研究的狗遵循它们的常用饮食,食物类型和进食间隔与它们习惯的相同。对内毒素血症结果的深入研究显示,在健康的狗的组中,患者01-k的内毒素血症水平与其他狗之间存在差异。尽管在健康的狗的组中的五个患者全部都符合此研究的纳入标准,但事实上,患者01-k遵循基于生食的饮食,可能对进餐后血流中吸收的内毒素水平具有影响。
[0161]
内毒素血症可以存在于狗中而没有任何临床体征。此外,它会发生在进餐后临床上健康的个体中,而无论饮食中的脂肪组成如何。在健康组中,我们观察到餐后6小时,平均内毒素血症水平上升(对比餐前水平)。在开始益生菌治疗之前和在完成30天益生菌治疗后,此观察结果确实如此。尽管我们报告了在狗完成益生菌治疗后,在这些狗中,餐后6小时的平均内毒素水平上升(对比餐前),但是我们还观察到,在益生菌治疗完成之前和之后,检测到的内毒素水平显著下降。在餐前和餐后(6小时和12小时)时间点,观察到此下降。当比较第0天和第31天的内毒素水平时,餐前水平下降了20.97%,餐后6小时的水平下降了15%,并且餐后12小时的水平下降了20.6%。这些结果支持我们的以下假设,益生菌治疗能够改善健康个体的肠消化,且由此降低炎症和内毒素血症水平。
[0162]
在患有生态失调的狗的组中观察到相同模式。与益生菌治疗完成后获得的那些结果相比,在开始益生菌治疗之前的全部三个时间点(餐前、餐后6小时、餐后12小时),内毒素血症水平都更高。此外,与健康组中的结果相比,平均百分比下降更大。我们报告了餐前内毒素水平的25.89%下降(第0天至第31天)、餐后6小时的35%下降和餐后12小时的44.93%下降。益生菌治疗后的内毒素水平下降的这一趋势表明了益生菌治疗对gi道中重新建立稳态具有功效和影响。
[0163]
目前,关于狗的餐后天然内毒素血症水平,没有可用数据。我们研究的主要假设是从人类医学(kirshnan,2017)(其中此类数据是可用的)外推的。然而,狗和人类的消化过程是不同的。其中部分消化的食物停留在狗的胃中的时间量是4小时至8小时,在个体和品种
之间略有差异,而对于人类,消化过程持续约1小时。两个物种之间的消化过程的另一差异是gi道长度在个体全身尺寸中的占比(the canine digestion process[犬消化过程],[全狗杂志](2019),可在https://www.whole-dog-journal.com/health/digestion/the-canine-digestio n-process上获得)。此类方面可能影响可检测血清内毒素的时间。考虑到该信息,我们决定在进餐后6小时和12小时评估血清内毒素水平。在狗的两个组中,对于所有餐后评估,均观察到血清内毒素水平上升(对比餐前),具有小的变异。此发现支持我们的以下假设,在进餐后,血清内毒素水平升高。
[0164]
进行了血清内毒素水平的动力学测试,目的是确认检测餐后内毒素水平的最佳时间。在分析我们的结果后,我们已经确定,对于检测餐后内毒素水平,不存在最佳的特定模式或时间点。在所研究的所有狗中,我们都观察到餐后内毒素水平升高。此观察结果支持以下假设:在进餐后,内毒素水平升高,这已经在人类中得到证明(mcfarlin等人,2015;kirshnan,2017)。结论
[0165]
此研究中获得的数据提供了在健康的狗和患有生态失调的狗两者中,关于天然内毒素血症水平的新信息。此外,对于入选研究的所有犬患者,向狗施用基于孢子的益生菌降低了治疗前和治疗后的内毒素水平,并且改善了消化过程。
[0166]
健康的狗
[0167]
在健康的狗中,使用本发明的益生菌组合物没有表现出不利影响。并没有对狗身体的总体功能造成不利影响。血液学参数和生化参数显示了施用本发明的益生菌组合物之前和之后的略微变化,其中值在正常范围内。施用本发明的益生菌组合物改善了粪便评分,并且减少了气胀。在治疗后粪便重量广泛下降,这是由于提高了饲料的消化率。关于饲料的消化率的研究测量了表观消化率系数,显示出所有研究的组分(干物质、粗脂肪、粗纤维素和无氮提取物)的消化率的重要改善。在餐前以及餐后6小时和12小时分析了内毒素血症。在一些狗中,在6小时后餐后内毒素血症值增加,而在其他狗中,12小时后增加。总体而言,在施用本发明的益生菌组合物30天后,观察到内毒素水平下降。取平均,在餐前,在第0天至第31天,内毒素血症减少了20.97%。取平均,在第0天至第31天,餐后(postprandial/post-meal)6小时,内毒素血症减少了15%,并且取平均,在第0天至第31天,餐后12小时,内毒素血症减少了20.60%。与内毒素水平下降的趋势直接关联的是cd14的演化。两个参数的相关系数(r=0.8452;r2=0.744)指示了统计显著性(p=0.05)。il1b水平保持相对恒定。
[0168]
患有生态失调的狗
[0169]
在患有生态失调的狗中,我们观察到消化障碍的减少和/或消失。观察到狗的整体状况的改善,这取决于原始诊断和病理学。血液学参数和生化参数显示了取决于病理学的变异,注意到受试者的有益变化。在施用之前和之后,内毒素血症减少,具有以下平均百分比差异:25.89%(餐前,第0至31天);35%,餐后6小时(第0至31天);和44.93%,餐后12小时(第0至31天)。施用后的内毒素血症的下降趋势包括显著递增的动力学(r2=0.9536)。cd14的演化趋向于下降,这与内毒素水平直接关联。餐前的施用之前和之后的值之间的相关性是统计学上显著的(p=0.05)。在研究期间,il1b水平保持相对恒定。
[0170]
生物伦理学委员会批准:此研究获克卢日-纳波卡农业科学与兽医大学
(university of agricultural sciences and veterinary medicine of cluj-napoca)的生物伦理学委员会批准。
[0171]
在将所有涉及的程序和测试产品充分告知每只参与狗的主人后,并且在所有主人自愿签署了关于让他们的狗参与的知情同意书后,进行研究程序。所有研究程序都在不伤害任何参与动物的情况下进行。
[0172]
除非本文另有说明或与上下文明显矛盾,否则在描述本发明的上下文中(尤其是权利要求的上下文中),使用术语“一个/一种(a、an)”、“该/这些(the)”以及相似的指示语应解释为包括单数和复数两者。除非本文另有说明,否则本文中对值范围的描述仅旨在用作逐一提及落入该范围内的每个单独值的简写方法,并且每个单独值被并入本说明书中,如同其在本文中被逐一描述一样。术语“约”的使用旨在描述在大约
±
10%范围内高于或低于所述值的值;在其他实施例中,这些值的范围值可以在大约
±
5%的范围内高于或低于所述值;在其他实施例中,这些值的范围值可以在大约
±
2%的范围内高于或低于所述值;在其他实施例中,这些值的范围值可以在大约
±
1%的范围内高于或低于所述值。前述范围旨在通过上下文变得清楚,并未隐含进一步的限制。除非本文另有说明或与上下文明显矛盾,否则本文描述的所有方法步骤均可以以任何合适的顺序进行。除非另外声明,否则本文提供的任何和所有实例或示例性语言(例如,“如”)的使用仅旨在更好地说明本发明,而非对本发明的范围施加限制。说明书中的文字不应被解释为表示任何未要求保护的要素对本发明的实践都是必不可少的。
[0173]
虽然在前述说明书中已经就本发明的某些实施例对本发明进行了描述,并且出于说明的目的已经提出了许多细节,但是对于本领域技术人员显而易见的是,本发明容许另外的实施例,并且可以在不偏离本发明的基本原理的情况下对本文描述的某些细节进行相当大的改变。
[0174]
在不偏离本发明的精神或本质属性的情况下,本发明可以以其他具体形式体现,且因此,应参考所附权利要求而非前述说明书来指示本发明的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。