1.本发明涉及信息处理技术领域,尤其涉及一种肝癌术后早期复发预测模型构建方法及装置。
背景技术:
2.肝癌(hepatocellular carcinoma,hcc)的术后复发率极高,是临床当前面临的关键问题之一,更有研究表明早期复发患者相对晚期复发患者的术后预后差。因此,对肝癌患者开展复发监测是至关重要的,它可以用来指导临床决策,极大改善患者的术后预后。
3.目前,tnm分期系统是评估肝癌术后预后的常用方法,但其并不能用于患者肝癌术后早期复发的预测。
4.因此,如何更好地对肝癌术后早期复发进行预测已成为业界亟待解决的问题。
技术实现要素:
5.本发明提供一种肝癌术后早期复发预测模型构建方法及装置,用以更好地对肝癌术后早期复发进行预测。
6.本发明实施例提供一种肝癌术后早期复发预测模型构建方法,包括:
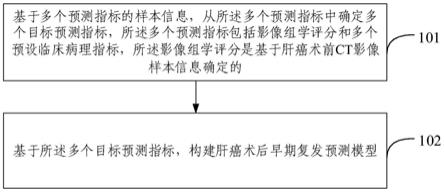
7.基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,其中,所述多个预测指标包括影像组学评分和多个预设临床病理指标,所述影像组学评分是基于肝癌术前ct影像样本信息确定的;
8.基于所述多个目标预测指标,构建肝癌术后早期复发预测模型。
9.根据本发明实施例提供的一种肝癌术后早期复发预测模型构建方法,所述基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,包括:
10.对所述多个预测指标的样本信息进行单因素cox回归分析,得到回归分析结果,以基于所述回归分析结果确定多个候选预测指标;
11.对所述多个候选预测指标进行多因素cox回归分析,确定多个目标预测指标。
12.根据本发明实施例提供的一种肝癌术后早期复发预测模型构建方法,在所述基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标之前,包括:
13.基于多个肝癌术前ct影像样本信息,确定每个所述肝癌术前ct影像样本信息的影像组学特征集;
14.基于所述影像组学特征集,确定目标影像组学特征集;
15.基于每个所述目标影像组学特征集,确定各个所述肝癌术前ct影像样本信息的影像组学评分。
16.根据本发明实施例提供的一种肝癌术后早期复发预测模型构建方法,所述基于多个肝癌术前ct影像样本信息,确定每个所述肝癌术前ct影像样本信息的影像组学特征集,包括:
17.基于预设体素大小,对各个所述肝癌术前ct影像样本信息进行重采样,得到每个
所述肝癌术前ct影像样本信息对应的重采样影像信息;
18.基于各个所述重采样影像信息中感兴趣区域的影像组学特征集,确定每个所述肝癌术前ct影像样本信息的影像组学特征集。
19.根据本发明实施例提供的一种肝癌术后早期复发预测模型构建方法,在所述基于多个肝癌术前ct影像样本信息,确定每个所述肝癌术前ct影像样本信息的影像组学特征集之前,还包括:
20.获取多个肝癌病例样本信息;
21.从所述多个肝癌病例样本信息中,去除满足预设排除条件的肝癌病例样本信息,得到多个目标肝癌病例样本信息,其中,所述预设排除条件包括不包含肝癌术前ct影像信息、肝癌术前ct影像信息的生成时间超过目标时间、临床与随访信息中至少部分信息缺失和接受过肝切、消融及经导管动脉化疗栓塞术手术;
22.基于所述多个目标肝癌病例样本信息,确定所述多个肝癌术前ct影像样本信息和每个所述肝癌术前ct影像样本信息对应的对象的多个预设临床病理指标的样本信息。
23.根据本发明实施例提供的一种肝癌术后早期复发预测模型构建方法,在构建肝癌术后早期复发预测模型之后,还包括:
24.基于所述肝癌术后早期复发预测模型,确定对应的列线图;
25.基于所述列线图,确定肝癌术后早期复发的概率。
26.本发明实施例还提供一种肝癌术后早期复发预测模型构建装置,包括:
27.第一处理模块,用于基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,其中,所述多个预测指标包括影像组学评分和多个预设临床病理指标,所述影像组学评分是基于肝癌术前ct影像样本信息确定的;
28.第一建模模块,用于基于所述多个目标预测指标,构建肝癌术后早期复发预测模型。
29.本发明还提供一种电子设备,包括存储器、处理器及存储在存储器上并可在处理器上运行的计算机程序,所述处理器执行所述程序时实现如上述任一种所述肝癌术后早期复发预测模型构建方法的步骤。
30.本发明还提供一种非暂态计算机可读存储介质,其上存储有计算机程序,该计算机程序被处理器执行时实现如上述任一种所述肝癌术后早期复发预测模型构建方法的步骤。
31.本发明还提供一种计算机程序产品,包括计算机程序,所述计算机程序被处理器执行时实现如上述任一种所述肝癌术后早期复发预测模型构建方法的步骤。
32.本发明提供的一种肝癌术后早期复发预测模型构建方法及装置,通过采用影像组学的方法,根据获取的多个对象的肝癌术前ct影像样本信息,确定各个对象的肝癌术前ct影像样本信息的影像组学评分,结果显示基于增强ct影像学特征拟合得到的影像组学评分与早期复发呈正相关联关系,进一步通过对包括影像组学评分和多个预设临床病理指标的多个预测指标的样本信息,进行单因素和多因素cox回归的联合分析,确定与肝癌术后早期复发相关联的多个目标预测指标,并基于该目标预测指标构建肝癌术后早期复发预测模型,本发明的预测模型可以高效地对肝癌患者早期复发做出准确预测,极大地改善了肝癌术后患者的预后。
附图说明
33.为了更清楚地说明本发明或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
34.图1是本发明实施例提供的肝癌术后早期复发预测模型构建方法的流程示意图;
35.图2是本发明实施例提供的肝癌术后早期复发预测模型构建方法的计算结果显示示意图之一;
36.图3是本发明实施例提供的肝癌术后早期复发预测模型的列线图示意图;
37.图4是本发明实施例提供的肝癌术后早期复发预测模型构建方法的计算结果显示示意图之二;
38.图5是本发明实施例提供的肝癌术后早期复发预测模型构建方法的计算结果显示示意图之三;
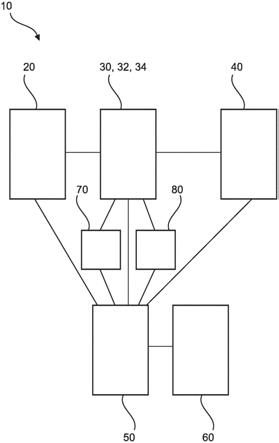
39.图6是本发明实施例提供的肝癌术后早期复发预测模型构建装置的结构示意图;
40.图7是本发明实施例提供的电子设备的结构示意图。
具体实施方式
41.为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明中的附图,对本发明中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
42.下面结合图1-图7描述本发明实施例提供的肝癌术后早期复发预测模型构建方法及装置。
43.需要说明的是,影像学手段是肝癌患者规范化管理中的关键一环,包括超声、电子计算机断层扫描(computed tomography,ct)和核磁(magnetic resonance imaging,mri)在内,均在肝癌的筛查和诊断中扮演重要角色。
44.肝癌在增强ct中典型的影像征象为“快进快出”,表现为动脉期病灶均匀或不均匀强化,门静脉期低于肝组织的强化。
45.近年来,随着人工智能技术的飞速发展,影像组学也逐渐进入人们的视野,与传统依赖影像医师的判断不同的是,影像组学可以挖掘图像里隐藏的潜在信息,而这些信息可能包含病理生理学的特性,对疾病诊断、疗效评估和预后预测起到非常重要的作用。
46.本发明基于影像组学研究的基础上,提出以下方法来解决现有技术中不能进行肝癌患者术后早期复发预测的缺陷。
47.图1是本发明实施例提供的肝癌术后早期复发预测模型构建方法的流程示意图,如图1所示,包括:步骤101和步骤102。
48.其中,步骤101,基于多个预测指标的样本信息,从多个预测指标中确定多个目标预测指标,其中,多个预测指标包括影像组学评分和多个预设临床病理指标,影像组学评分是基于肝癌术前ct影像样本信息确定的;在本步骤中,本发明实施例所描述的肝癌术前ct影像样本信息指的是肝癌患者在进行肝癌根治性切除术前的增强ct影像信息,其主要为增
强ct图像信息。
49.本发明实施例所描述的影像组学评分指的是基于影像学特征的单发hcc患者术后生存的预后指标,其具体可以是通过对肝癌术前ct影像样本信息中提取到的影像组学特征进行回归分析得到,可用于评价患者术后的预后。
50.在本实施例中,根据各个肝癌患者的肝癌术前ct影像样本信息中的影像组学特征的值与对应的线性组合,分别计算出每个患者的影像组学评分。
51.本发明实施例所描述的多个预测指标包括影像组学评分和多个预设临床病理指标。
52.本发明实施例所描述的多个预设临床病理指标指的是预先选取的肝癌病例中多个临床病理指标,其可以包括乙型肝炎表面抗原(hbsag)(有或无)、肝硬化(有或无)、微血管侵犯(microvascular invasion,mvi)(有或无)、血清甲胎蛋白(alpha fetoprotein,afp)(》200vs.≤200ng/ml)、肿瘤大小(cm)、血小板(
×
109/l)、谷氨酰转移酶(gamma-glutamyl transpeptidase,ggt)(u/l)、肝硬化fib-4指数和白蛋白-胆红素(albumin-bilirubin,albi)中的任意一个或任意多个信息。
53.在一些实施例中,在基于多个预测指标的样本信息,从多个预测指标中确定多个目标预测指标之前,包括:
54.基于多个肝癌术前ct影像样本信息,确定每个肝癌术前ct影像样本信息的影像组学特征集;
55.基于影像组学特征集,确定目标影像组学特征集;
56.基于每个目标影像组学特征集,确定各个肝癌术前ct影像样本信息的影像组学评分。
57.在本实施例中,基于多个肝癌术前ct影像样本信息,确定每个肝癌术前ct影像样本信息的影像组学特征集之前,还包括:
58.获取多个肝癌病例样本信息;
59.从多个肝癌病例样本信息中,去除满足预设排除条件的肝癌病例样本信息,得到多个目标肝癌病例样本信息,其中,预设排除条件包括不包含肝癌术前ct影像信息、肝癌术前ct影像信息的生成时间超过目标时间、临床与随访信息中至少部分信息缺失和接受过肝切、消融及经导管动脉化疗栓塞术手术;
60.基于多个目标肝癌病例样本信息,确定多个肝癌术前ct影像样本信息和每个肝癌术前ct影像样本信息对应的对象的多个预设临床病理指标的样本信息。
61.需要说明的是,为了便于说明,以下所描述的预测模型即为本发明构建的肝癌术后早期复发预测模型。
62.本发明实施例所描述的肝癌术前ct影像样本信息对应的对象即为肝癌术前ct影像样本信息所对应的肝癌患者。
63.本发明实施例所描述的预设排除条件指的是预先设置筛选预测模型所需病例样本数据而设置的排除条件,用于将不符合要求的病例数据进行排除。
64.本发明实施例所描述的目标肝癌病例样本信息指的是多个肝癌病例样本信息中去除满足预设排除条件的肝癌病例样本信息后所剩下的肝癌病例样本信息。
65.其中,预设排除条件包括不包含肝癌术前ct影像信息、肝癌术前ct影像信息的生
成时间超过目标时间、临床与随访信息中至少部分信息缺失和接受过肝切、消融及经导管动脉化疗栓塞术手术
66.在本实施例中,根据预设排除条件,从两个医务中心收集了537例接受了根治性切除的单发hcc患者,中心一和中心二中分别有277和125位患者符合要求而被纳入到本发明的研究中,对这些患者的肝癌病例样本信息进行收集与汇总。
67.在本实施例中,肝癌病例样本信息包括患者的基本信息、术前增强ct影像信息、临床病理资料和实验室检查结果等信息,其中,患者的基本信息包括性别、年龄等,临床病理资料是从医院病例系统采集而来,内容包括肿瘤大小、微血管浸润等;实验室检查结果指的是术前最后一次实验室检查的内容,其包括血常规、肝功能和甲胎蛋白等。
68.可以理解的是,临床病理资料可以获取到多个预设临床病理指标的样本信息。
69.在本发明的实施例中,从两个中心机构中纳入了共402例含术前增强ct的肝癌患者,其中,中心一的277名患者的肝癌病例样本信息作为训练集;中心二的125名患者的肝癌病例样本信息作为验证集,基线特征如表1所示。除ast外,两个队列之间其他指标均没有显着差异,可以看到大多数为男性(均为85.6%)、合并肝硬化(92.1%和93.6%)和乙肝感染(分别为83.8%和82.4%)的肝癌患者。
70.其中,中心一的中位随访时间为54.2个月,中位总生存时间为40.0个月,277例中有102例复发,早期复发率为36.8%;中心二的中位随访时间为50.7个月,总生存时间为37.0个月,126例中有41例复发,早期复发率为32.8%。
71.在本发明的实施例中,早期复发指的是2年内的复发。
72.需要说明的是,术后复发的监测均按照各中心机构的标准实施,术后两年内至少每2个月随访一次,2年后每3-6个月随访一次,检查内容包括腹部超声、血清afp和其他血清学指标。一旦被怀疑为复发,则进行增强ct或mri检查。
73.进一步地,从各个目标肝癌病例样本信息中,获取对应的肝癌术前ct影像样本信息,由此可以得到多个肝癌术前ct影像样本信息和每个肝癌患者术前ct影像样本信息所对应对象的多个预设临床病理指标的样本信息。
74.本发明实施例的方法,通过预设排除条件,从获取的多个肝癌病例样本信息中去除不符合的病例样本,从而得到符合要求的目标肝癌病例样本信息,确定多个肝癌术前ct影像样本信息,以对本发明构建的预测模型提供有效的样本数据,确保构建的预测模型的准确性。
75.在本发明的实施例中,各个肝癌术前ct影像样本信息都是已经勾画了感兴趣区(region of interest,roi)的影像数据,基于影像组学中运用的高通量计算,可以在勾画好的roi的影像数据中,能够快速提取成百上千个影像组学特征。
76.其中,本发明实施例所描述的影像组学特征集指的是提取的影像组学特征的集合,其可以包括一阶直方图特征、形状特征,如2d形状特征和3d形状特征、灰度共生矩阵、灰度运行长度矩阵、灰度大小区域矩阵和相邻灰度差分矩阵。
77.在本实施例中,roi指的是动脉期和门静脉期的肿瘤区域。
78.其中,在一些实施例中,基于多个肝癌术前ct影像样本信息,确定每个肝癌术前ct影像样本信息的影像组学特征集,包括:
79.基于预设体素大小,对各个肝癌术前ct影像样本信息进行重采样,得到每个肝癌
术前ct影像样本信息对应的重采样影像信息;
80.基于各个重采样影像信息中感兴趣区域的影像组学特征集,确定每个肝癌术前ct影像样本信息的影像组学特征集。
81.具体地,本发明实施例所描述的预设体素大小指的是预先设置的图像体素尺寸,其可以为不同大小的尺寸,如1
×1×
1m3、2
×2×
2m3等,其具体可以根据实际需求进行设置。
82.在本实施例中,为了最大程度地对肝癌术前ct影像样本信息进行图像标准化,所有的肝癌术前ct影像样本信息都被重采样为1x 1x 1m3的体素,以此,通过对所有图像重采样,减少不同图像之间的不一致性,有利于提高影像组学特征提取的效率和可重复性。
83.进一步地,对各个肝癌术前ct影像样本信息进行预设体素的重采样,以得到每个肝癌术前ct影像样本信息对应的重采样影像信息,进而对各个重采样影像信息中感兴趣区域进行影像组学特征提取,得到影像组学特征集,将该影像组学特征集作为对应肝癌术前ct影像样本信息的影像组学特征集。
84.其中,在本发明的实施例中,可以通过python平台的程序包pyradiomics,使用pyradiomics库从roi中提取影像组学特征集。
85.本发明实施例的方法,通过对所有肝癌术前ct影像样本信息进行预设体素的重采样,实现图像标准化,进而基于重采样影像信息进行影像组学特征提取,有利于确保影像组学特征集提取的效率和可重复性。
86.本发明实施例所描述的目标影像组学特征集指的是通过回归分析方法从影像组学特征中筛选出的多个影像组学特征,其可以作为与肝癌术后早期复发相关联的影像组学特征的集合。
87.在本发明的一个具体实施例中,为了过滤和筛选早期复发相关联的目标影像组学特征集,可以使用lasso cox回归分析,该方法是一种压缩估计,它通过构造一个惩罚函数得到一个较为精炼的模型,使得它压缩一些回归系数,即强制系数绝对值之和小于某个固定值;同时设定一些回归系数为零,从而实现特征变量的筛选。
88.具体地,基于从roi中提取的影像组学特征,构建lasso回归的损失函数,通过控制损失函数中的参数λ,能够筛选出较少的特征变量,由此,根据最小λ值得到目标影像组学特征集。
89.进一步地,基于目标影像组学特征集建立cox回归模型,根据模型回归系数计算影像组学评分。
90.表1
[0091][0092]
在一个具体的实施例中,如上述表1所示,基于lasso回归,控制参数λ最小,筛选增强ct图像信息中动脉期和门静脉期时期的目标影像组学特征集,在本实施例中,从增强ct图像信息中提取的影像组学特征集中总共包含有1915个影像组学特征,其中筛选得到的目标影像组学特征集包括31个目标影像组学特征,这些目标影像组学特征被用于计算影像组学评分。
[0093]
其中,目标影像组学特征集的具体内容可见表1,目标影像组学特征集包括31个目标影像组学特征,具体包括7个一阶直方图特征、5个形状特征、4个灰度共生矩阵、11个灰度大小区域矩阵和4个相邻灰度差分矩阵。
[0094]
进一步地,基于每个目标影像组学特征,可以得到各个肝癌术前ct影像样本信息的影像组学评分。在本实施例中,基于表1所示的目标影像组学特征,影像组学评分的具体公式如下所示:
[0095]
radiomics score=0.00241102866054083
×
original_firstorder_kurtosis 0.00103935017538724
×
log-sigma-4-0-mm-3d_gldm_largedependenceemphasis 3.29265498443856e-07
×
log-sigma-4-0-mm-3d_ngtdm_busyness -0.00278950794927153
×
wavelet-llh_firstorder_energy -0.745176233146374
×
wavelet-llh_glcm_imc2 0.402765595173488
×
wavelet-llh_glszm_small area low gray level emphasis 0.0231318849625246
×
wavelet-lhh_gldm_dependence variance 0.00149406284067344
×
wavelet-hll_firstorder_kurtosis -0.0105618491990747
×
wavelet-hll_firstorder_skewness 0.107590892774391
×
wavelet-hll_glszm_high gray level zone emphasis -1.57012280235555e-07
×
wavelet-hll_glszm_low gray level zone emphasis -0.206364983031861
×
wavelet-hll_glszm_small area low gray level emphasis 0.482335788287376
×
wavelet-hlh_glszm_size zone nonuniformity normalized 2.82684579394048
×
wavelet-hhh_glszm_gray level nonuniformity normalized -5.91055937169995e-06
×
wavelet-hhh_glszm_gray level variance -8.95965086558836e-10
×
wavelet-hhh_glszm_zone variance 0.292514718247067
×
diagnostics_image-interpolated_minimum -1.23410066333207
×
original_shape_elongation 0.0236512673356836
×
original_firstorder_skewness 0.0622209829350435
×
original_glszm_size zone nonuniformity normalized -0.0395358372705624
×
log-sigma-4-0-mm-3d_glcm_imc1 0.159341596846025
×
log-sigma-4-0-mm-3d_glcm_imc2 0.0867595218277089
×
log-sigma-4-0-mm-3d_gldm_dependence entropy 0.895562050952573
×
log-sigma-4-0-mm-3d_glszm_smallareaemphasis 0.00872892880125978
×
log-sigma-4-0-mm-3d_glszm_smallareahighgraylevel emphasis -0.0187124454472297
×
wavelet-llh_firstorder_skewness 0.00862344544953026
×
wavelet-lhh_firstorder_kurtosis 0.0232703178647521
×
wavelet-lhh_gldm_dependence variance -0.110126477083458
×
wavelet-hll_glcm_imc2 -0.0898127762442921
×
wavelet-hhl_glszm_small area low gray level emphasis 0.301195917977213
×
wavelet-hhl_glszm_small area low gray level emphasis;
[0096]
其中,radiomics score表示影像组学评分。
[0097]
需要说明的是,为了验证影像组学评分模型的识别能力,可以通过绘制总生存期(overall survival,os)和无复发生存期(recurrence-free survival,rfs)的生存曲线来判断。其中,os为手术日至死亡或者随后一次随访的时间,rfs为手术日直到任何部位的复发、死亡或最后一次随访。
[0098]
接收者操作特征(receiver operating characteristic curve,roc)曲线,是反映敏感性和特异性连续变量的综合指标,其可以很好地对模型输出结果的准确性进行评估。其中,曲线下方部分的面积(area under curve,auc),用来表示模型输出结果的准确性,auc值越大,即曲线下方的面积越大,说明预测结果准确性越高,也就是说,曲线越接近左上角,则预测结果的准确性越高。
[0099]
图2是本发明实施例提供的肝癌术后早期复发预测模型构建方法的计算结果显示示意图之一,如图2所示,基于对训练集和验证集进行影像组学评分计算结果以及预测rfs
的影像组学评分的roc曲线,显示出早期复发和非早期复发的影像组学评分之间存在显著差异,通过影像组学评分可以很好地区分早期复发和非早期复发,基于训练集和验证集的roc曲线中auc均为0.73,由此可以说明影像组学评分对早期复发肝癌具有一定预测价值。
[0100]
在本发明的实施例中,通过提取每个肝癌术前ct影像样本信息的影像组学特征集,基于lasso cox回归分析筛选出与肝癌术后早期复发相关联的目标影像组学特征集,并基于每个目标影像组学特征集,来计算影像组学评分,可以快速有效地得到各个肝癌术前ct影像样本信息的影像组学评分。
[0101]
本发明实施例所描述的目标预测指标在单因素和多因素cox回归分析中也称为独立预测指标,其指的是直接影响肝癌术后早期复发的预测指标。
[0102]
本发明的实施例中,根据对多个预测指标的样本信息,即各个影像组学评分和每个肝癌患者术前ct影像样本信息所对应对象的各个临床病理指标的样本信息,先进行单因素cox回归分析,确定单因素cox回归分析结果,根据单因素cox回归分析结果,再进行多因素cox回归分析,可以从这些预测指标中可以确定出与肝癌术后早期复发相关联的多个目标预测指标。
[0103]
在一些实施例中,基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,包括:
[0104]
对所述多个预测指标的样本信息进行单因素cox回归分析,得到回归分析结果,以基于所述回归分析结果确定多个候选预测指标;
[0105]
对所述多个候选预测指标进行多因素cox回归分析,确定多个目标预测指标。
[0106]
具体地,本发明实施例所描述的候选预测指标指的是对肝癌术后早期复发预测具有统计学意义的信息。
[0107]
在本发明的实施例中,根据对各个影像组学评分和每个肝癌术前ct影像样本信息所对应对象的各个临床病理指标的样本信息,进行单因素cox回归分析计算,得到回归分析结果,基于回归分析结果可以获得影像组学评分和各个临床病理指标的样本信息对应的风险比率值(hazard ratio,hr)与显著性p值,基于显著性p值,可以从影像组学评分和众多临床病理指标的样本信息中,筛选出对肝癌术后早期复发预测具有统计学意义的多个候选预测指标;
[0108]
进一步地,将这些候选预测指标再纳入多因素cox回归分析,可以得到各个候选预测指标对应的hr值和p值,根据p值,从这些候选预测指标中可以确定出与肝癌术后早期复发相关联的多个目标预测指标。
[0109]
表2是本发明实施例提供的单因素和多因素cox回归分析表,如表2所示,在单因素cox回归分析中,选取p值小于0.05作为对肝癌术后早期复发预测具有统计学意义的多个预测指标,可以看出,具有统计学意义的多个预测指标包括影像组学评分、微血管侵犯、血清afp、肿瘤大小和γ-谷氨酰胺转移酶这4个预测指标。
[0110]
表2
[0111][0112]
如表2所示,在多因素cox回归分析中,选取p值小于0.05作为与肝癌术后早期复发相关联的多个目标预测指标。通过对影像组学评分、微血管侵犯、血清afp、肿瘤大小和γ-谷氨酰胺转移酶这4个预测指标进行多因素cox回归分析,可以得到各个预测指标对应的hr值和p值,可以看出,p值小于0.05的预测指标只有影像组学评分和血清afp。
[0113]
由此,通过对各个影像组学评分和每个肝癌术前ct影像样本信息对应的对象的临床病理信息,进行单因素和多因素cox回归分析,最终统计分析得到影像组学评分和血清afp为与肝癌术后早期复发相关联的目标预测指标。
[0114]
本发明实施例的方法,通过对所述多个预测指标的样本信息进行单因素和多因素cox回归分析,得到影像组学评分和血清afp为与肝癌术后早期复发相关联的目标预测指标,有利于提高本发明构建的预测模型预测结果的准确性。
[0115]
步骤102,基于多个目标预测指标,构建肝癌术后早期复发预测模型。
[0116]
在确定多个目标预测指标之后,可以建立基于影像组学和临床指标的联合模型,即肝癌术后早期复发预测模型,通过肝癌术后早期复发预测模型,可以计算预测肝癌术后早期复发的概率。
[0117]
在本实施例中,预测模型的具体公式如下:
[0118]
rs=α0 α1*f1 α2*f2 α3*f3
…
αn*fn;
[0119]
其中,rs表示预测模型的风险值(risk score,rs),f1~fn表示目标预测指标,α0表示常数,α1~αn分别表示与f1~fn一一对应的回归系数。
[0120]
在上述实施例的基础上,确定目标预测指标为影像组学评分和血清afp,基于目标预测指标,构建肝癌术后早期复发预测模型,具体如下:
[0121]
rs=1.3718
×
f1 0.4537
×
f2;
[0122]
其中,f1表示影像组学评分,f2表示血清afp(0:≤200ng/ml,1:》200ng/ml)。
[0123]
本发明提供的一种肝癌术后早期复发预测模型构建方法及装置,通过采用影像组学的方法,根据获取的多个对象的肝癌术前ct影像样本信息,确定各个对象的肝癌术前ct
影像样本信息的影像组学评分,结果显示基于增强ct影像学特征拟合得到的影像组学评分与早期复发呈正相关联关系,进一步通过对包括影像组学评分和多个预设临床病理指标的多个预测指标的样本信息,进行单因素和多因素cox回归的联合分析,确定与肝癌术后早期复发相关联的多个目标预测指标,并基于该目标预测指标构建肝癌术后早期复发预测模型,本发明的预测模型可以高效地对肝癌患者早期复发做出准确预测,极大地改善了肝癌术后患者的预后。
[0124]
在一些实施例中,在构建肝癌术后早期复发预测模型之后,还包括:
[0125]
基于肝癌术后早期复发预测模型,确定对应的列线图;
[0126]
基于所述列线图,确定肝癌术后早期复发的概率。
[0127]
具体地,本发明实施例所描述的列线图又称诺莫图(nomogram图),它是建立在多因素回归分析的基础上,将多个预测指标进行整合,然后采用带有刻度的线段,按照一定的比例绘制在同一平面上,从而用以表达预测模型中各个变量之间的相互关系。
[0128]
在本实施例中,基于多因素cox回归模型构建肝癌术后早期复发预测模型后,可以采用r软件包rms绘制模型对应的列线图。
[0129]
由此,通过列线图可以根据预测模型中各个目标预测指标对结局变量的贡献程度,即回归系数的大小,给每个目标预测指标的每个取值水平进行赋分,然后再将各个评分相加得到总评分,最后通过总评分与肝癌术后早期复发事件发生概率之间的函数转换关系,从而计算出该个体肝癌术后早期复发的预测值。
[0130]
图3是本发明实施例提供的肝癌术后早期复发预测模型的列线图示意图,如图3所示,基于影像组学评分和术前血清afp水平建立放射组学与临床结合模型,即肝癌术后早期复发预测模型,列线图中各指标综合的总分所对应的预测复发率,即为肝癌术后早期复发的预测值。
[0131]
本发明实施例的方法,通过列线图将肝癌术后早期复发预测模型,转变为了可视化的图形,使预测模型的结果更具有直观性和可读性。
[0132]
进一步地,对本发明预测模型进行roc分析评估,对训练集和验证集进行模型计算以及预测rfs的roc曲线。
[0133]
图4是本发明实施例提供的肝癌术后早期复发预测模型构建方法的计算结果显示示意图之二,如图4所示,图4中的a显示了预测训练集1-2年rfs的roc曲线,在训练集中1年和2年复发的auc分别为0.79(95ci%,0.73-0.84)和0.77(95ci%,0.70-0.83);
[0134]
图4中的b显示了预测验证集中1-2年rfs的roc曲线,在验证集中1年和2年复发的auc分别为0.65(95ci%,0.58-0.73)和0.74(95ci%,0.63-0.77);
[0135]
图4中的c和d分别显示了训练集和验证集中1-2年rfs的校准曲线,c和d中校准曲线都显示了预测模型预测结果和观测结果之间具有良好的一致性;
[0136]
图4中的e和f分别显示了预测模型分别在训练集和验证集中的决策曲线分析,结果显示在相同获益范围下,本发明的预测模型具有更高的净效益。
[0137]
在一些实施例中,为了进一步验证本发明预测模型的识别能力,基于训练集和验证集中的中位风险比率值,绘制rfs和os的生存曲线。
[0138]
图5是本发明实施例提供的肝癌术后早期复发预测模型构建方法的计算结果显示示意图之三,如图5所示,显示了肝癌早期复发的风险积累曲线和生存曲线,其中,图5中的a
为训练集中rfs的风险积累曲线;图5中的b为训练集中os的生存曲线;图5中的c为验证集中rfs的风险积累曲线;图5中的d为验证集中os的生存曲线;图5中的e和f为训练集和验证集中afp阴性组rfs的风险累积曲线;图5中的g和h为训练集和验证集中afp阳性组rfs的风险累积曲线。
[0139]
继续参照图5可知,如图5中的a和c,通过log-rank检验,无论在训练集还是在验证集中,高风险组的患者更有可能出现早期复发,其中,p《0.0001;如图5中的b和d,通过log-rank检验,高风险组和低风险组中总生存期具有显著差异,其中,训练集中p《0.0001,验证集中p=0.0109。
[0140]
在本发明的实施例中,还对afp阴性组和阳性组进行亚组分析,如图5中的e、f、g和h,可知,不管血清afp水平小于20ng/ml,还是大于等于20ng/ml,本发明预测模型计算的风险比率值与早期复发和总生存率密切相关联,其中,p《0.0001。
[0141]
综合上述结果分析可知,本发明的预测模型具有良好的分层效果。
[0142]
本发明的实施例的方法,基于对各个肝癌ct影像信息进行影像组学研究分析,分析结果显示由增强ct影像信息中影像组学特征拟合得到的影像组学评分与肝癌术后早期复发呈正相关联关系,并通过结合cox回归分析得到的目标预测指标血清afp,使得本发明预测模型的预测准确率得到进一步提升,预测模型在训练集和验证集中的roc曲线下auc分别为0.77和0.74,能够准确地预测肝癌术后的无复发生存期,决策曲线则体现出预测模型的临床获益情况,未来可能用于指导临床决策。
[0143]
肝癌的复发一直是临床的检点问题,此前已有学者从单细胞基因层面发现了原发和复发性肝癌基因表达模式的差异,给临床诊断和治疗带来了新的突破。但由于技术限制,此方法难以在大队列的肝癌患者上实施。
[0144]
因此,本发明实施例中通过结合影像组学的方法,可以无创对肝癌患者术前信息做出有效挖掘,提取得到高维度影像组学特征,并从中挖掘出与早期复发最相关联的目标影像组学特征,并拟合得出影像组学评分,然后结合血清afp构建肝癌术后早期复发预测模型,可以很好对肝癌患者早期复发做出准确预测;
[0145]
本发明的肝癌术后早期复发预测模型还可以对患者进行分层,从而识别出更倾向于发生早期复发的患者。而随着免疫检查点抑制剂和抗血管靶向药的获益,对于高风险患者,可预防性地进行用药以防止复发,为临床治疗提供了新的思路。
[0146]
综上所述,本发明构建的肝癌术后早期复发预测模型可以为现有的传统血清学模型进行很好的补充,是预测肝癌患者术后早期复发的有力工具。
[0147]
下面对本发明提供的肝癌术后早期复发预测模型构建装置进行描述,下文描述的肝癌术后早期复发预测模型构建装置与上文描述的肝癌术后早期复发预测模型构建方法可相互对应参照。
[0148]
图6是本发明实施例提供的肝癌术后早期复发预测模型构建装置的结构示意图,如图6所示,包括:
[0149]
第一处理模块601,用于基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,其中,所述多个预测指标包括影像组学评分和多个预设临床病理指标,所述影像组学评分是基于肝癌术前ct影像样本信息确定的;
[0150]
第一建模模块602,用于基于所述多个目标预测指标,构建肝癌术后早期复发预测
模型。
[0151]
本实施例所述的装置可以用于执行上述方法实施例,其原理和技术效果类似,此处不再赘述。
[0152]
图7是本发明实施例提供的电子设备的结构示意图,如图7所示,该电子设备可以包括:处理器(processor)710、通信接口(communications interface)720、存储器(memory)730和通信总线740,其中,处理器710,通信接口720,存储器730通过通信总线740完成相互间的通信。处理器710可以调用存储器730中的逻辑指令,以执行上述各方法所提供的肝癌术后早期复发预测模型构建方法,该方法包括:基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,其中,所述多个预测指标包括影像组学评分和多个预设临床病理指标,所述影像组学评分是基于肝癌术前ct影像样本信息确定的;基于所述多个目标预测指标,构建肝癌术后早期复发预测模型。
[0153]
此外,上述的存储器730中的逻辑指令可以通过软件功能单元的形式实现并作为独立的产品销售或使用,可以存储在一个计算机可读取存储介质中。基于这样的理解,本发明的技术方案本质上或者说对现有技术做出贡献的部分或者该技术方案的部分可以以软件产品的形式体现出来,该计算机软件产品存储在一个存储介质中,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)执行本发明各个实施例所述方法的全部或部分步骤。而前述的存储介质包括:u盘、移动硬盘、只读存储器(rom,read-only memory)、随机存取存储器(ram,random access memory)、磁碟或者光盘等各种可以存储程序代码的介质。
[0154]
另一方面,本发明还提供一种计算机程序产品,所述计算机程序产品包括计算机程序,计算机程序可存储在非暂态计算机可读存储介质上,所述计算机程序被处理器执行时,计算机能够执行上述各方法所提供的肝癌术后早期复发预测模型构建方法,该方法包括:基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,其中,所述多个预测指标包括影像组学评分和多个预设临床病理指标,所述影像组学评分是基于肝癌术前ct影像样本信息确定的;基于所述多个目标预测指标,构建肝癌术后早期复发预测模型。
[0155]
又一方面,本发明还提供一种非暂态计算机可读存储介质,其上存储有计算机程序,该计算机程序被处理器执行时实现以执行上述各方法所提供的肝癌术后早期复发预测模型构建方法,该方法包括:基于多个预测指标的样本信息,从所述多个预测指标中确定多个目标预测指标,其中,所述多个预测指标包括影像组学评分和多个预设临床病理指标,所述影像组学评分是基于肝癌术前ct影像样本信息确定的;基于所述多个目标预测指标,构建肝癌术后早期复发预测模型。
[0156]
以上所描述的装置实施例仅仅是示意性的,其中所述作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部模块来实现本实施例方案的目的。本领域普通技术人员在不付出创造性的劳动的情况下,即可以理解并实施。
[0157]
通过以上的实施方式的描述,本领域的技术人员可以清楚地了解到各实施方式可借助软件加必需的通用硬件平台的方式来实现,当然也可以通过硬件。基于这样的理解,上
述技术方案本质上或者说对现有技术做出贡献的部分可以以软件产品的形式体现出来,该计算机软件产品可以存储在计算机可读存储介质中,如rom/ram、磁碟、光盘等,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)执行各个实施例或者实施例的某些部分所述的方法。
[0158]
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。