1.本发明属于医药领域,具体涉及双黄酮类化合物和苯甲酮类化合物的药物组合物,尤其是大叶藤黄种子提取物(双黄酮类化合物和苯甲酮类化合物含量较高)在制备抗肿瘤药物中应用,以及所述提取物的制备方法。
背景技术:
2.大叶藤黄(garcinia xanthochymus hook. f. ex t. anderson)为藤黄科(clusiaceae)藤黄属的多年生常绿乔木植物,自然分布于我国云南和广西地区,在东南亚也有分布,如缅甸和泰国。该植物在我国民间具有多种传统用途,包括食用、药用、观赏和文化价值等。传统上,其成熟的果实可以直接食用或用于饮品制作,果汁可以作为鱼酱,嫩叶可以当野菜食用。作为传统的傣药之一,大叶藤黄的茎和叶部位的汁液内服可以驱虫,外用可驱使蚂蟥退出鼻腔。此外,根据民族植物学调查发现,其树皮能用于治疗痢疾、胃痛,果实具有清热解毒的功效。
3.现代药理学研究表明,大叶藤黄植物的不同部位,如树皮和叶的提取物或单体化合物具有多种生物活性,例如抗氧化、抗糖尿病、抗炎、抗菌、抗肿瘤等,活性化合物主要包括
ி
酮类、黄酮类和苯甲酮类化合物,因此该植物在药理学、食品等领域具备较大开发潜力。
4.虽然大叶藤黄具有多种利用价值和较好的生物活性,但是关注度较低,我国对该植物资源的保护、开发和利用仍然十分匮乏。目前,该植物仍处于野生状态,且随着现代化进程的推进,人们对大叶藤黄的传统利用迅速减少,如一些在医药方面的利用已难觅其踪迹。更为紧要的是该植物的生存也受到多方面因素的威胁,例如城市化建设、经济作物开发和保护意识薄弱等,由于经济发展的需要而砍伐该植物的现象时有发生,其资源分布量呈现逐年减少趋势,因此对该植物资源的保护亟待开展。对植物资源价值的深度挖掘及可持续利用,是促进植物资源及生物多样性保护的有效路径之一。
5.癌症(恶性肿瘤)是威胁人类生命健康的主要疾病之一,世界范围内每年有数百万人因此病而死亡。近些年,由于环境污染、人口老龄化、不良生活习惯等因素,癌症的发病率不断攀升,一些药物对肿瘤细胞虽具有较好的治疗效果,但肿瘤细胞易产生耐药性,从而导致药效降低,因此寻找高效的抗肿瘤药仍然十分迫切。
6.目前关于大叶藤黄种子部位的抗肿瘤细胞的生物活性研究或相关专利仍然未见报道,也未见大叶藤黄种子相关专利的公开。
技术实现要素:
7.本发明为充分挖掘大叶藤黄种子的价值,服务人类健康产业,提供了一种对肿瘤细胞具有显著抑制活性的提取物及其制备方法。一方面,本发明提供的提取物对3种肿瘤细胞(包括肺癌细胞a549,宫颈癌细胞hela和胃癌细胞hgc-27)具有极为显著抑制活性,显著高于阳性对照(顺铂),化学成分研究表明大叶藤黄种子中具有多种活性成分,例如双黄酮
类和苯甲酮类化合物,因此有望进一步开发为抗肿瘤剂。同时,本发明提供的提取物制备方法操作极为简便,对仪器设备要求低,生产成本低,有利于大规模生产制备。
8.本发明因此提供一种具有抗肿瘤活性的组合物,其特征在于,其包括下式所示化合物为活性成分:式1
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
式2式3
ꢀꢀꢀꢀꢀꢀꢀꢀ
式4式5式6式7。
9.优选地,各化合物的重量配比为式1:式2:式3:式4:式5:式6:式7=30-40:20-30:5-15:4-12:3-11:20-30:4-12。任选地,还包括其他药学上可接受的辅料等其他成分。
10.本发明尤其提供一种具有抗肿瘤活性的大叶藤黄种子提取物的制备方法,包括以下步骤:(1)种子去皮:取新鲜成熟果实,获取种子后去皮,并破碎成块;(2)种子碎块的干燥:将种子碎块置于真空冷冻干燥机中,进行冻干处理;(3)种子碎块的粉碎:将干燥后的种子碎块进行粉碎,过筛后得到种子粉末备用;(4)超声辅助提取:称量干燥的种子粉末,加入有机溶剂混匀,随后超声辅助提取,离心取上清液;(5)过滤:将上清液用聚四氟乙烯膜过滤,得到滤液;(6)减压浓缩:对得到的滤液进行减压浓缩,获得干燥的大叶藤黄种子提取物。
11.在优选实施方式中,第(1)步中的种子是取新鲜成熟果实。更优选地,第(1)步的具体操作如下:将采摘的新鲜成熟果实用清水冲洗干净,然后切开,将种子取出,种子表面用蒸馏水清洗除去残留汁液,随后除去种皮,得到去皮的种子,将种子破成碎块,置于干净的托盘中。
12.在具体实施方式中,第(2)步的具体干燥条件为:温度为-60至-80℃,真空压力小于 0.140 mbar,干燥时间为36-64h;更优选地,温度-80℃,真空压力小于 0.140 mbar,干燥时间为48h。
13.在优选实施方式中,第(3)步中采用电动粉碎机,过40目筛后得到种子粉末,将粉末放置于阴凉干燥处。
14.在一个具体实施方式中,第(4)步中的有机溶剂是甲醇、乙醇、丙酮或乙酸乙酯。更优选地,第(4)步中的有机溶剂是80%的甲醇;所混匀是涡旋混匀30-90秒钟。
15.在另一个具体实施方式中,第(4)步中的超声辅助提取时间为15-30分钟,具体操作条件是:频率为20-50 khz,功率为50-500 w,并确保温度不超过40℃。
16.在一个优选实施方式中,第(4)步中的超声辅助提取重复2-4次,超声频率为20 khz,功率为200 w,合并上清液;离心以转速3500-4500rpm进行3-8分钟。
17.在一个具体实施方式中,第(5)步中是用孔径为0.45/0.22μm的聚四氟乙烯膜或尼龙膜过滤,或用孔径为10-25 μm的滤纸过滤;在一个具体实施方式中,第(6)步中采用旋转蒸发仪进行于30-45℃条件进行减压浓缩,真空度为8-600 mbar。更优选地,第(4)步中的旋转蒸发仪温度为38℃,减压真空度为8-200 mbar.任选地,还包括将得到大叶藤黄种子提取物于-20℃封口储存的步骤。
18.本发明由此提供所述的制备方法得到的具有抗肿瘤活性的大叶藤黄种子提取物。
19.尤其提供所述的具有抗肿瘤活性的大叶藤黄种子提取物在制备抗肿瘤药剂中的用途。优选地,所述肿瘤是肺癌、宫颈癌或胃癌。
20.本发明提供了一种具有显著抗肿瘤活性的大叶藤黄种子提取物及其制备方法,能够为抗肿瘤剂的开发提供天然来源,服务人类的健康产业,也能够使种子“变废为宝”,进一步挖掘该植物的价值,进而促进该植物的保护和可持续利用。同时,本发明对仪器设备要求低,所用设备均为常见仪器,购买容易且配置费用低,操作方法也极为简易,一般技术人员均能熟练掌握所用仪器的操作。其中,提取溶剂为80%甲醇,甲醇为十分常用的有机溶剂,价格低,污染小,对人体毒性小,且沸点低,可重复回收利用,极大降低制备成本;且采用超声辅助提取的方法,不仅经济环保,还能够缩短提取时间,提高提取率。利用冻干机在低温真空的环境下对种子进行干燥,可避免高温对提取物成分产生的影响,为活性实验提供稳定、可重复获得的提取物。本发明还对提取物的化学成分进行了分离和结构鉴定,结果表明其中含有多种活性成分,为阐明其抗肿瘤活性奠定了物质基础。
21.同时,本发明旨在采收大叶藤黄的种子以获得其种子提取物,在今后的开发利用过程中必然加大该植物的人工繁殖力度和大面积栽培,从而减轻对野生居群的压力,十分有利于保护该物种。此外,作为我国藤黄属植物的典型代表,其价值开发也可为其他藤黄属或其他属植物的可持续利用和保护提供参考。
附图说明
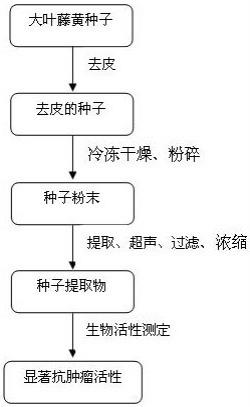
22.图1 大叶藤黄种子提取物的制备方法示意图。
具体实施方式
23.下面通过具体实施例对本发明进行阐述以期对本发明有更好的理解,但并对本发明构成限制。
24.实施例一:提取物的制备实施例一种具有抗肿瘤活性的大叶藤黄种子提取物的制备方法(图1),包括以下详细步骤:(1)种子去皮:将采摘的新鲜成熟果实用清水冲洗干净,然后切开,将种子取出,种子表面用蒸馏水清洗除去残留汁液,随后除去种皮,得到去皮的种子,将种子破成碎块,置
于干净的托盘中。
25.(2)干燥、粉碎:将种子碎块置于真空冷冻干燥机中,进行冻干处理,干燥条件为:温度为-80℃,真空压力小于 0.140 mbar,干燥时间为48h。将干燥后的种子碎块,用电动粉碎机进行粉碎,过40目筛后得到种子粉末,将粉末放置于阴凉干燥处。
26.(3)提取、干燥:称量2.0 g干燥的种子粉末,置于50 ml的离心管中,加入30 ml 80%的甲醇溶液,涡旋混匀1 min,随后超声辅助提取20 min(温度不超过40℃,超声频率为20 khz,功率为200 w),于4000 rpm转速下进行离心5 min,将上清液转移到100 ml三角瓶中,重复该步骤三次。将上清液合并后用孔径为0.45 μm的聚四氟乙烯膜过滤,得到的滤液用旋转蒸发仪在38℃、真空度为8-200 mbar的减压条件下浓缩,获得干燥的大叶藤黄种子提取物,即为本发明的大叶藤黄种子提取物,于-20℃封口储存。
27.其中,采自广西壮族自治区那坡县德隆乡德康村的大叶藤黄种子,按以上步骤制备获得提取物,为简便起见编码为提取物1;采自广西壮族自治区那坡县百合乡清华村的大叶藤黄种子,按以上步骤制备获得提取物,编码为提取物2;采自云南省西双版纳傣族自治州景洪市基诺山亚诺村的大叶藤黄种子,按以上步骤制备获得提取物,编码为提取物3。
28.实施例二:提取物的活性验证实施例以下是根据本发明获得的大叶藤黄种子提取物的体外抗肿瘤细胞实验。
29.采用cck8法测定上述实施例一中得到的大叶藤黄种子提取物对3种肿瘤细胞,包括肺癌细胞a549,宫颈癌细胞hela和胃癌细胞hgc-27的生长抑制活性,具体包括以下步骤:(1)细胞复苏:从-80℃冰箱中取出冻存的肿瘤细胞,每种肿瘤细胞各取一管,用冰盒迅速转移至细胞间,将冻存管置于37℃的水浴锅中,使细胞融化。在超净工作台中,将融化的细胞转移到50 ml的离心管中,加入10 mldme/f-12完全培养液(含10%的胎牛血清和1%的双抗),1000 rpm离心5min,弃去上清,重复三次该步骤,再加入5mldme/f-12完全培养液吹打成单细胞,转移至培养瓶后置于培养箱(37℃,5%co2)中进行培养。
30.(2)细胞传代:当肿瘤细胞生长密度为80%左右时,将细胞浓度调整为1
×
105个/ml,转移至新的培养瓶中,将传代3次后的细胞用于实验。
31.(3)细胞种板:用dme/f-12完全培养液配置浓度为5
×
10
4 个/ml的单细胞悬液,将单细胞悬液接种于96孔板中,每孔加入100 μl,于培养箱中培养24 h。
32.(4)添加提取物:提取物先用dmso溶解配置100 mg/ml的母液,然后用dme/f-12培养液稀释成1mg/ml的溶液,再进行稀释得到一系列不同浓度的提取物溶液,浓度范围在0.625-12.5 μg/ml。将96孔板上清液吸出后,加入100 μl不同浓度的提取物溶液,最高浓度下dmso的含量低于0.13
‰
,将临床常用的抗肿瘤药物顺铂作为阳性对照,不含提取物的dme/f-12培养液作为空白对照,每个处理五个重复。
33.(5)吸光值测定:将培养48 h的96孔板取出,吸走上清液,每孔加入10%的cck8溶液100 μl,在培养箱中孵育1-2 h,用酶标仪测450 nm下的吸光值。
34.(6)ic
50
测定:根据以下公式计算提取物对肿瘤细胞生长的抑制率:其中as表示提取物或阳性对照处理的吸光值,a
c1
表示空白对照的吸光值,a
c2
表示10%的cck8溶液本身的吸光值。将各浓度提取物得到的抑制率数值用graphadprsm软件计算
ic
50
值,即能够抑制50%肿瘤细胞生长的浓度,再用spss软件的单因素anova和turkey多重分析进行具有统计学意义的差异性分析。
35.实验结果如表1所示。
36.表1实施例一制备的提取物对肿瘤细胞的抑制活性注:上标字母代表各提取物和阳性对照对同一肿瘤细胞抑制活性ic
50
值的显著性差异分析结果,含相同字母代表无显著性差异,反之则说明有显著性差异,p<0.05。
37.表1中的结果表明,按照实施例一得到的提取物对3种肿瘤细胞,肺癌细胞a549、宫颈癌细胞hela和胃癌细胞hgc-27均具有极为显著的抑制活性。实施例一所得的三种提取物的抗肿瘤活性的ic
50
值之间没有显著差异,说明本发明的技术方案对不同地点采集到的大藤黄种子均有效,适用性广。实验采用顺铂作为阳性对照,该化合物是目前临床用于抗肿瘤治疗最常用的药物之一,显著性分析结果表明,本发明获得的所有提取物的ic
50
值均显著低于顺铂(p《0.05),表明本发明提取物对测试肿瘤细胞生长的抑制活性更为有效,进一步证实了本发明得到的提取物具有显著的抗肿瘤活性,极具开发潜力和应用前景。
38.实施例三:提取物的化学成分分析取实施例一制备得到的总提取物200 g,加入适量蒸馏水进行混悬,然后加入石油醚除去种子油,再加入乙酸乙酯进行萃取,萃取液浓缩至干后得到乙酸乙酯层浸膏63.3g。对乙酸乙酯层浸膏进行硅胶柱层析,二氯甲烷/甲醇(100:0~0:100, v/v)进行梯度洗脱,得到5个主要组分。分别经反复硅胶、葡聚糖凝胶(sephadex lh-20)柱层析进行纯化,硅胶柱层析采用二氯甲烷和甲醇溶剂体系进行梯度洗脱,sephadex lh-20柱层析则采用二氯甲烷/甲醇(1:1, v/v)作为流动相进行等度洗脱,得到的主要组分经循环制备液相色谱仪或全制备高效液相色谱仪进一步制备纯化得到7个主要化学成分,最后通过波谱数据分析,包括一维或二维核磁共振和高分辨质谱分析对化合物的结构进行鉴定,得到3个双黄酮类化合物:藤黄双黄酮(morelloflavone,结构如式1所示)35.6 mg、倭氏藤黄双黄酮(volkensiflavone,结构如式2所示)25.1 mg、阿曼托黄酮(amentoflavone,结构如式3所示)11.7 mg,2个多异戊烯基取代的苯甲酮类化合物:异大叶藤黄醇(isoxanthochymol,结构如式4所示)8.5 mg、gambogenone(结构如式5所示)(7.8 mg),以及2个苯的简单衍生物:2,4-二叔丁基硝基苯(2,4-ditert-butyl-1-nitrobenzene,结构如式6所示)24.7 mg、3-甲氧基-4-羟基苯乙二醇(3-methoxy-4-hydroxyphenyl glycol,结构如式7所示)8.1 mg。
39.经文献查阅可知,分离得到的化合物包括藤黄双黄酮、倭氏藤黄双黄酮、阿曼托黄酮、异大叶藤黄醇和gambogenone对多种肿瘤细胞具有显著的抑制活性,例如异大叶藤黄醇能够显著抑制肺癌细胞a549和宫颈癌细胞hela的生长,ic
50
值分别为13.99
±
0.09 和10.18
±
0.51μm,阳性对照顺铂的ic
50
值为19和18μm。因此这些活性成分为阐明本发明提取物的抗肿瘤药效奠定了化学物质基础。
40.式1
ꢀꢀꢀꢀꢀꢀ
式2式3
ꢀꢀꢀꢀꢀꢀꢀ
式4式5式6式7。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。