1.本发明涉及生物医药领域。更具体地说,本发明涉及骨质疏松症的生物标志物、检测所述生物标志物的检测试剂盒及其应用。
背景技术:
2.骨质疏松症是一种慢性疾病,其特征是骨密度(bmd)降低、微结构结构恶化和骨骼脆弱。随着人们寿命的延长,骨质疏松症正在成为一种全球性的流行病。全球有2亿多人患有骨质疏松症。低骨密度是骨折的一个很强的危险因素,骨密度的每一个低标准差(sd)都与骨折的风险加倍有关。在50岁以上的女性中,三分之一的女性和五分之一的男性将发生骨质疏松性骨折,这通常会导致依赖性生活状况和过早死亡。低骨密度和骨质疏松症是没有明显症状的,换言之,不进行检测或者不出现诸如骨折等严重的状况,患者是不容易知晓自身情况的。因此,治疗的受益风险比是非常有希望的,并且建议在65岁或65岁左右进行骨密度测量。目前骨密度测量的金标准是双能x射线吸收测量(dxa)扫描。然而,骨密度测量往往比较复杂,对仪器场地和操作人员的要求较高,无法实现高通量的测试。
3.血液生物标志物在临床上用于反映不同的骨代谢过程。例如,i型胶原的c末端端肽(ctx-i)表示旧骨的吸收,i型前胶原的n末端端肽(pinp)表示新骨的形成,可用于监测治疗后的骨反应。然而,这些可用的生物标记物不可靠,不能提高对骨丢失或骨折的预测,不建议用于临床诊断。
4.代谢组学是一个创新和高通量生物分析方法,旨在对存在于任何生物系统或任何特定生理状态的小分子(分子量小于1500道尔顿)进行鉴定和定量。在过去十年中,两个主要的分析技术,核磁共振(nmr)和质谱(ms),在测量内源性化合物的应用中呈指数式的增长。自2005年以来,基于ms技术有了长足的发展,并因比nmr具有以下优势使得其得到更频繁地使用:灵敏度更高;代谢组覆盖度更高;代谢物鉴定和辨别能力更高;以及组分-分类-特异分析的模块化(griffiths,w.j.et al.targeted metabolomics for biomarker discovery.angew.chem.int.ed.49,5426
–
5445(2010),通过引用并入本文)。ms主要与色谱方法如液相色谱质谱(lc-ms)结合使用。
5.人体的系统代谢状态是骨骼健康的决定因素,为骨质疏松症的早期诊断和骨质疏松性骨折的预防,迫切需要寻找新的血液生物标志物。然而,目前骨质疏松症的代谢组学研究还有许多不足。
6.本领域迫切需要对骨相关代谢组学,尤其是骨质疏松生物标志物进行进一步的研究,以期发现新的骨质疏松症的生物标志物,从而能够对临床风险因素进行更全面的评估。
技术实现要素:
7.本发明的目的在于提供用于骨质疏松症诊断的生物标志物;这种生物标志物能够简单、准确地检测骨质疏松症。
8.本发明的另一目的在于提供通过检测所述生物标志物来诊断骨质疏松症的检测
或诊断试剂盒。
9.本发明的还有一目的在于提供利用所述生物标志物或所述检测或诊断试剂盒来诊断骨质疏松症的方法。
10.在第一方面,本发明提供一种检测或诊断待测对象的骨质疏松症或评估待测对象的骨质疏松患病风险的生物标志物,所述生物标志物是选自下组的任一生物标志物或它们的组合:肌苷、次黄嘌呤。
11.在具体的实施方式中,所述生物标志物是肌苷和次黄嘌呤的组合。
12.在第二方面,本发明提供第一方面所述的生物标志物在制备检测或诊断待测对象的骨质疏松症或评估待测对象的骨质疏松患病风险的检测试剂或检测试剂盒中的用途。
13.在第三方面,本发明提供一种检测第一方面所述生物标志物的检测试剂。
14.在具体的实施方式中,所述检测试剂用于检测或诊断待测对象的骨质疏松症或评估待测对象的骨质疏松患病风险。
15.在第四方面,本发明提供一种检测试剂盒,所述检测试剂盒中包含检测第一方面所述生物标志物的检测试剂。
16.在第五方面,本发明提供一种筛选具有骨质疏松症治疗活性的药物的方法,所述方法包括以下步骤:
17.1)检测具有骨质疏松症的对象的血液、血清或血浆中第一方面所述的生物标志物水平;
18.2)将待测药物给予所述对象;
19.3)检测给药后所述对象的血液、血清或血浆中第一方面所述的生物标志物水平;
20.4)比较步骤1)和3)得到的生物标志物水平,如果步骤3)所得生物标志物水平低于步骤1)所得的生物标志物水平,则将所述待测药物判定为具有骨质疏松症治疗活性的药物。
21.在第六方面,本发明提供一种评估待测对象的骨质疏松患病风险或待测对象骨质疏松诊断的方法,所述方法包括步骤:
22.1)提供来源于待测对象的血液、血清或血浆样品,并检测样品中第一方面所述的生物标志物水平;
23.2)将步骤1)测得的生物标志物水平与参考数据集或参考值(如健康对照者的参考值)进行比较;
24.如果步骤1)测得的生物标志物水平高于该参考值,则判定该对象具有骨质疏松患病风险或诊断该对象患有骨质疏松症。
25.在具体的实施方式中,所述参考数据集包括来源于骨质疏松患者和健康对照的第一方面所述的生物标记物的水平。
26.应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
27.图1示出了30例健康对照和30例骨质疏松患者的opls-da得分图。图中每个点代表
一个样品,其中黑色菱形点代表测试样。opls-da的pc1(41.26%)、pc2(14.73%)表明,骨质疏松患者和健康对照的血浆样品的代谢谱存在明显差异;
28.图2示出了5000余个代谢产分子离子峰检测值的载荷图。图中的黑色三角状点代表各样品的分子离子峰值;红色菱形点分别代表正常人群和骨质疏松人群。距离中心点越远的表明健康人群和骨质疏松人群的潜在差异代谢产物;
29.图3示出了opls模型的5000余个代谢产分子离子峰检测值的s散点载荷图。图中的黑色三角状点代表各样品的分子离子峰值。右上区间和左下区间的散点分别代表相对比于正常人群,骨质疏松患者中潜在差异代谢产物的分子离子峰;
30.图4示出了利用图3筛选出的有差异的100个分子离子峰(q值<0.05,vip>1.2,fc>1.2或fc<0.8)的热图。绿色表示在骨质疏松患者中降低,红色表示在骨质疏松患者中升高;
31.图5示出了已鉴定的6种潜在生物标志物用于鉴别低骨密度和正常骨密度roc曲线。其中次黄嘌呤和肌苷auc分别为0.914和0.686。
具体实施方式
32.发明人经过广泛而深入的研究,出乎意料地发现多个可用于骨质疏松症诊断的血液生物标志物,利用这些生物标志物可以高灵敏性、高特异性地评估待测对象的骨质疏松症风险,从而能够骨质疏松症的诊断并具有重要的应用价值。在此基础上完成了本发明。
33.术语
34.本文所用的术语的含义与本领域技术人员常规理解的相同或相似。为了更好地理解本发明,对一些术语定义如下。但需要说明的是,在此提供术语的解释仅为了使本领域技术人员更好地理解本发明,并非对本发明限制。
35.骨质疏松症
36.本文所用的术语“骨质疏松症”或“骨质疏松”具有相同的含义,是指多种原因引起的一组骨病。对于该疾病,骨组织有正常的钙化,钙盐与基质呈正常比例,以单位体积内骨组织量减少为特点的代谢性骨病变。在本领域,骨质疏松的诊断通过双能x射线吸收测量(dxa)扫描。
37.生物标志物
38.本文所用的术语“生物标志物”,也称为“生物学标志物”,是指个体的生物状态的可测量指标。这样的生物标记物可以是在个体中的任何物质,只要它们与被检个体的特定生物状态(例如,疾病)有关系,例如,核酸标志物(例如dna),蛋白质标志物,细胞因子标记物,趋化因子标记物,碳水化合物标志物,抗原标志物,抗体标志物,物种标志物(种/属的标记)和功能标志物(ko/og标记)等。生物标记物经过测量和评估,经常用以检查正常生物过程,致病过程,或治疗干预药理响应,而且在许多科学领域都是有用的。
39.本发明人利用取自骨质疏松患者、骨量偏低者与正常人各30人。根据骨密度测量结果,将受试者分为:正常骨密度(t评分<-1)和低骨密度,其中低骨密度包括骨质减少(2.5<t评分<-1)和骨质疏松(t评分<-2.5)。我们使用基于代谢组学的综合液相色谱-质谱法作血液非靶标代谢物分析。共90个血液试剂进行了预备实验。在本研究鉴定的代谢物中,肌苷和次黄嘌呤与低骨密度(fdr q值<0.05)相关,从而得以确认这些代谢产物具有作为骨质疏松血液生物标志物的可能性,把上述2种骨质疏松血液生物标志物组合后通过多元统计分
析法(mva)对骨质疏松诊断能力进行评估时,发现这些标志物的诊断能力得到了提升。具体地说把2种血液生物标志物组合后适用弹性网回归分析法(elastic net regression)对骨吸收的经典危险因素和血浆生物标志物的预测模型进行预测,极大地提高了低骨密度的预测性能(aucs:0.782vs.0.698,p0.002)。
40.本发明的检测方法能够把血液中的骨质疏松血液生物标志物肌苷和次黄嘌呤全部予以检测,这些检测值则由医师之类的医疗专家用来判断骨质疏松罹患与否、骨质疏松发展程度及/或骨质疏松治疗经过。
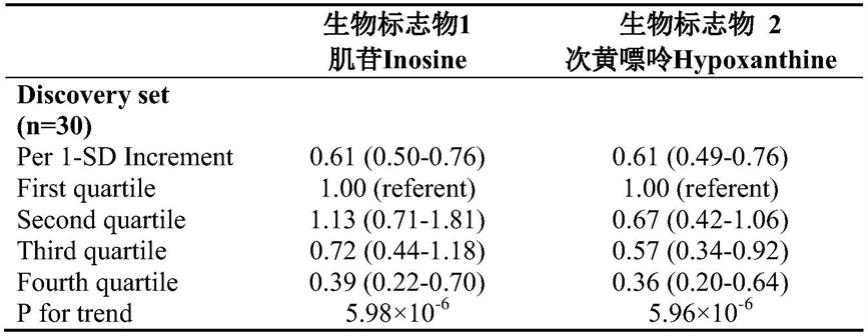
41.表1.低骨密度代谢标志物的发现
[0042][0043]
在本发明中,提供用于检测或诊断待测对象的骨质疏松症或评估待测对象的骨质疏松患病风险的生物标志物,所述生物标志物是肌苷或次黄嘌呤。在优选的实施方式中,本发明的生物标志物是肌苷和次黄嘌呤的组合。
[0044]
肌苷,又称次黄嘌呤或肌苷,分子式为c
10
h
12
n4o5,分子量为268.0808,属于嘌呤核苷类有机化合物。嘌呤核苷是由连接到核糖或脱氧核糖基的嘌呤碱组成的化合物。肌苷是一种中等碱性的化合物(基于pka)。肌苷存在于从细菌到人类的所有生物中。在人类体内,肌苷参与许多酶促反应。特别是,肌苷可以通过与胞浆嘌呤5
’-
核苷酸酶的相互作用从肌苷酸生物合成。此外,肌苷可以通过与嘌呤核苷磷酸化酶的相互作用,转化为次黄嘌呤和核糖1-磷酸。肌苷,就人类而言,被发现与一些疾病有关,如溃疡性结肠炎、退行性椎间盘疾病、肾脏疾病和痛风。肌苷是一种嘌呤核苷,它的次黄嘌呤由n9氮连接到核糖的c1碳。它是嘌呤和嘌呤核苷降解为尿酸和嘌呤回收途径的中间产物。它也存在于某些转移rna分子的反密码子中(dorland,第28版)。肌苷与嘌呤核苷磷酸化酶缺乏和i型黄嘌呤有关,后者是先天性代谢错误。
[0045]
次黄嘌呤,又称嘌呤-6-醇或hyp,分子式为c5h4n4o,分子量为136.038,属于被称为次黄嘌呤的一类有机化合物。次黄嘌呤是含有嘌呤衍生物1h-嘌呤-6(9h)-酮的化合物。嘌呤是一种双环芳香化合物,由嘧啶环和咪唑环熔融而成。次黄嘌呤是一种天然的嘌呤衍生物,是腺苷代谢和通过补救途径形成核酸的反应中间体。次黄嘌呤是一种中等碱性化合物(基于其pka)。次黄嘌呤存在于从细菌到人类的所有生物中。在正常情况下,次黄嘌呤很容易转化为尿酸。在人类体内,次黄嘌呤参与许多酶促反应。尤其是次黄嘌呤和1-磷酸核糖可以由肌苷与嘌呤核苷磷酸化酶相互作用合成。此外,次黄嘌呤鸟嘌呤磷酸核糖基转移酶可以通过肌苷酸生物合成次黄嘌呤和焦磷酸磷酸核糖基。在人类中,次黄嘌呤参与了被称为嘌呤核苷磷酸化酶缺乏途径的代谢紊乱。肺部和胸壁之间的积液(胸腔积液)也可能导致呼
吸急促。在人体外,次黄嘌呤平均在牛奶(奶牛)中的浓度最高。次黄嘌呤也被检测到,但没有在几种不同的食物中定量,如萝卜、山药、大葱、绿线茶和普通甜菜。这可能使次黄嘌呤成为食用这些食品的潜在生物标志物。次黄嘌呤是一种潜在的有毒化合物。摄入:引起呕吐。次黄嘌呤也是腺嘌呤的自发脱氨产物。
[0046]
在本发明的生物标志物的基础上,本发明还提供于检测或诊断待测对象的骨质疏松症或评估待测对象的骨质疏松患病风险的检测试剂或检测试剂盒。
[0047]
在进一步的实施方式中,本发明还提供筛选具有骨质疏松症治疗活性的药物的方法,所述方法包括在待测药物给药前后,检测具有骨质疏松症的对象的血液、血清或血浆中本发明的生物标志物水平;如果给药后的生物标志物水平低于给药前的生物标志物水平,则将所述待测药物判定为具有骨质疏松症治疗活性的药物。
[0048]
在进一步的实施方式中,本发明还提供评估待测对象的骨质疏松患病风险或待测对象骨质疏松诊断的方法,所述方法包括检测来源于待测对象的血液、血清或血浆样品中本发明的生物标志物水平;并将测得的生物标志物水平与参考数据集或参考值(如健康对照者的参考值)进行比较;如果测得的生物标志物水平高于该参考值,则判定该对象具有骨质疏松患病风险或诊断该对象患有骨质疏松症。在具体的实施方式中,所述参考数据集包括来源于骨质疏松患者和健康对照的本发明的生物标记物水平。
[0049]
质谱
[0050]
在本发明中,可采用质谱(ms)技术检测本发明的生物标志物。质谱可以分为离子阱质谱、四极杆质谱、轨道阱质谱和飞行时间质谱,偏差分别为0.2amu、0.4amu、3ppm和5ppm。在本发明中,利用轨道阱质谱获得ms数据。在本发明中,生物标志物质的水平通过ms峰强度指示。
[0051]
根据本发明,由现有技术已知,质荷比(m/z)和保留时间(rt)具有相同的含义。在本发明中,m/z单位为amu,这是指原子质量单位,也命名为道尔顿。道尔顿表示物质在原子或分子级(原子质量)的标准单位。一个统一的原子质量单位相当于1克/摩尔。它的定义为:碳-12原子质量的十二分之一。本发明对代谢物鉴定时的允许质量分辨率(误差)为10ppm,ppm即百万分之一。例如,某代谢物a同位素准确质量=118da,仪器测量的质量=118.001da;偏差=0.001amu;误差[偏差/准确质量
×
106]=8.47ppm。
[0052]
本领域的技术人员应当清楚:m/z和保留时间的值在使用不同的检测方法或lc-ms仪器时会有一定范围的波动。例如,m/z可以在
±
3.00,或
±
2.00,或
±
1.00的范围内波动;保留时间可以在
±
60秒,或
±
45秒,或
±
30秒,或
±
15秒的范围内波动。
[0053]
本文所用的术语“参考集”是指训练集。
[0054]
根据本发明,由现有技术可知,训练集和验证集具有相同的含义。在本发明的一个实施方式中,训练集指骨质疏松患者和健康对照生物样品中的生物标志物水平的集。在本发明的一个实施方式中,验证集是指用于测试训练集性能的数据集。在本发明的一个实施方式中,生物标志物的水平可以根据测定的方法代表为绝对值或相对值。例如,当用质谱来测定生物标记物的水平时,峰的强度可以代表生物标记物水平,这是一个相对值的水平;当用pcr来测定生物标志物的水平时,基因的拷贝数或基因片段的拷贝数可以代表的生物标志物的水平。
[0055]
在本发明的一个实施方式中,参照值是指健康对照的参考值或正常值。本领域的
技术人员清楚,在样品数量足够多情况下,每个生物标记的正常值(绝对值)的范围可以通过检验和计算方法得到。因此,当利用除质谱以外的其他方法来检测生物标志物的水平时,这些生物标记物水平的绝对值,可以直接与正常值比较,从而评价患有骨质疏松的风险,以及诊断或早期诊断骨质疏松。任选地,还可以使用统计方法。
[0056]
本文所用的术语“个体”指动物,特别是哺乳动物,如灵长类动物,最好是人。
[0057]
本文所用的术语“血浆”指的是全血的液体成分。根据所使用的分离方法,血浆可能完全不含细胞成分,也可能含有不同量的血小板和/或少量其它细胞成分。
[0058]
本文所用的术语如“一”、“这”和“该”不仅指单数的个体,而是包括可以用来说明特定实施方式的通常的一类。
[0059]
本发明的优点:
[0060]
1.本发明以血浆代谢物作为生物标志物用于骨质疏松的早期筛查、预判、防治,具有高灵敏性、高特异性的优点,具有重要的应用价值;
[0061]
2.血浆作为生物标志物检测样本具有取材方便、操作步骤简单和可连续体外检测等优点;
[0062]
3.本发明的生物标志物用于骨质疏松的早期筛查、预判、防治具有重复性好的特点。
[0063]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
[0064]
实施例
[0065]
1.材料与方法
[0066]
1.1样品收集
[0067]
从罗店医院招募90位志愿者。其中,30位为经双能x射线吸收测量(dxa)扫描确诊为骨质疏松患者,30名为经双能x射线吸收测量(dxa)扫描的骨密度低者,其他30位为健康对照。利用通过vacuette edta血液收集管收集志愿者血液样品,并于以4℃下,14000g离心10分钟,得到血浆样品,保存于-80℃备用。(志愿者的录入标准如下),本实验得到了罗店医院伦理审查委员会批准。并且样品收集前,得到了所有志愿者的书面同意。
[0068]
2015年3月至2018年11月,志愿者受邀参加我们的研究。排除标准包括:
[0069]
1)未满18岁的受试者;
[0070]
2)有影响骨代谢或钙吸收的疾病,如骨折、内分泌系统疾病(包括糖尿病和甲状腺疾病)、血液系统疾病(包括白血病和骨髓瘤)、系统性红斑狼疮或肾脏病;
[0071]
3)在研究前三个月内接受可能影响骨密度的药物或治疗的患者,如糖皮质激素和免疫抑制剂。每位参与者均获得书面知情同意。共有90名受试者接受了dxa扫描测量脊柱或髋部骨密度,并在dxa扫描后两天内捐献了血样。这项研究得到了每个中心道德委员会的批准,并符合1975年赫尔辛基宣言的道德准则。
[0072]
人口统计学数据由受过训练的护士收集。用轻便衣服测量体重和身高。体重指数(bmi)计算为体重(千克)除以身高(米)的平方。腰椎(l1到l4)或髋部的骨密度通过dxa扫描(ge lunar,madison,wi,usa)在每个中心进行测量。所有的骨密度测量都是由训练有素的技术人员使用标准化方案进行的。使用脊柱模型进行每日质量控制扫描。通过与同性健康
青年的骨密度比较,计算脊柱和髋部的骨密度t值。根据世界卫生组织骨质疏松症标准,t-1及以上定义为正常骨密度,t-1至-2.5表示骨质疏松,t-2.5及以下表示骨质疏松。在发现集中,大多数参与者(90%)只有脊椎骨密度扫描,而复制集中的所有参与者只有脊椎骨密度扫描。
[0073]
1.2材料与试剂
[0074]
hplc级甲酸购自赛默飞世尔科技公司(英国拉夫伯勒),实验所用纯水用milli-q超纯水系统(密里博公司,美国麻萨诸塞州比尔里卡)制备。所用分分析柱为waters xbridge-beh酰胺柱(2.5μm,100
×
2.1mm)。
[0075]
1.3样本处理和lc-ms分析
[0076]
空腹血液样本被收集到真空管中,保存在装有冰袋(0-4℃)的便携式聚苯乙烯泡沫塑料盒中,并在两小时内离心。离心后,立即将血浆样本储存在-80℃下。非靶向代谢物检测和量化分别在发现集和复制集中由基于lc-ms的代谢物平台进行。采用agilent 1290infinity
ⅱꢀ
uhplc系统和agilent 6545 uhd精密质谱仪进行采集。所有血浆样品(包括质量控制样品)与200μl制备的含4μg/ml l-苯丙氨酸(d8)的内标甲醇溶液(剑桥同位素实验室)旋涡1分钟。各质控样品内标的变异系数均小于0.2。提供了代谢组分析方法的详细信息如下所述。采用elisa试剂盒(血清crosslaps(ctx-i))测定血浆ctx-i水平,ids,中国上海。
[0077]
采用waters xbridge-beh酰胺柱(2.5μm,100
×
2.1mm),在安捷伦1290infinity ii uhplc系统和安捷伦6545uhd精密质谱仪上对等离子体样品和质量控制样品进行分析。采用流动相a(水中0.1%甲酸和10mm甲酸铵)和流动相b(乙腈中0.1%甲酸)的13分钟梯度。以高效液相色谱法测定默克公司产品中乙腈和甲酸的含量,以sigma-aldrich公司产品中甲酸铵的含量。最佳洗脱梯度为:0-1min,95%b;1-3min,95%-85%b;3-13min,85%-60%b。流速设定为0.4ml/min;柱温设定为25℃;进样量为2μl。系统运行后5分钟内立即返回初始条件进行柱重平衡。质量数据在esi 和esi-模式下采集,质量范围从50到1100。在esi 模式下,毛细管电压为4kv,喷嘴电压为250v,气体温度为325℃,碎片电压为120v。在esi-模式下,毛细管电压为3.5kv,喷嘴电压为1500v,气体温度为325℃,碎片电压为120v。用于监测质量轴精度的参考离子为121.0507,esi 模式下为922.0098,esi-模式下为112.9856、1033.9881。在该序列中,qc样品和空白样品每隔10个研究样品进行分析。
[0078]
安捷伦masshaunter定性分析b.07.00用于将原始质量数据转换为mzdata格式。使用开源r软件包xcms对峰值进行提取、对齐和集成。在is标准化后进行最近的qc标准化。is标准化值是用is准分子离子([m h] 在esi 模式下,[m-h]-在esi-模式下)与所有等离子体样品和qc样品中is离子的平均值之比计算的。然后,使用每个血浆样本中的is标准化值与最近的qc样本中相同特征的值乘以整个qc样本中测得的中值的比率计算标准化值。
[0079]
本发明人根据代谢组学分析得到的准确m/z值和qc样品得到的ms/ms片段与metlin和hmdb数据库中的条目匹配来识别特征。结合esi 和esi-模式后,一些代谢物会有多重加合。以qc样品方差最低的离子值作为代谢物的值。
[0080]
1.4统计分析
[0081]
在临床特征分析中,将受试者分为3组,即对照组(脊柱和髋部t评分均在-1以上)、骨质疏松组(脊柱或髋部t评分均在-2.5以下)和骨密度降低组(脊柱或髋部t评分均在-1
到-2.5之间)。采用连续变量方差分析和分类变量卡方检验比较各组的临床特征。
[0082]
分析前去除缺失值>20%(n=118)或变异系数较大(>0.25,n=20)的代谢物,对于剩余代谢物,用研究人群中代谢物的半可检测最小值估算其缺失值。将基于秩的逆正态变换应用于代谢组学数据,以便分别对发现和复制集中剩余的265种代谢物的代谢物水平的正态分布进行近似。对于初步分析,我们将骨量减少组和骨质疏松组的参与者合并为低骨密度组,并将低骨密度组和对照组的代谢物水平进行比较。采用年龄、性别、bmi和中心调整的多变量logistic回归模型,分别检查发现集和复制集中各代谢物与bmd状态的关系。使用benjamini-hochberg错误发现率(fdr)方法对发现集中的265种代谢物进行多重测试调整。对于成功复制的代谢物,其水平进一步分析为四分位数(使用参考组中定义的切点)。然而,除次黄嘌呤和肌苷外的4种代谢物中没有一种代谢物区分两组的灵敏度在80%以上。
[0083]
由于性激素对骨代谢有重要影响,进一步按性别进行分层分析作为二级分析。除非另有说明,否则双侧p<0.05被认为具有统计学意义。所有的统计分析都是使用r版本3.5.1进行的(https://www.r-project.org/).
[0084]
2.实验结果
[0085]
2.1志愿者临床信息
[0086]
表2显示了研究人群在发现和复制组中的正常骨密度、骨质减少和骨质疏松的特征。在这两组中,骨质疏松和骨质减少组的参与者更有可能是老年人、女性、更年期、较低的bmi和较高的脊柱bmd。与发现集的正常骨密度组相比,骨质疏松组和骨质疏松组的血浆ctx-i水平更高。
[0087]
表2.研究参与者的基线特征
[0088][0089][0090]
bmi,体重指数;ctx-i,i型胶原c末端端肽;bmd,骨密度。
[0091]
2.2 qc样品分析
[0092]
利用基于非靶标hplc-ms代谢组技术,从血浆样品中获得2588种代谢物(m/z,质荷比)。为了评估数据集的稳定性和再现性,在整个实验期间测定了qc样品。对qc样品和测试样品进行主成分分析(pca),从而得到一个二维pca得分图,示于图1。结果表明,qc样品形成的簇与测试样品形成的簇没有明显的分散,由此证实,我们目前的代谢组数据具有良好的稳定性和再现性。
[0093]
2.3血浆代谢组数据分析
[0094]
为了鉴定骨质疏松患者中显著改变的代谢物以及骨质疏松的潜在生物标志物,发
明人进行了两种类型的分析。首先,从opls-da模型中获得所有5000余种代谢物的vip得分,推测的生物标志物用s图示出(图1,2,3)。0pls-da模型的协方差(x轴)和相关性(y轴)一起示于散点图中。将骨质疏松患者中的每一个代谢物的错误发现率(q-value)、改变倍数(fc)和平均强度用健康对照的相同代谢物的平均值进行标准化,然后利用双侧wilcoxon秩和检验进行检验。将改变大小与统计检验结果一起绘制成热图(图4),这使得可以对改变倍数较大的代谢物进行快速直观地识别,结果表明,与健康对照组进行比较,其中120个分子离子峰在骨质疏松患者的血浆样品中显著增加或者降低(升高倍数>1.2、降低倍数<0.8)。为了鉴定潜在生物标志物,将120种显著改变的代谢物比对到kegg和hmdb数据库(<10ppm)。通过已知的鉴定检测到403种代谢物,包括61种氨基酸途径、17种碳水化合物、4种辅助因子和维生素、28种能量代谢途径、231种脂类、12种核苷酸、21种肽和29种其他代谢物。最终,重叠区域下的23种代谢物符合以下标准(q值<0.05,fc>1.2或fc<0.8,vip>1)。,它们的详细信息在表3中列出。在这23种代谢物中,有6个的参照标准品得到了验证(图5),可以认为是骨质疏松诊断的候选潜在生物标志物。这6种潜在生物标志物分别为肌苷、次黄嘌呤、pc(o-18:0/22:6)、sm(d18:1/21:0)、异亮氨酸脯氨酸和pc(16:0/18:3)。
[0095]
表3.骨质疏松病人血清中显著变化的23种代谢产物
[0096][0097][0098]
为了评估低骨密度状态下弹性模型中所选代谢物的性能,roc曲线分析显示,根据建立的预测模型,由30例骨质疏松病人和30例健康志愿者的两种诊断标志物的定量数据计算得到的roc曲线(图5)下的次黄嘌呤和肌苷的面积达到了0.975和0.877,根能够准确的预
测。结果表明本发明的诊断标志物对骨质疏松患者预测具有较高的准确性。
[0099]
表4骨质疏松6个标志物的曲线下面积
[0100][0101]
a.在非参数假设下
[0102]
b.零假设:实面积=0.5
[0103]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。