1.本发明涉及氢氧化镁制备方法领域,具体是一种用高钠镁比硫酸钠工业废水制备花球状氢氧化镁的方法。
背景技术:
2.随着我国近年来环保标准的提高,工业废液的绿色资源化利用得到了较大的发展。现阶段,规模化处理高盐废水仍然存在处理效率低,运行成本高的特点,还有很多需要突破和解决的关键技术问题。高钠镁比工业废水主要来源于印染、炼化、制药、制盐等企业生产过程中产生的排水,具有高含量的硫酸钠,以及少量的硫酸镁的特点。如果不处理直接蒸发结晶会导致硫酸钠纯度太低,并且其中镁资源无法综合利用,会造成资源的严重浪费。若直接排放会对土壤以及水质造成严重的污染。
3.氢氧化镁作为一个无机材料、具有无毒、无味、无腐蚀性、分解温度高等特性,在阻燃、环保、医用、食品、陶瓷、化妆品等领域都有着非常重要的用途。随着现代社会科学技术不断的发展,人们对新材料的要求不断提高,在不同领域使用的氢氧化镁的要求也有所不同,因此近年来主要关注在氢氧化镁的形貌、比表面积、粒度等性能。
4.目前生产氢氧化镁的方法有以下几种:一是由卤水和熟石灰反应制得。二是以经净化处理除去硫酸盐、二氧化碳、少量硼等杂质的卤水为原料,以氨水作为沉淀剂在反应釜中进行沉淀反应,从而制得氢氧化镁。三是菱镁矿石与无烟煤或焦炭在竖窑内煅烧,生成氧化镁和二氧化碳。苦土粉用水调成浆状后与规定浓度的盐酸反应制备氯化镁溶液。其氯化镁溶液与一定浓度的氨水在反应器中进行反应,生成物经洗涤、沉降、过滤分离、干燥、粉碎得到氢氧化镁产品。四是在利用浓海水提取浆状氢氧化镁。现有技术尚没有从高钠镁比硫酸钠工业废水中回收利用氢氧化镁的方法,因此有必要提供一种方法以回收工业废水中的氢氧化镁。
5.现有技术从含镁的溶液中制备氢氧化镁的方法大多数是直接加入强碱沉淀得到氢氧化镁产品,此工艺制得的氢氧化镁多为片状,且存在固液分离困难的技术问题。其他方法是直接加入氨水,通过搅拌得到氢氧化镁,此工艺过程中反应比较剧烈,且有大量未反应的氨水未能得到回收利用。
技术实现要素:
6.本发明的目的是提供一种用高钠镁比硫酸钠工业废水制备花球状氢氧化镁的方法,以解决现有技术没有从高钠镁比硫酸钠工业废水中回收利用氢氧化镁的问题。
7.为了达到上述目的,本发明所采用的技术方案为:用高钠镁比硫酸钠工业废水制备花球状氢氧化镁的方法,包括以下步骤:步骤1、取用氨水、高钠镁比硫酸钠工业废水,将氨水、高钠镁比硫酸钠工业废水分别装于不同敞口容器内,其中氨水的质量浓度为10
‑
30%,取用的氨水和高钠镁比硫酸钠工业废水的体积质量比为1:0.1
‑
1:1;
步骤2、将装有氨水、高钠镁比硫酸钠工业废水的敞口容器分别置于密闭环境中,于20
‑
100℃静置反应12
‑
48h,使氨水挥发氨气,并由挥发氨气溶解于高钠镁比硫酸钠工业废水中与镁离子反应,由此在装有高钠镁比硫酸钠工业废水的敞口容器中得到白色固体;步骤3、步骤2结束后,将含有白色固体的高钠镁比硫酸钠工业废水过滤后得到滤渣,将滤渣于80
‑
110℃温度干燥5
‑
10h,得到形貌为花球状的氢氧化镁。
8.进一步的,步骤1所述高钠镁比硫酸钠工业废水中,硫酸镁含量为0.1
‑
0.2mol/l,钠镁比为20
‑
40。
9.进一步的,步骤2所述的反应温度为20
‑
100℃,反应时间为12
‑
48h。
10.进一步的,步骤2反应结束后,步骤2反应结束后,高钠镁比硫酸钠工业废水的ph值范围为10.5
‑
12.5,若ph在10.5以下,需要按步骤2继续静置反应5
‑
10h。
11.进一步的,所述步骤3中滤渣的干燥温度为80
‑
110℃,干燥时间为5
‑
10h。
12.进一步的,步骤3中过滤后得到的滤液为高纯饱和硫酸钠溶液。
13.本发明可净化除去高钠镁比硫酸钠工业废液的镁,同时制备得到花球状的氢氧化镁。通过高钠镁比硫酸钠工业废液与氨水挥发氨气之间的沉淀反应,使高钠镁比硫酸钠工业废液中的镁离子和挥发氨气中的铵根离子以及水发生反应生成氢氧化镁沉淀,其反应方程式如下:mg
2
2nh3 2h2o=mg(oh)2↓
2nh
4
与现有技术相比,本发明的优点为:本发明解决了高钠镁比硫酸钠工业废水的绿色资源化利用问题,通过利用氨水的挥发性和溶解性将高钠环境中含量比较低的镁净化除尽得到纯度高的硫酸钠溶液,同时使镁转化为实用价值高的氢氧化镁;该工艺流程简单,生产成本低,无需任何添加剂。
14.与现有技术相比,本发明的优点为:本发明不是直接将含氨原料与其他原料直接混合,而是氨水形成氨气,使氨气溶解于高钠镁比的硫酸钠工业废水,这使得反应平缓稳定,安全性高。
15.与现有技术相比,本发明的优点为:本发明不是含有镁的溶液直接与强碱反应制备氢氧化镁,从而使反应结束后固液分离速率显著提升。
16.与现有技术相比,本发明的优点为:本发明反应过程中不需要搅拌,从而使制备的氢氧化镁为花球状,并且因为氨水未直接加入到反应原料中,从而反应结束后氨水可以重复利用,直到氨水完全没有挥发性。
附图说明
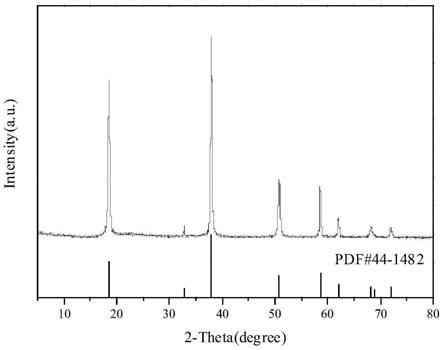
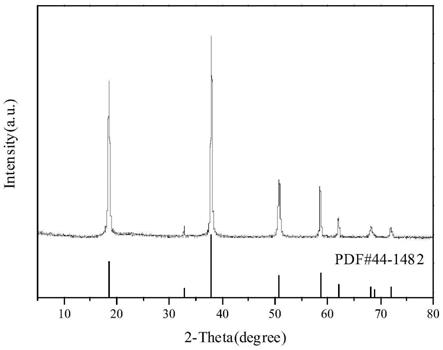
17.图1为本发明产品的x
‑
射线衍射谱图。
18.图2为本发明产品放大倍数为3千倍的扫描电镜图。
19.图3为本发明产品放大倍数为1.1万倍的扫描电镜图。
具体实施方式
20.下面结合实施例对本发明进一步说明。
21.实施例1用高钠镁比硫酸钠工业废水制备花球状氢氧化镁的方法包括以下步骤:
步骤1、量取150ml的高钠镁比硫酸钠工业废水装于烧杯a中,再量取100ml质量分数为25%的氨水装于烧杯b中。
22.所采用的高钠镁比硫酸钠工业废水中硫酸钠接近饱和,而硫酸镁含量比较低,其硫酸镁含量为0.2mol/l,钠镁比为25。
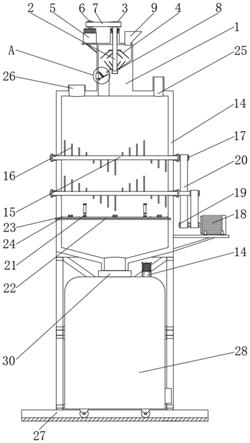
23.步骤2、将装有高钠镁比硫酸钠工业废水的烧杯a和装有氨水的烧杯b以相间隔的形式放入密封反应器c中,在温度为25℃,等静置反应24h后,在静置反应过程中氨水挥发形成氨气,氨气溶解于烧杯a中的高钠镁比硫酸钠工业废水作为沉淀剂,并由溶解的氨气与高钠镁比硫酸钠工业废水中的镁离子反应,由此在烧杯a中产生白色沉淀。
24.步骤3、步骤2结束后,将烧杯a中溶液抽滤后得到滤渣、滤液,其中滤液为高纯饱和硫酸钠溶液;将滤渣多次水洗后,再将洗涤后的滤渣在温度为95℃环境下干燥5h后即可得到花球状氢氧化镁。
25.实施例2用高钠镁比硫酸钠工业废水制备花球状氢氧化镁的方法包括以下步骤:步骤1、量取150ml的高钠镁比硫酸钠工业废水装于烧杯a中,再量取100ml质量分数为10%的氨水装于烧杯b中。
26.所采用的高钠镁比硫酸钠工业废水中硫酸钠接近饱和,而硫酸镁含量比较低,其硫酸镁含量为0.2mol/l,钠镁比为25。
27.步骤2、将装有高钠镁比硫酸钠工业废水的烧杯a和装有氨水的烧杯b以相间隔的形式放入密封反应器c中,在温度为25℃,等静置反应24h后,在静置反应过程中氨水挥发形成氨气,氨气溶解于烧杯a中的高钠镁比硫酸钠工业废水作为沉淀剂,并由溶解的氨气与高钠镁比硫酸钠工业废水中的镁离子反应,由此在烧杯a中产生白色沉淀。
28.步骤3、步骤2结束后,将烧杯a中溶液抽滤后得到滤渣、滤液,其中滤液为高纯饱和硫酸钠溶液;将滤渣多次水洗后,再将洗涤后的滤渣在温度为95℃环境下干燥5h后即可得到花球状氢氧化镁。
29.实施例3用高钠镁比硫酸钠工业废水制备花球状氢氧化镁的方法包括以下步骤:步骤1、量取150ml的高钠镁比硫酸钠工业废水装于烧杯a中,再量取100ml质量分数为25%的氨水装于烧杯b中。
30.所采用的高钠镁比硫酸钠工业废水中硫酸钠接近饱和,而硫酸镁含量比较低,其硫酸镁含量为0.2mol/l,钠镁比为25。
31.步骤2、将装有高钠镁比硫酸钠工业废水的烧杯a和装有氨水的烧杯b以相间隔的形式放入密封反应器c中,在温度为60℃,等静置反应12h后,在静置反应过程中氨水挥发形成氨气,氨气溶解于烧杯a中的高钠镁比硫酸钠工业废水作为沉淀剂,并由溶解的氨气与高钠镁比硫酸钠工业废水中的镁离子反应,由此在烧杯a中产生白色沉淀。
32.步骤3、步骤2结束后,将烧杯a中溶液抽滤后得到滤渣、滤液,其中滤液为高纯饱和硫酸钠溶液;将滤渣多次水洗后,再将洗涤后的滤渣在温度为95℃环境下干燥5h后即可得到花球状氢氧化镁。
33.图1是实施例1,实施例2,实施例3得到的产物的x
‑
射线衍射谱图,从图1中可以看出,制备的样品与氢氧化镁的标准卡片一致,说明用上述方法得到的产物与前面本技术的
产物一致。
34.图 2、图3是实施例1通过在放大倍数为3千倍和1.1万倍的扫描电镜图可以看出,产物为规则花球形状,说明用上述方法得到的产物与前面本技术的形貌一致。
35.本发明所述的实施例仅仅是对本发明的优选实施方式进行的描述,并非对本发明构思和范围进行限定,在不脱离本发明设计思想的前提下,本领域中工程技术人员对本发明的技术方案作出的各种变型和改进,均应落入本发明的保护范围,本发明请求保护的技术内容,已经全部记载在权利要求书中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。