1.本发明涉及一种药物,特别涉及一种用于治疗肿瘤的药物。
背景技术:
2.在肿瘤的药物治疗中,使用单一药物会引起获得性耐药及不良反应事件发生,而且,单一药物的疗效、响应率均有限,即使是炙手可热的免疫治疗,临床响应率也仅有20%左右。因此,nccn指南从增强药物作用、提高患者生存质量、降低毒副作用出发,将联合用药纳入临床用药规范,并指出其具有不可替代的作用。所以,充分分析和总结药物特点、深入挖掘联合用药策略,是进一步提高疗效、克服耐药的关键,具有重要的科学研究价值及临床使用意义。
3.顺铂具有抗瘤谱广、作用强、疗效确切等特点,为治疗多种实体肿瘤的一线药物,在临床上被广泛应用,但是存在三个严峻的问题:获得性耐药、安全范围窄、组织或器官毒性明显,尤其是肝肾毒性,这三大类问题严重危害患者的生存质量,导致早期治疗终止,引起药物的使用率降低,是当前顺铂应用的棘手问题。因此有必要开发与顺铂组合使用的方案用以协同增敏、提高疗效、减轻毒性。
技术实现要素:
4.本发明的目的在于,提供一种能够与顺铂组合使用的方案用以协同增敏、提高疗效、减轻毒性。
5.本发明提供一种用于抑制肿瘤的药物组合物,所述药物组合物的活性成分为山椒子烯酮和顺铂。
6.其中,所述顺铂为注射用顺铂。
7.其中,所述药物组合物中还包括用于溶解山椒子烯酮和顺铂的溶剂。
8.其中,所述溶剂为生理盐水。
9.其中,所述组合药物中山椒子烯酮与顺铂的质量比为15-30:1。
10.其中,所述抑制肿瘤为抑制肿瘤细胞的生长。
11.其中,所述肿瘤为肉瘤。
12.其中,抑制肿瘤细胞的生长为抑制肿瘤的瘤重和/或抑制肿瘤细胞的数目。
13.山椒子烯酮和顺铂在制备抑制肿瘤产品中的应用也应在本发明的保护范围之中。
14.所述的物组合物在制备抑制肿瘤产品中的应用也应在本发明的保护范围之中。
15.其中,所述肿瘤为肉瘤。
16.其中,抑制肿瘤细胞的生长为抑制肿瘤的瘤重和/或抑制肿瘤细胞的数目。
17.上述药物可含有药学上可接受的载体。所述药学上可接受的载体可为冻干保护剂糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;西黄蓍胶粉末;麦芽;明胶;滑石;固体润滑剂,如硬脂酸和硬脂酸镁;硫酸钙;植物油,如花生油、棉籽油、芝麻油、橄榄油、玉米油和可可油;多元醇,如甘油、甘露糖醇;海藻酸;乳化剂,如tween;磷脂,如卵磷脂,大
豆磷脂,磷脂酰乙醇胺,磷脂酰甘油,磷脂酰肌醇,磷脂酰丝氨酸,硬脂酰胺;胆固醇;大分子高聚物,如聚乙烯亚胺,壳聚糖,透明质酸;润湿剂,如月桂基硫酸钠;着色剂;调味剂;压片剂、稳定剂;抗氧化剂;防腐剂;无热原水;等渗盐溶液;和磷酸盐缓冲液等;生理盐水、甘油和磷酸盐缓冲盐水。
18.上述应用中,所述产品可为药物。
19.上述药物和产品中,山椒子烯酮和顺铂可分别独立包装,也可混合在一起。
20.上文中,所述肿瘤可为实体肿瘤或非实体肿瘤。所述实体肿瘤可为肉瘤。
21.本发明中,zey与顺铂联用在抗肉瘤细胞增殖中呈明显的协同效应。在肉瘤s180细胞中,当以zey的起效剂量去联用时,具有强协同效应和顺铂剂量减低效应,并降低ic50值。这种在高抑制率(>80%)水平下的协同效应,一般对应更高的治疗水平和开发价值。
22.从体内实验结果来看,在小鼠肉瘤s180移植瘤模型上,单用zey和单用顺铂的抑瘤效果明显,当二者联用后,抑瘤率大幅增加,协同增效显著,因此,有利于为临床顺铂毒性明显的患者减轻顺铂的剂量,获得更长的顺铂使用时间。与体外实验有高度的显著一致性。
23.同时,在安全性评估中,通过体重数据可以大体看出zey联合顺铂后,未出现体重的进一步下降,显示可能并没有叠加毒性,在顺铂的主要蓄积器官——肝、肾的相关检测中,联用方案没有诱导非靶组织的进一步损伤,显示出较高的安全性。
附图说明
24.图1为本发明的实施例中实验终点时剥离的各组肿瘤图片。
25.图2为给药过程中各组小鼠的体重变化图。
26.图3为各组小鼠肝脏组织的病理学观察,其中,放大倍数为200
×
和400
×
,黑色箭头表示肝细胞坏死,核碎裂;白色箭头表示炎性细胞浸润;黑方框内表示中央静脉与门静脉轻度淤血扩张,血管腔有少量白细胞。
27.图4为各组小鼠肾脏组织的病理学观察,其中,放大倍数为200
×
和400
×
,黑色箭头表示肾皮质血管中含铁血黄素渗出;白色箭头表示肾小球囊腔轻微的萎缩。
具体实施方式
28.下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
29.材料说明:
30.山椒子烯酮,英文名zeylenone,cas:193410-84-3,以下简称zey,为白色粉末,干燥保存,纯度>97.5%(hplc法检测)。zey的化学结构为zey是毒副作用低的天然产物。
31.顺铂,结构式为cas:15663-27-1,本发明采用注射用顺铂,购自齐鲁制药有限公司,规格10mg。使用时用10ml的生理盐水溶解,制成浓度为1mg/ml的注射液,使用
时稀释。
32.s180小鼠肉瘤细胞,悬浮生长,购自中国医学科学院基础医学研究所细胞中心,在含有10%胎牛血清和1%青霉素链霉素混合物rpmi-1640(w/o hepes)完全培养基中培养。
33.雌性icr小鼠(18-20g),规范饲养于spf级动物房。购自斯贝福(北京)生物技术有限公司,许可证号scxk(京)2016-0002,实验动物质量合格证号no.11401500044849。
34.实验试剂说明:rpmi-1640(w/o hepes)培养基,康宁生物科技有限公司;ausbian特级胎牛血清(fbs),上海威正翔禹生物科技四季青公司;cck8试剂,日本同仁试剂公司;二甲基亚砜(dmso),sigma公司;磷酸盐缓冲液(pbs),北京索莱宝生物科技有限公司;蓖麻油聚氧乙烯醚cas:61791-12-6,阿拉丁试剂公司;无水乙醇(分析纯)和4%甲醛,北京化工厂;0.9%生理盐水,石家庄四药有限公司;谷草转氨酶(ast)、谷丙转氨酶(alt)、总胆红素(tbil)和尿素(urea)试剂盒,中生北控生物技术有限公司;苏木素-伊红染液,北京艾普希隆生物科技有限公司;二甲苯、盐酸、氨水和中性树胶,国药集团化学试剂有限公司。
35.1.zey的配制
36.用于体外的研究时,称取适量的zey用dmso完全溶解,至浓度为15mg/ml,此为储备溶液,分装,放于-20℃冰箱备用。给药时,用培养基稀释至所需浓度。
37.用于体内的研究时,先用聚氧乙烯蓖麻油和乙醇(1:1,w/w)为溶剂溶解zey,放于4℃冰箱,当给药时再使用生理盐水稀释至所需浓度。
38.2.顺铂的配制
39.将顺铂用生理盐水溶解,制成浓度为1mg/ml的注射液,使用时稀释至所需浓度。
40.实施例1cck8法检测细胞增殖抑制率
41.1.按照如下步骤进行不同浓度的顺铂溶液对s180小鼠肉瘤细胞的抑制情况。
42.1)将s180小鼠肉瘤细胞在含有10%胎牛血清和1%青霉素链霉素混合物rpmi-1640(w/o hepes)完全培养基中培养。将处于对数生长期的s180细胞离心收集后,制备细胞悬液并计数,调整细胞密度为1
×
105个/ml;
43.2)将上述单细胞悬液依次加入96孔板中,每孔100μl,边缘一周用pbs补齐(避免边缘效应),加完细胞后,用手轻拍96孔板边缘,使其铺板均匀,防止聚集,随后将96孔板放于培养箱中;将细胞随机分为18个药物组(6个顺铂药物组、6个zey组和6个顺铂 zey组)和1个对照组,每组5个复孔。
44.3)在管中使用倍半稀释方法配制6种浓度的顺铂溶液,6种浓度的顺铂溶液中的最高浓度为33.30μm,其它浓度如表1的第1列所示。将配制好的6种顺铂溶液按照浓度从小到大的顺序放于管架上,6个顺铂药物组每孔加入100μl相应浓度的顺铂溶液,对照组每孔加入100μl培养基,轻轻拍打96孔板边缘,使药物在孔中尽量均匀(每个浓度设置5个复孔);
45.4)药物作用24h后,每孔加10μl的cck8试剂,继续培养3h;
46.5)将96孔板拿出,观察细胞状态,记录好现象后,拿出细胞间;
47.6)使用酶标仪的absorption板块,在450nm下测定od值,细胞增殖抑制率%=(1-od
药物组
/od
对照组
)
×
100%,用graphpad prism 5绘制结果图,并用compusyn软件计算ic50值。
48.2.按照如下操作进行不同浓度的zey溶液对s180小鼠肉瘤细胞的抑制情况。
49.将步骤1中3)替换为如下操作,保持其他步骤不变,测试zey溶液对s180小鼠肉瘤细胞的抑制情况:在管中使用倍半稀释方法配制6种浓度的zey溶液,6种浓度的zey溶液中
的最高浓度为26.16μm,其它浓度如表1的第3列所示。将配制好的6种zey溶液按照浓度从小到大的顺序放于管架上,6个zey药物组每孔加入100μl相应浓度的zey溶液,对照组每孔加入100μl培养基,轻轻拍打96孔板边缘,使药物在孔中尽量均匀(每个浓度设置5个复孔)。
50.3.按照如下操作进行不同浓度的顺铂和一种浓度的zey溶液和对s180小鼠肉瘤细胞的抑制情况。
51.将步骤1中3)替换为如下操作,保持其他步骤不变,测试顺铂和zey溶液对s180小鼠肉瘤细胞的抑制情况:在管中使用倍半稀释方法配制6种浓度的顺铂溶液,6种浓度的顺铂溶液中的最高浓度为33.28μm,其它浓度如表1的第1列所示,向该6种浓度的顺铂溶液中加入zey储备液,至zey的含量为1.6μm,得到6种顺铂 zey溶液,该6种顺铂 zey溶液中的zey的含量均为1.6μm,顺铂的含量分别为33.28μm、16.64μm、8.32μm、4.16μm、2.08μm和1.04μm。将配制好的6种顺铂 zey溶液按照浓度从小到大的顺序放于管架上,6个顺铂 zey药物组每孔加入100μl相应浓度的顺铂 zey溶液,对照组每孔加入100μl培养基,轻轻拍打96孔板边缘,使药物在孔中尽量均匀(每个浓度设置5个复孔)。
52.4.中位效应评价药物组合的效应
53.选择国际标准的计算方法—中位效应法(chou-talalay)来分析评估zey与顺铂联合应用的效果。将获得的数据输入国际通用的compusyn软件中,运用该方法的主要判断指标—联合指数(combination index,ci)和剂量减低指数(dose reduction index,dri)进行分析,对该组合进行药物相互作用的评价。
54.在这里,ci值反映两个药物之间的相互作用。公式为ci=d1/(dx)1 d2/(dx)2;(dx)1和(dx)2是两个化合物达到特定抑制率独自所需要的浓度;d1和d2是两种化合物联合使用时,达到与单药使用时相同的抑制率各自所需要的浓度。判定方式为:ci>1.1,=0.9~1.1和<0.9分别代表两种药物呈拮抗、相加和协同作用。
55.dri值反映在给定的效应水平上,与单独使用每种药物的剂量相比,协同使用的每种药物的剂量可以减少的倍数。两药联合的dri计算公式为(dri)1=(dx)1/(d)1,dri值越大,说明某一治疗效果的剂量减少越大,但并不一定总是表明协同作用,还需和ci一起分析,才可得出正确的结论。dri在临床中非常重要,减少剂量可以降低对宿主的毒性,同时保留治疗效果。
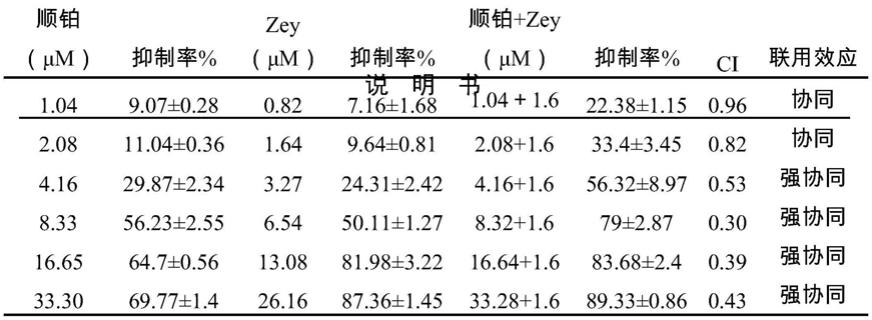
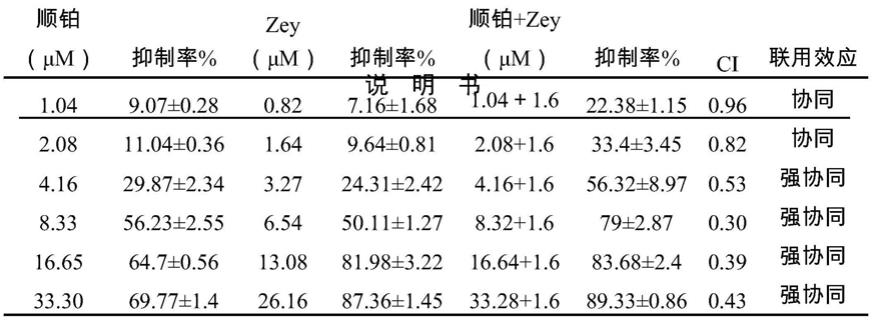
56.ci分析结果如表1所示,从表1的数据可以看出,当顺铂和zey分别单独作用于肉瘤s180细胞时,均有明显的抑制肉瘤细胞增殖的作用,表明两者单用时均有效,且从抑制率上看,zey的抗肿瘤效果与顺铂相当;当把固定浓度的zey(起效剂量,1.6μm)和顺铂联合作用于肉瘤s180细胞时,出现了比单用顺铂更明显的增殖抑制效果。而后,经过compusyn软件计算联合指数,发现ci值均小于1,说明两药联用为协同作用。此外,当联用组抑制率在56%-89%时,为强协同效应。
57.表1 zey与顺铂联合作用于肉瘤s180细胞24h的联合指数(ci)分析
[0058][0059]
在对联合指数(ci)进行分析后,进一步对剂量减低(dri)进行评估,结果如表2所示。从表2的dri指数分析可以看出,zey与顺铂联用后对各自都有剂量减低的作用,zey的dri值在2.54-4.89的范围,顺铂的dri值在1.60-17.98的范围,可以看出,二者联用时对顺铂的剂量减低作用比zey明显。因此,当达到相同抑制率效果时,联用可实现明显的剂量减低,从而有望改善顺铂的毒性现象,有进一步研究的重要价值。
[0060]
表2 zey与顺铂联合作用于s180细胞24h的剂量减低指数(dri)分析
[0061][0062]
实施例2
[0063]
为了进一步明确该组合的体内有效性,通过建立小鼠肉瘤s180模型来进一步考察zey联合顺铂的体内协同抗肿瘤作用。
[0064]
1.s180荷瘤小鼠模型的建立
[0065]
1.1s180体内传代
[0066]
取10只4周龄、体重为18-20g的雌性icr小鼠,活动、体重、进食和饮水均正常,取对数生长期s180小鼠肉瘤细胞,用生理盐水调整细胞密度为2.5
×
106个/ml,0.2ml/只,摇匀后,腹腔注射于icr小鼠的腹部,待长到第8天,见到小鼠的腹部隆起,此时,需要传代。
[0067]
传代时,将腹部隆起较明显的icr小鼠脱颈椎处死,将之完全泡入75%的酒精溶液中消毒片刻,稍微沥干后,拿到超净台中,用已灭菌的小剪刀在右侧腹部开口,用注射器将1ml生理盐水打入小鼠腹部,用以稀释腹水,随后,用移液枪将乳白色的腹水抽出,放于15ml的离心管内,用生理盐水100倍稀释后,计数,调整细胞密度为2.5
×
106个/ml,摇匀后,再次0.2ml/只腹腔注射于10只icr小鼠的腹部,此为第二代。以同样的方式,在体内传代4次。
[0068]
1.2s180皮下移植瘤模型的建立
[0069]
收集步骤1.1的体内传代4次的接种s180小鼠肉瘤细胞腹水,用生理盐水100倍稀释后,计数,调整s180小鼠肉瘤细胞含量为5
×
106个/ml,将离心管封口,迅速拿到动物房。
将细胞悬液轻轻摇匀,在无菌条件下使用注射器吸取0.2ml细胞悬液(1
×
106个细胞/只)接种于icr小鼠的右侧腋窝皮下,既得s180荷瘤小鼠模型。
[0070]
2动物分组及给药
[0071]
接种后的第二天,将动物按体重随机分为5组(每组10只),具体组别及药物注射情况如下:
[0072]
(1)正常组(10只四周龄,体重为22.3-24.8g的未接种s180细胞的icr小鼠):正常饮食饮水;
[0073]
(2)模型组(10只四周龄,体重为22.7-26.7g,按照步骤1中的方法接种s180细胞的icr小鼠):对小鼠进行腹腔注射生理盐水,每天注射1次,按照0.1ml生理盐水/10g体重给药;
[0074]
(3)顺铂组(10只四周龄,体重为22.3-26.4g,按照步骤1中的方法接种s180细胞的icr小鼠):对小鼠进行腹腔注射顺铂溶液,每两天注射一次,顺铂的使用剂量为2mg/kg/2day;
[0075]
(4)zey组(10只四周龄,体重为22.0-25.5g,按照步骤1中的方法接种s180细胞的icr小鼠):对小鼠进行腹腔注射zey溶液,每天注射1次,zey的使用剂量为15mg/kg/day;
[0076]
(5)联用组(10只四周龄,体重为23.4-25.8g按照步骤1中的方法接种s180细胞的icr小鼠):对小鼠进行腹腔注射,每天注射1次zey,zey的使用剂量为15mg/kg/day;每两天注射一次顺铂,顺铂的使用剂量为2mg/kg/2day;
[0077]
以上各组均按照0.1ml药剂/10g体重小鼠体重腹腔注射给药至10天,期间并测量小鼠体重及观察肿瘤生长,计算抑瘤率,评价zey对顺铂的协同增效作用。如表3所示。
[0078]
其中,zey溶液的配置方法如下:zey以聚氧乙烯蓖麻油和乙醇(1:1,w/w)为溶剂溶解zey制备贮备液,使用时用生理盐水稀释至所需浓度,得到zey溶液。
[0079]
顺铂溶液的配置方法如下:将顺铂用生理盐水溶解,制备贮备液,使用时用生理盐水稀释至所需浓度,得到顺铂溶液。
[0080]
结果如表3所示和图1所示。采用graphpad prism 5.0软件(graphpad software,la jolla,ca,usa)进行统计分析,实验数据采用均值
±
标准差(means
±
sd)表示。采用单因素方差分析(one-wayanova),然后使用tukey’s post hoc test(t-test)进行组间两两比较,当p<0.05时认为差异具有统计学意义。
[0081]
肉瘤s180模型是非常经典的动物肿瘤模型,有体外细胞增殖和体内移植功能,被广泛应用于抗肿瘤药物筛选中。表3和图1的数据显示,其中,由于正常组的小鼠体内无肿瘤生长,故表3和图1仅显示模型组、顺铂组、zey组和联用组四组的数据。zey和顺铂分别给药时,s180荷瘤小鼠的肿瘤生长均受到抑制,当zey和顺铂联合使用时,对s180实体瘤的抑制率显著提高,与单用顺铂比,差异显著(p<0.01);且通过chou分析后,体内同样具有协同效应。因此,zey与顺铂联合使用能明显增强顺铂的抗肿瘤作用。体内实验的这一结果,结合先前实例所示的体外实验结果,进一步表明,zey提高了顺铂对肉瘤的敏感性,协同抑制肉瘤的体外增殖与体内生长。
[0082]
表3 zey和顺铂协同抑制s180荷瘤小鼠肿瘤的体内生长
[0083][0084]
注:
**
p<0.01vs.模型组,
##
p<0.01vs.顺铂组
[0085]
实施例3
[0086]
顺铂的主要毒性靶器官为肝、肾、耳,严重影响化疗效果和患者生存质量,因此,通过协同增敏进而减轻顺铂毒性、增强化疗效果是目前研究的热点。综上,在本实施例3中,通过探究在肉瘤s180小鼠模型中,判断联用后是否加剧了顺铂的主要毒性靶器官肝、肾的不良反应,即确定该方案在协同增效的同时,会不会有叠加毒性的安全性隐患。
[0087]
3.1体重变化分析
[0088]
同时实施例2中的五组小鼠进行药物试验过程中的体重数据,统计分析和作图,结果如图2所示,在给药过程中,各组小鼠均无死亡现象出现,比较图2中的体重变化趋势,可以看出,正常组、模型组和zey组的小鼠体重均平缓增加,顺铂组和联用组的小鼠体重增长较慢,尤其是给药第10天时,这两组的体重与正常组出现差异,这说明给药后期的铂蓄积会造成小鼠的体重下降,会对小鼠的生活状态造成影响。
[0089]
3.2血清alt、ast活性、tbil、urea水平检测
[0090]
alt、ast是检测肝功能的最重要、最敏感的指标,其活性的高低反映了肝脏受损的程度。urea是由肾脏排泄的低分子含氮废物的主要成分,其对肾病的病程、病情观察及预后判断均有意义,是肾病的主要检测项目。
[0091]
将实施例2中获得的血清从-80℃中取出(血清的获取:在实施例2中的五组小鼠完成给药后,先摘眼球取血,然后脱颈椎处死,最后剥离肿瘤,取肝肾。取的血先室温沉淀1h,随后离心既得血清,将血清保存在-80℃条件下),取适量血清分装于ep管中,按照谷草转氨酶(ast)、谷丙转氨酶(alt)、总胆红素(tbil)和尿素(urea)试剂盒(生北控生物技术有限公司)操作检测血清中的alt、ast活性、tbil、urea水平。血清生化结果如表4所示,从表4中可以看出,顺铂组小鼠血清alt、ast活力、tbil、urea水平显著增加,其中alt、ast活力、tbil水平较正常组分别升高了46.39%、61.34%和22.34%,urea水平较正常组升高了12.23%,这提示顺铂对肾脏及肝脏造成一定的损伤,并且比较可知,肾脏对顺铂的耐受较高,肝脏对顺铂的敏感度高于肾脏。在联用组中,urea变化虽不明显,但在alt、ast、tbil指标上,联用减弱了顺铂造成的改变,一定程度改善生化指标,减轻了顺铂所致的肝毒性。
[0092]
表4药物处理对小鼠血清中的alt、ast活性和tbil、urea水平的影响(n=10)
[0093][0094]
注:*是所有组与正常组相比,用于表示每个组的异常,#是联用组与顺铂组比,表示是否减毒。
[0095]
*p<0.05,**p<0.01;#p<0.05,##p<0.01
[0096]
3.3肝脏、肾脏的病理学检测
[0097]
将实施例2中进行了10天药物试验的五组小鼠,每组随机取6只进行肝脏和肾脏的病理学检测,五组小鼠肝脏的病理切片结果如图3所示,五组小鼠肾脏的病理切片结果如图4所示。
[0098]
图3中,上列图放大倍数为200
×
,下列图放大倍数为400
×
,黑色箭头表示肝细胞坏死,核碎裂;白色箭头表示炎性细胞浸润;黑方框内表示中央静脉与门静脉轻度淤血扩张,血管腔有少量白细胞。由图3的肝脏的病理切片结果可看出:模型组出现炎细胞浸润和淤血,顺铂组造成较大面积的肝细胞坏死、核碎裂和炎细胞浸润,而单用zey组和联用组肝细胞形态基本正常,仅有微量白细胞和淤血扩张,损伤较轻微,这与上述生化指标检测结果相吻合。
[0099]
图4中,上列图放大倍数为200
×
,下列图放大倍数为400
×
,黑色箭头表示肾皮质血管中含铁血黄素渗出;白色箭头表示肾小球囊腔轻微的萎缩。肾脏是顺铂的主要排泄器官,从图4的肾脏的病理结果可以看出:模型组和联用组的肾脏组织结构正常,各结构间界限清晰,着色均匀,仅表现出肾小球嚢腔萎缩,顺铂组有铁血黄素渗出现象、并伴有炎性细胞浸润。
[0100]
上述步骤中病理学检测按照常规的石蜡包埋—4μm切片—he染色—显微镜镜检—图像采集—阅片分析进行逐步的操作。
[0101]
结合上述实施例,从体外实验的结果,发现zey与顺铂联用在抗肉瘤细胞增殖中呈明显的协同效应。在肉瘤s180细胞中,当以zey的起效剂量去联用时,具有强协同效应和顺铂剂量减低效应,并降低ic50值。这种在高抑制率(>80%)水平下的协同效应,一般对应更高的治疗水平和开发价值。
[0102]
从体内实验结果来看,在小鼠肉瘤s180移植瘤模型上,单用zey和单用顺铂的抑瘤效果明显,当二者联用后,抑瘤率大幅增加,协同增效显著,因此,有利于为临床顺铂毒性明显的患者减轻顺铂的剂量,获得更长的顺铂使用时间。与体外实验有高度的显著一致性。
[0103]
同时,在安全性评估中,通过体重数据可以大体看出zey联合顺铂后,未出现体重的进一步下降,显示可能并没有叠加毒性,在顺铂的主要蓄积器官——肝、肾的相关检测中,联用方案没有诱导非靶组织的进一步损伤,显示出较高的安全性。
[0104]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本申
请中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。