1.本发明涉及如下领域,使用iv铁碳水化合物复合物(例如羧基麦芽糖铁)治疗铁缺乏,监测或识别个体以确定对其给药所述iv铁碳水化合物复合物的可行性,以及将所述iv铁碳水化合物复合物与额外药物组合以减缓或减少所述iv铁碳水化合物复合物诱发的副作用。
背景技术:
2.铁缺(id)乏会损害身体产生血红蛋白(关键的氧气转运体)的能力,和损害产生关键能量(atp)的酶的功能。因此其症状包括疲劳和其他缺乏能量的体征,例如心跳加速、呼吸短促和胸痛。
3.id具有严重的后果。在慢性心力衰竭(chf)病人中,相对于铁状态正常的病人,患有id的病人的死亡和住院的风险提高。铁储存严重影响生活质量(qol),但随着铁储存的恢复,生活质量迅速改善。患有id或ida的病人进行手术时会具有不好的结果——部分原因是输血时的风险更大。母体的铁缺乏与早产及胎儿大脑发育受损的风险的提高有关。
4.缺铁性贫血(ida)在铁储备耗尽时发生。其为广泛存在的。根据who,全球大约10亿人患有ida。450万病人被诊断为ida。每日口服铁是大多数ida病人的一线治疗,但往往因缺乏依从性、效力不佳和副作用而失败。
5.高剂量静脉注射(iv)铁是一种有吸引力的治疗方案。病人一般每年需要1
‑
3克铁,高剂量iv铁有效且快速改善症状,并提高血红蛋白水平。高剂量iv铁可以在一次或几次访视中实现治疗,并且iv铁是不能口服铁的病人的唯一选择。
6.羧基麦芽糖铁(fcm)属于新一代的高剂量铁产品。旧的低剂量产品(葡萄糖酸铁和蔗糖铁)要求5
‑
20次访视,而这些新一代产品通过快速输注产品,可以在一次或两次的访视中进行铁校正。
7.在所有给药iv铁复合物治疗铁缺乏和缺铁性贫血的人中,观察到了中等程度和短暂的血清磷酸盐(s
‑
phosphate)下降。这种普遍现象被认为与红细胞生成中的磷酸盐的消耗有关,这是胃肠外铁治疗的主要预期效果。例如,参见vanwycketal.,2009.。其他人倾向于磷酸盐消耗理论,认为肾脏磷酸盐的流失可能是近端肾小管功能障碍的结果,近端肾小管功能障碍由iv铁对近端肾小管上皮细胞的直接毒性作用导致(pratsetal.,2013.)。
8.羧基麦芽糖铁(fcm)是非常常用的铁碳水化合物复合物,其用于治疗未进行透析的患有id或ida的病人。在美国,其商品名为是可商购的,以及在欧盟和许多其他国家,其商品名为是可商购的。典型的fcm治疗方案包括以静脉输注给予两剂量的750mg元素,两次剂量间隔一周(这是美国标签上批准的用途),或者输注1000mg元素铁后一周额外给予500
‑
1000mg的剂量(这是其欧盟标签上批准的用途)。
9.与葡聚糖铁(wolfetal.,2013)、蔗糖铁(wo2013/134273a1)和异麦芽糖苷铁1000(bageretal.,2016,schaeferetal.,2016,zolleretal.,2017)相比,fcm显示出其导致更剧烈和更长效的血清磷酸盐减少,并且结果导致更高的低磷血症患病率,即特征为过低的血
清磷酸盐的病症。
10.尽管如此,虽然个别病例报道了用fcm治疗导致低磷血症(anandg,schmidc,bmjcaserep2017)和随后几个月发生的骨并发症,例如骨软化症(例如,参见schaeferetal.2017;kleinetal.2018),但大多数出版物对这些发现提出积极的争议,或被定性为罕见并令人好奇的。大量的关于fcm用途的科学出版物描述了相关的低磷血症是如何被认为是短暂的、无症状的和/或与临床无关的。例如,参见aksanetal.,2007;bregmanetal.,2014;charytanetal.,2013;evstatiev,2011;hussainetal.,2013;ikutaetal.,2018;pratsetal.,2013;qunibietal.,2011;sarietal.,2017;seidetal.,2008;steinetal.,2018;vanwycketal.,2009.。目前,虽然生化参数发生了变化,但尚无研究证明降低的磷酸盐水平对临床的任何短期影响,这一观点得到了支持。
11.美国(us)和欧盟(eu)的监督管理机构目前所持的立场是,fcm相关的低磷血症是短暂的、无症状的并且与临床无关。虽然在2007年的一封非批准函中,美国fda将临床上重要的低磷血症列为三种潜在安全性风险之一,为了验证产品的安全性,需要通过额外的临床数据来解决,但的出资人随后提交的数据使该机构在2013年得出结论,非批准函中提出的所有临床(效力和安全性)问题,包括临床上重要的低磷血症问题已得到圆满解决(u.s.federal drug administration center for drug evaluation and research,申请号:203565orig1s000,summary review 2013).。目前批准的标签中也反映了与fcm相关的低磷血症是轻度和短暂的观点,其中将低磷血症列为副作用,但没有提供与低磷血症有关的特别警告,也没有提供短期或长期后果。相反,除了将其列为副作用以外,在欧盟产品特征摘要(eu summary of product characteristics,smpc)(其形成fcm在欧洲监管批准的一部分)中唯一提到低磷血症的是以下声明:“在临床试验中,最低血清磷值是在大约2周后得到的,并且铁注射治疗后的4至12周该值已恢复到基线范围以内”。
12.成纤维细胞生长因子23(fibroblast growth factor 23,fgf23)是一种调节磷酸盐和维生素d体内平衡的骨细胞衍生的性激素。其经过蛋白水解切割并最后得到未裂解的混合物,即完整的fgf23(ifgf23)和它的裂解片段在体内被发现。由于对静脉注射铁响应的血清磷酸的盐降低被认为是由fgf23的急性增加所介导的,wolf等人研究了铁缺乏的影响,及其快速纠正对于患有的缺铁性贫血女性的c端和完整的fgf23水平的影响,所述缺铁性贫血是子宫大出血继发的缺铁性贫血。其研究结果表明铁缺乏提高c端fgf23(cfgf23)的水平,并且fcm暂时提高了ifgf23的水平并降低血清磷酸盐(wolfetal.,2013;wo2013/134273a1.)。
13.我们惊奇地发现,与本领域的一般理解相反,按照现行方法使用fcm进行治疗会导致直接的临床后果,例如降低的肌肉功能和升高的骨周转。此外,我们还发现,现行的间隔一周重复fcm的剂量给药的相关方法导致对ifgf23的自协同效应,相比于第一剂量,第二剂量具有2
‑
3倍的增长。
14.基于这样的认知,显然需要改进的方法,在基础的id或ida的治疗中使用fcm,该方法大幅降低ifgf23诱发后果的风险,例如降低的肌肉功能和升高的骨周转。这些以及其他fcm治疗产生的ifgf23诱发的代谢、营养和肌肉骨骼后果将在以下称为ifgf23介导的或ifgf23诱发的副作用。
技术实现要素:
15.在本发明的一个方面,使用羧基麦芽糖铁的治疗可以在不损失效力的情况下完成,但通过调整给药fcm的时间和/或给药量以避免自协同效应,降低ifgf23介导的副作用风险。
16.在本发明的第二个方面,不仅基于通常用于确定iv铁的可行性的标准(即id或ida的诊断以及耐受或吸收口服铁能力的可能的缺乏),还基于更低可能地遭受ifgf23介导的副作用,选择使用羧基麦芽糖铁治疗的病人。
17.在本发明的第三个方面,对已经给药第一剂量的羧基麦芽糖铁的个体进行监测,以确定所述个体是否或何时可以给药第二剂量的羧基麦芽糖铁。
18.在本发明的第四个方面,识别具有降低的fgf23介导的副作用风险的个体。
19.在本发明的第五个方面,羧基麦芽糖铁与支持药物联合使用以减缓或减少ifgf23介导的副作用的影响。
20.根据这些方面,本发明特别涉及治疗铁缺乏的治疗方法,其包括根据个体的确定的治疗方案和/或选定的亚组给药羧基麦芽糖铁;监测已经给药第一剂量的fcm的个体以调整进一步给药fcm的时间和/或给药量的诊断方法,或识别适合于本发明的治疗方法的个体的诊断方法;fcm与其他药物的组合,其他药物减缓或减少ifgf23介导的副作用。
21.在所述的第一方面的第一个实施方案中,本发明涉及一种治疗铁缺乏的方法,所述方法包括给药第一剂量和第二剂量的羧基麦芽糖铁,其中第一剂量和第二剂量之间的时间为至少10天。
22.在所述的第一方面的第二个实施方案中,本发明涉及一种治疗铁缺乏的方法,其包括给药第一剂量和第二剂量的羧基麦芽糖铁,其中第一剂量和第二剂量的各自的元素铁不超过500mg。
23.在所述的第一方面的第三个实施方案中,本发明涉及一种治疗铁缺乏的方法,其包括给药单剂量或多剂量的羧基麦芽糖铁,其中12个月内给药的元素铁的总量不超过5000mg。
24.在所述的第二方面的第一个实施方案中,本发明涉及一种治疗铁缺乏的方法,其包括给药羧基麦芽糖铁,其中具有降低的fgf23介导的副作用风险的个体具有本文公开的血液参数。
25.在所述的第二方面的第二个实施方案中,本发明涉及一种治疗铁缺乏的方法,其包括给药羧基麦芽糖铁,其中具有降低的fgf23介导的副作用风险的个体的特征在于,不存在本文公开的淘汰标准。
26.在所述的第二方面的第三个实施方案中,本发明涉及一种治疗铁缺乏的方法,其包括给药羧基麦芽糖铁,其中具有降低的fgf23介导的副作用风险的个体的特征在于,其呼吸容量如本文所公开。
27.在所述的第三方面的第一个实施方案中,本发明涉及一种监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液或尿液参数:(1)血清磷酸盐水平,(2)血清维生素d水平,(3)血清离子钙水平,(4)血清pth水平以及(5)尿磷酸盐排泄分数(fractionary urinary phosphate excretion),其中如果至少一个血液或尿液参数如本文所公开,则可以向所述个体给药第
二剂量的羧基麦芽糖铁。
28.在所述的第三方面的第二个实施方案中,本发明涉及一种监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液参数:(1)血清骨特异性碱性磷酸酶水平(bone specific alkaline phosphatase level),(2)血清碱性磷酸酶水平(serum alkaline phosphatase level),(3)血清i型胶原n端前肽(pinp)水平(serum n
‑
terminal propeptide of type i collagen(pinp)level)以及(4)血清羧基末端胶原交联(serum carboxy
‑
terminal collagen crosslinks,ctx)水平,其中如果至少一个血液参数如本文所公开,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
29.在所述的第三方面的第三个实施方案中,本发明涉及一种监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包括确定所述个体的呼吸容量,其中如果所述呼吸容量如本文所公开,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
30.在所述的第四方面的第一个实施方案中,本发明涉及一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液或尿液参数:(1)血清磷酸盐水平,(2)血清维生素d水平,(3)血清离子钙水平,(4)血清pth水平以及(5)尿磷酸盐排泄分数,其中如果至少一个血液或尿液参数如本文所公开,则所述个体具有降低的fgf23介导的副作用风险。
31.在所述的第四方面的第二个实施方案中,本发明涉及一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液参数:(1)血清骨特异性碱性磷酸酶水平,(2)血清碱性磷酸酶水平,(3)血清i型胶原n端前肽(pinp)水平以及(4)血清羧基末端胶原交联(ctx)水平,其中如果至少一个血液参数如本文所公开,则所述个体具有降低的fgf23介导的副作用风险。
32.在所述的第四方面的第三个实施方案中,本发明涉及一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括确定所述个体的特征是否在于以下的一个或多个,特别地,所有的淘汰标准:
33.(1)接受过减肥手术;
34.(2)肥胖;
35.(3)心律失常风险增加的心脏病症;
36.(4)原发性或继发性甲状旁腺机能亢进;
37.(5)肺部疾病,例如哮喘或慢性阻塞性肺病(copd)
38.(6)导致低磷血症的遗传性疾病,例如x
‑
连锁低磷血症、常染色体显性低血磷性佝偻病(autosomal dominant hypophosphatemic ricket)、常染色体隐性低血磷性佝偻病(autosomal recessive hypophosphatemic ricket);
39.(7)继发性低磷血症或者肿瘤诱发的低磷血症;
40.(8)骨骼疾病,例如骨质疏松症或骨软化症(osteomalacia);以及
41.(9)给药铁1天至2个月以内安排手术,其中如果所述个体的特征在于不存在一个或多个,特别地,不存在所有的所述的淘汰标准,则所述个体具有降低的fgf23介导的副作用风险。
42.在所述的第四方面的第四个实施方案中,本发明涉及一种识别具有降低的fgf23
介导的副作用风险的个体的方法,其包括确定所述个体的呼吸容量(respiratory capacity),其中如果所述呼吸容量如本文所公开,则所述个体具有降低的fgf23介导的副作用风险。
43.在所述的第五方面的第一个实施方案中,本发明涉及一种羧基麦芽糖铁与一种或多种额外药物的组合,其中,所述额外药物选自:
44.(1)维生素d,例如钙化三醇;
45.(2)磷酸盐,例如葡萄糖
‑1‑
磷酸、磷酸钙或磷酸钠;和
46.(3)抗fgf23拮抗抗体,例如burosumab。
附图说明
47.图1为表格,其汇总了用于研究ida
‑
04的低磷血症(主要终点)的发生的分析。
48.图2为表格,其汇总了用于研究ida
‑
05的低磷血症(主要终点)的发生的分析。
49.图3示出了每次访视时,磷酸盐水平≤2.0mg/dl的发病率(ida
‑
04和ida
‑
5组合;fcm:左侧的条,iim:右侧的条)。
50.图4示出了每次访视时,磷酸盐水平≤1.0mg/dl的发病率(ida
‑
04和ida
‑
5组合;fcm:左侧的条,iim:右侧的条)。
51.图5示出了随时间变化的平均绝对磷酸盐水平(ida
‑
04和ida
‑
5组合)。
52.图6示出了ifgf23随时间的变化(ida
‑
04)。
53.图7示出了ifgf23随时间的变化(ida
‑
05)。
54.图8示出了cfgf23随时间的变化(ida
‑
04)。
55.图9示出了cfgf23随时间的变化(ida
‑
05)。
56.图10示出了部分尿磷酸盐排泄随时间的变化(ida
‑
04和ida
‑
05组合)。
57.图11示出了维生素d水平随时间的相对基线的平均变化和绝对变化(ida
‑
04和ida
‑
05组合)。
58.图12示出了完整的甲状旁腺激素水平随时间的相对基线的变化和绝对变化(ida
‑
04和ida
‑
05组合)。
59.图13示出了钙离子随时间的相对基线的变化和绝对变化(ida
‑
04和ida
‑
05组合)。
60.图14示出了肌肉功能和骨周转的几个标记物随时间的平均变化(ida
‑
04和ida
‑
05组合)。
61.图15示出了呼吸肌肉力量随时间的平均变化(ida
‑
04和ida
‑
05组合)。
具体实施方式
62.本发明描述了治疗铁缺乏的治疗方法,其包括给药铁碳水化合物复合物,监测已经给药第一剂量的铁碳水化合物复合物的个体的方法,识别适合于本发明的治疗方法的个体的方法以及铁碳水化合物复合物与额外药物的组合,其中所述铁碳水化合物复合物诱导治疗中的个体的ifgf23水平的显著(例如,统计学上显著的)提升。因此本发明的方法适用于具有如下机理的复合物,其诱导ifgf23的显著升高,并因此可以降低血清磷酸盐水平,从而导致低磷血症。尽管这不包括欧洲和美国通常使用的其他的iv铁药物,例如蔗糖铁葡萄糖酸铁异麦芽糖苷铁或葡聚糖铁(
和),但包括亚太地区某些复合物,包括在日本可用的含糖氧化铁如(尽管名称相似,但与中的蔗糖铁不同),一些种类的多聚麦芽糖铁和以上所有羧基麦芽糖铁(fcm)。临床试验和病例报告结果表明,ifgf23介导的血清磷酸盐水平降低和低磷血症发展的最大风险与多聚麦芽糖铁、含铁氧化物和以上所有羧基麦芽糖铁有关。例如参见wolfetal.,2013。
63.因此,本发明优选的铁碳水化合物复合物是羧基麦芽糖铁(fcm)。本文所用的术语“羧基麦芽糖铁”是指包含铁(例如铁氧化物氢氧化物)和羧基麦芽糖的胶体复合物。羧基麦芽糖基于羧基化的淀粉或淀粉衍生物(即修饰为包含羧基,例如通过氧化醛的末端基团)。通过氧化麦芽糖糊精获得一种特定的羧基麦芽糖铁,例如,如wo2007/081744a1中描述的vit
‑
45和wo2004/037865a1所描述的。羧基麦芽糖铁的优选的实例是在美国可以商购的商品名为的羧基麦芽糖铁,以及在欧盟和许多其他国家可以商购的商品名为的羧基麦芽糖铁。
64.术语
65.为了本发明可以更容易理解,首先对某些术语进行定义。详细说明中还列出了其他定义。
66.个体的“治疗”和“疗法”是指对个体进行的任何类型的干预或过程,或对个体给药活性试剂,其目的是逆转、减轻、改善、抑制、减缓或预防与疾病相关的症状、并发症、病症或生化指标的发生、进展、发展、恶化或复发。
[0067]“个体”包括任何人类或非人类动物。术语“非人类动物”包括但不限于脊椎动物例如非人类灵长类、羊、狗和啮齿类,例如小鼠、大鼠和豚鼠。在优选的实施方案中,所述个体是人。术语“个体”和“病人”在此可以互换使用。
[0068]
药物或治疗剂的“治疗有效量”或“治疗有效剂量”是指任何剂量的药,当单独使用或与另一个治疗剂联合使用时,保护个体抵御疾病的发生,或通过疾病症状严重程度的降低、疾病无症状期的频率和持续时间的增加或预防由于疾病痛苦产生的损伤或残疾证实,促进疾病的退化。治疗剂促进疾病退化的能力可以使用本领域技术人员熟知的多种的方法评估,例如在临床试验期的人类个体、在动物模型系统中预测对人的有效性或在体外试验中测定试剂的活性。
[0069]“成纤维细胞生长因子23(fgf23)”是一种调控磷酸盐和维生素d平衡的骨细胞衍生的激素。fgf23经过蛋白水解切割,结果在体内发现未切割的(即完整的fgf23(ifgf23))片段与其裂解片段的混合物。完整形式的ifgf23是与磷酸盐代谢相关的活性形式,其控制尿液中的磷酸盐排泄,ifgf23水平的升高会导致尿液中磷酸盐的消耗。目前主要存在两种抗体检测方法,一种是只捕获ifgf23,另一种是与激素的c末端结合,从而同时捕获ifgf23和c端片段。因此,后一个度量中,cfgf23是完整的fgf23和c端fgf23片段的总和的度量。因此,存在两种与fgf23相关的检测,即ifgf23和cfgf23,其具有不同的解释。
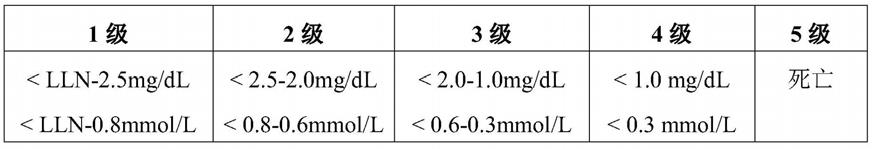
[0070]“低磷血症”是一种以过低的血清磷酸盐水平为特征的疾病。不良反应通用术语标准(the common terminology criteriafor adverse events,ctcae)4.0版提供了四个等级的低磷血症。
[0071][0072]
lln是特定实验室使用的正常范围的下限。
[0073]
除非有特定说明,本文所用的低磷血症发病率是指血清磷酸盐水平低于2mg/dl。
[0074]
本文所用的术语“血清磷酸盐(s
‑
phosphate)”是指血清血液中无机磷的水平,其通过具有式(nh4)3[po4](moo3)
12
的磷钼酸复合物测量,在硫酸的存在下,所述磷钼酸复合物由无机磷与钼酸铵反应形成。使用roche modular和cobas analyzer,在光谱的紫外区(340nm),光度法测定所述复合物。
[0075]
本文所用的术语“血清维生素d”是指血液血清中的维生素d的水平,特别是25
‑
羟基维生素d、1,25
‑
二羟基维生素d和24,25
‑
二羟基维生素d,其通过液相色谱和串联质谱(lc
‑
ms/ms)测定。
[0076]
本文所用的术语“血清离子钙”是指血液血清中钙离子(ca
2
)的水平,其使用ilgem premier 3500pak试剂盒进行测量。核心部件是传感器卡,其提供一个低容量的气密腔室,其中,血液样本呈现至传感器。ph和电解质传感器都基于离子选择性电极的原理;即,可以在膜上建立电势,所述膜可选择性地渗透特定的离子。ph和电解质传感器为基于聚氯乙烯(pvc)的离子选择性电极,其由内部的ag/agcl参比电极和内部盐层组成。相对于卡参比电极测量所述电势。
[0077]
本文所用的术语“血清甲状旁腺激素(pth)”是指血液血清中的血清甲状旁腺激素水平,其使用两点夹心免疫测定法,利用直接化学发光技术测定,所述方法使用恒定量的两种抗人pth抗体。甲状旁腺产生的pth是调节细胞外钙浓度的主要循环因子。异常低的离子钙浓度会触发pth的分泌。pth分子与目标组织的1型pth受体结合,并引发一系列反应,导致细胞外钙浓度增加。pth刺激破骨细胞骨重吸收,导致钙从骨中释放。pth刺激肾小管的跨细胞钙重吸收,并刺激肾脏产生1,25
‑
二羟基维生素d,其作用于肠道以提高钙的重吸收。在大多数临床条件下,细胞外钙水平的上升会通过负反馈机制抑制pth的分泌。
[0078]
术语“尿磷酸盐排泄分数(fepi)”(有时缩写为fepo4)是衡量肾脏未从前尿中重吸收的磷酸盐的量的量度,即,最终尿中的磷酸盐的量占个体血液中磷酸盐含量的比例。其是这样计算的:fepi=[po4(尿)*肌酐(血清)]/[po4(血清)*肌酐(尿)]*100。通常认为fepi为10
‑
20%(0.1
‑
0.2分数)是正常的;通常认为fepi<10%(<0.1分数)是低的;以及通常认为fepi>20%(>0.2分数)是高的。使用与测定血清中的磷酸盐相同的方法测定尿中的磷酸盐。
[0079]
本发明所用的术语“血清骨特异性碱性磷酸酶”是指血液血清中骨特异性碱性磷酸酶的水平,其使用beckman
‑
coulter ostase试验测定,所述测定方法为一步免疫酶化学发光试验,其使用对骨特异性碱性磷酸酶(bap)具有特异性的小鼠单克隆抗体。
[0080]
本文所用的术语“血清碱性磷酸酶”是指血液血清中碱性磷酸酶的水平,其使用roche modular analyzer,通过酶法测定。在镁和锌离子存在的情况下,对硝基苯磷酸酯被磷酸酶裂解为磷酸根和对硝基苯酚。释放的对硝基苯酚与碱性磷酸酶的活性成正比,并通过光度法测量。
[0081]
本文所用的术语“血清i型胶原n端前肽(pinp)”是指血液血清中pinp的水平,其使
用夹心原理、电化学发光免疫法(eclia),在cobas e601 analyzer上测定。在第一次孵育过程中,将样品中的pinp和生物素化的单克隆pinp特异性抗体一起孵育。在第二次孵育过程中,加入链霉亲和素包被标记的微粒和钌复合物(三(2,2
‑
双吡啶基)钌(ii)
‑
复合物(ru(bpy)23 ))标记的单克隆pinp特异性抗体,以形成夹心复合物,其通过生物素和链霉亲和素的相互作用与固相结合。反应混合物被吸入到测量池中,其中的微粒被磁力捕获至电极表面。在电极上施加电压,引起化学发光发射,通过光电倍增管测量化学发光发射。测量结果通过校准曲线确定,所述校准曲线由仪器特定生成,即通过2点校准和通过试剂条形码提供的主曲线生成。
[0082]
本文所述的术语“血清羧基末端胶原交联(ctx)”是指血液血清中ctx的水平,其使用夹心原理、电化学发光免疫法(eclia),在cobas e601 analyzer上测定。在第一次孵育过程中,50μl的样品和生物素化的单克隆抗
‑
β
‑
骨胶原交联(crosslaps)抗体一起孵育。在第二次孵育过程中,加入链霉亲和素包被标记的微粒和钌复合物标记的单克隆p
‑
β
‑
骨胶原交联特异性抗体,以形成夹心复合物,其通过生物素和链霉亲和素的相互作用与固相结合。反应混合物被吸入到测量池中,其中的微粒被磁力捕获至电极表面。然后使用procell除去未结合的物质。在电极上施加电压,引起化学发光发射,通过光电倍增管测量化学发光发射。测量结果通过校准曲线确定,所述校准曲线由仪器特定生成,即通过2点校准和通过试剂条形码提供的主曲线生成。
[0083]
本文所用的术语“血清肌酸激酶(ck)”是指血液血清中的ck水平,其使用roche modular和cobas analyzers,通过酶法测定。ck催化磷酸肌酸对adp的磷酸化。atp使得葡萄糖磷酸化,产生的葡萄糖
‑6‑
磷酸将nadp 转化为nadph。形成nadph的速率与ck的活性成正比,其用光度法测定。ck是一种酶,其催化磷酸盐的由atp向肌酸的可逆转移。这使得高能磷酸盐可以更稳定的形式储存在atp中。ck在骨骼肌、心肌、甲状腺、前列腺和大脑中含量较高;在肝、肾、肺和其他组织中仅少量存在。因此,血清ck活性的提高主要归因于横纹肌(骨骼的或心脏的)的损伤,在少数情况下,归因于大脑的损伤。经常可以根据临床理由区分这些不同的疾病,但也有不能区分的情况。ck同工酶的测定有助于解决该问题。
[0084]
本文所用的术语“血清铁蛋白”是指血液血清中铁蛋白的水平,其使用双位免疫酶法(“夹心”试验)测定。铁蛋白是人体的主要储铁蛋白。铁蛋白的浓度直接与人体铁总储量成正比,因此血清铁蛋白水平成为评估铁状态的常用诊断工具。缺铁性贫血的病人的血清铁蛋白水平约为正常个体的十分之一,而铁过载(血色病、含铁血黄素沉着症)病人的血清铁蛋白水平远高于正常个体。铁蛋白水平还提供了一种早期检测铁缺乏的灵敏手段。无论是成人还是儿童,慢性炎症导致与铁储存相关的铁蛋白水平的不成比例的增加。急性和慢性肝病、慢性肾衰竭和某些类型的肿瘤病都会观察到铁蛋白水平提升。
[0085]
需要注意的是,虽然上述血液参数是在血清中测定的,但同样也可以在血浆中测定。血清和血浆水平相关且可以相互转换。
[0086]
本文所用的术语“减肥手术”是指通过胃束带缩小胃的尺寸,或切除胃的一部分(袖状胃切除术或胆胰分流并十二指肠转位术),或通过切除小肠并将其重新导入小胃囊袋而达到减肥目的的外科手术。
[0087]“肥胖”是指具有如下特征的情况,体重过重,体重指数(bmi)超过30kg/m2,体重指数为一种度量,其通过一个人的体重除以身高的平方获得。
[0088]“心律失常风险增加的心脏病症”是指以心血管病症和风险因素为特征的病症,其增加了发生心律失常或心律异常的可能,增加心律失常风险的心脏病症包括但不限于:冠状动脉疾病、心内膜炎、瓣膜性心脏病、高血压、糖尿病和肥胖。
[0089]“原发性或继发性甲状旁腺机能亢进”是一种病症,其特征在于甲状旁腺素分泌过多。
[0090]“哮喘”是一种以慢性肺部疾病为特征的病症,其使得气道发炎、缩小气道,引起反复发作的喘息、胸闷、气短和咳嗽。
[0091]“慢性阻塞性肺病(copd)”是一种以慢性炎症性肺部疾病为特征的病症,其引起肺部气流受阻。
[0092]“x
‑
连锁低磷血症”是一种遗传性肾磷酸盐消耗失调症,其特征在于,血液中磷酸盐水平低、佝偻病和/或骨软化症和发育缓慢。
[0093]“常染色体显性或隐性低血磷性佝偻病”是一种由于血液中磷酸盐水平低,使骨骼变软且容易弯曲的病症。
[0094]“继发性低磷血症”是一种由于口服摄入量减少或肠道吸收减少,使血液中磷酸盐水平低的病症。
[0095]“肿瘤诱发的低磷血症”是一种病症,其特征在于,肿瘤(例如产生fgf23的肿瘤)继发的血液中磷酸盐水平低。
[0096]“骨质疏松症”是一种病症,其特征在于,当身体失去过多骨质、制造太少骨质或两者皆有时会发生骨骼疾病,其导致骨骼变得脆弱。
[0097]“骨软化症”是一种病症,其特征在于,主要原因为可用磷酸盐、钙和维生素d水平不足,或由于钙的重吸收导致骨代谢受损,从而引起骨质的软化。骨代谢障碍导致骨矿化不足。
[0098]“给药铁1天至2个月以内安排手术”的个体是指,会在给药铁1天至2个月以内进行手术。
[0099]
本发明为了本发明的目的,当以mg或g指定铁碳水化合物的剂量时,与文献中的做法一致,该值是指以mg为单位的提供的元素铁的量。
[0100]
a.治疗方法
[0101]
本文描述了治疗铁缺乏的治疗方法,其包括根据确定的治疗方案和/或选定的个体的亚组给药羧基麦芽糖铁。因此,本发明还涉及上述方法中使用的羧基麦芽糖铁、羧基麦芽糖铁用于治疗铁缺乏的用途以及或羧基麦芽糖铁在制备用于治疗铁缺乏的药物中的用途。
[0102]
i.给药方案
[0103]
根据本发明这方面的第一实施方案,治疗铁缺乏的方法包括重复给药铁碳水化合物复合物,特别是fcm,其特征在于,第一和第二剂量之间的时间为至少10天。例如,如果第一剂量在第0天给药,则第二剂量在第10天或之后给药。优选地,第一和第二剂量之间的时间为至少14天、18天、21天、28天、35天、42天、49天或56天。在某些情况下,第一和第二剂量之间的时间甚至可以为至少3个月或6个月。
[0104]
元素铁的每日给药剂量是治疗有效量,其可以为500mg至1000mg,例如,为500mg、750mg或1000mg元素铁。
[0105]
特别地,所述剂量为每日一次的剂量。例如,典型的羧基麦芽糖铁的每日一次的剂量为500mg、750mg或1000mg元素铁。对于重复给药,在第一剂量750mg元素铁之后给药第二剂量750mg元素铁,或第一剂量1000mg元素铁之后给药500mg至1000mg元素铁,例如,500mg、750mg或1000mg元素铁。随后可能会给药更多剂量的fcm。
[0106]
根据本发明这方面的第二实施方案,治疗铁缺乏的方法包括重复给药铁碳水化合物复合物,特别是fcm,其特征在于,第一和第二剂量各自不超过、或为500mg以下的元素铁。示例性的量包括500mg、400mg、300mg、200mg和100mg。
[0107]
根据本发明这方面的第三实施方案,治疗铁缺乏的方法包括给药铁碳水化合物复合物,特别是fcm,其特征在于,12个月内给药的元素铁的总量不超过5000mg。优选地,12个月内给药元素铁的总量不超过4000mg、3000mg或2000mg。
[0108]
ii.选定的个体亚组
[0109]
本发明的方法通常在有需要的个体上实施。需要本发明方法的个体是指具有、诊断为、怀疑具有或有发生铁缺乏风险的个体,特别是与如下相关的铁缺乏,慢性失血、急性失血、妊娠、分娩、哺乳、儿童发育、子宫大出血、月经、消化道出血、慢性内出血、炎症性肠病、充血性心力衰竭、不安腿综合征、寄生虫感染、例如由于慢性肾病或肾衰竭、透析、手术、慢性药剂(例如酒精、水杨酸盐、类固醇、非类固醇抗炎药、红细胞生成刺激剂(esas)或抑制铁吸收的药物)摄入引起的肾功能丧失或受损。铁储存耗尽时会发生缺铁性贫血(ida)。患有id的病人可能患有ida;患有ida的病人必然患有id。在本领域已很好地建立了诊断id和ida的方法,并在临床实践中普遍使用。
[0110]
如果个体对口服铁剂不耐受或无效,具有、诊断为、怀疑具有或有发生铁缺乏风险的个体将被给予铁碳水化合物复合物的形式的iv铁,特别是羧基麦芽糖铁。另一种指定iv铁的情形是需要快速输铁。
[0111]
适于本发明治疗的一组特别的个体的特征在于,具有降低的fgf23介导的副作用风险。
[0112]
根据本发明这方面的第一实施方案,具有降低的fgf23介导的副作用风险的个体具有选自如下的血液或尿液参数:
[0113]
(1)正常的血清磷酸盐水平,特别地,>2.5mg/dl;
[0114]
(2)正常的血清维生素d水平,特别地,1,25
‑
二羟基维生素d在以下范围以内:男性:<16岁:24
‑
86pg/ml,≥16岁:18
‑
64pg/ml,女性:<16岁:24
‑
86pg/ml,≥16岁:18
‑
78pg/ml;
[0115]
(3)正常的血清离子钙水平,特别地,1.16
‑
1.32mmol/l;
[0116]
(4)正常的血清pth水平,特别地,15
‑
65pg/ml;
[0117]
(5)正常的尿磷酸盐排泄分数,特别地,10%
‑
20%(0.1
‑
0.2分数)的fepi;以及
[0118]
(6)(1)、(2)、(3)、(4)和(5)的组合。
[0119]
根据本发明这方面的第二实施方案,具有降低的fgf23介导的副作用风险的个体具有选自如下的血液参数:
[0120]
(1)正常的血清骨特异性碱性磷酸酶水平,特别地,6.5
‑
22.4u/l;
[0121]
(2)正常的血清碱性磷酸酶水平,特别地,31
‑
140u/l;
[0122]
(3)正常的血清i型胶原n端前肽(pinnp)水平,特别地,15.13
‑
85.50ng/ml;
[0123]
(4)正常的血清羧基末端胶原交联(ctx)水平,特别地,0.03
‑
1.01ng/ml;以及
[0124]
(5)(1)、(2)、(3)和(4)的组合。
[0125]
根据本发明这方面的第三实施方案,具有降低的fgf23介导的副作用风险的个体的特征在于,不存在以下的一项或多项,特别是所有的淘汰标准:
[0126]
(1)接受过减肥手术;
[0127]
(2)肥胖;
[0128]
(3)心律失常风险增加的心脏病症;
[0129]
(4)原发性或继发性甲状旁腺机能亢进;
[0130]
(5)肺部疾病,例如哮喘或慢性阻塞性肺病(copd)
[0131]
(6)导致低磷血症的遗传性疾病,例如x
‑
连锁低磷血症、常染色体显性低血磷性佝偻病、常染色体隐性低血磷性佝偻病;
[0132]
(7)继发性低磷血症或者肿瘤诱发的低磷血症;
[0133]
(8)骨骼疾病,例如骨质疏松症或骨软化症;以及
[0134]
(9)给药铁1天至2个月以内安排手术,例如优选给药铁1到3周以内安排手术。
[0135]
根据本发明这方面第四实施方案,具有降低的fgf23介导的副作用风险的个体的特征在于,正常的呼吸容量,其测量为最大呼气压力和最大吸气压力,特别地,最大呼气压力为:男性:≥117
‑
(0.83x年龄)cm h2o,女性:≥95
‑
(0.57x年龄)cm h2o;和/或最大吸气压力:男性:≥62
‑
(0.15x年龄)cm h2o,女性:≥62
‑
(0.50x年龄)cm h2o。
[0136]
根据第五方面,具有降低的fgf23介导的副作用风险的个体具有本发明公开的血液/尿液参数并且其特征在于,不存在本发明公开的淘汰标准。
[0137]
根据第六方面,具有降低的fgf23介导的副作用风险的个体具有本发明公开的血液/尿液参数,其特征在于,不存在本发明公开的淘汰标准,并且其特征在于,本发明公开的正常的呼吸容量。
[0138]
适于本发明的治疗的另一组特别的个体是患有慢性肾病(ckd)的个体。铁治疗后,在慢性肾病(ckd)病人中出现低磷血症的频率低得多,慢性肾病病人的肾功能受损,因此排泄尿液中磷酸盐的能力受损,结果倾向于患上高磷血症(磷酸盐过高)。另一方面,由于高磷血症的倾向,ckd病人倾向于具有非常高的fgf23水平功能,这是由于机体不断尝试通过产生ifgf23以提高经肾脏的磷酸盐的尿排泄分数来抵消高血清磷酸盐水平。因此,在ckd病人中,ifgf23水平升高,结果尽管低磷酸血症的风险较低,但ifgf23的其他下游效应可能会更明显。
[0139]
b.诊断方法
[0140]
本发明进一步描述了监测已经给药第一剂量的铁碳水化合物复合物的个体的方法,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液或尿液参数:(1)血清磷酸盐水平,(2)血清维生素d水平,(3)血清离子钙水平,(4)血清pth水平以及(5)尿磷酸盐排泄分数,其中如果至少一个血液或尿液参数如本文所公开,则可以向所述个体给药第二剂量的铁碳水化合物复合物。
[0141]
本发明进一步描述了监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁其包括从所述个体获得的生物样品中确定至少一个选自如下的血液参数:(1)血清骨特异性碱性磷酸酶水平,(2)血清碱性磷酸酶水平,(3)血清i型胶原n端前肽(pinp)水平
以及(4)血清羧基末端胶原交联(ctx)水平,其中如本发明所公开的,如果至少一个血液参数是正常的,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
[0142]
本发明还进一步描述了监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包括确定所述个体的呼吸容量,其中如本发明所公开的,如果所述呼吸容量是正常的,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
[0143]
本发明还描述了识别适合本发明的治疗方法的个体的方法。这样的方法包扩识别具有降低的fgf23介导的副作用风险的个体的方法,其包扩从所述个体获得的生物样品中确定至少一个选自如下的血液或尿液参数:(1)血清磷酸盐水平,(2)血清维生素d水平,(3)血清离子钙水平,(4)血清pth水平和(5)尿磷酸盐排泄分数,其中如本发明所公开的,如果至少一个血液或尿液参数正常的,则所述个体具有降低的fgf23介导的副作用风险。
[0144]
本发明进一步描述了识别具有降低的fgf23介导的副作用风险的个体的方法,其包括从所述个体获得的生物样品中测定至少一个选自如下的血液参数:(1)血清骨特异性碱性磷酸酶水平,(2)血清碱性磷酸酶水平,(3)血清i型胶原n端前肽(pinp)水平和(4)血清羧基末端胶原交联(ctx)水平,其中,如本发明所公开的,如果至少一个血液或尿液参数是正常的,则所述个体具有降低的fgf23介导的副作用风险。
[0145]
本发明还进一步描述了识别具有降低的fgf23介导的副作用风险的个体的方法,其包括确定所述个体的特征是否在于以下的一个或多个,特别地,所有的淘汰标准:
[0146]
(1)接受过减肥手术;
[0147]
(2)肥胖;
[0148]
(3)心律失常风险增加的心脏病症;
[0149]
(4)原发性或继发性甲状旁腺机能亢进;
[0150]
(5)肺部疾病,例如哮喘或慢性阻塞性肺病(copd)
[0151]
(6)导致低磷血症的遗传性疾病,例如x
‑
连锁低磷血症、常染色体显性低血磷性佝偻病、常染色体隐性低血磷性佝偻病;
[0152]
(7)继发性低磷血症或者肿瘤诱发的低磷血症;
[0153]
(8)骨骼疾病,例如骨质疏松症或骨软化症;以及
[0154]
(9)给药铁1天至2个月以内安排手术,其中如果所述个体的特征在于不存在一个或多个,特别地,不存在所有淘汰标准,则所述个体具有降低的fgf23介导的副作用风险。
[0155]
并且本发明还描述了识别具有降低的fgf23介导的副作用风险的个体的方法,其包括确定所述个体的呼吸容量,其中如本发明所公开的,如果所述呼吸容量是正常的,则所述个体具有降低的fgf23介导的副作用风险。
[0156]
生物样品可以是获得自个体的任何样品,其中样品可以确定所述的血液或尿液参数。在一些实施方案中,生物样品包括血液样品。在一些实施方案中,生物样品包括血浆样品。在优选的实施方案中,生物样品包括血清样品。在其他优选的实施方案中,生物样品包括尿液样品。由于诊断方法在个体的样品上实施,因此这些方法在离体条件下实施,特别是体外。
[0157]
生物样品可以通过本领域已知的任何方法收集和/或获得。在一些实施方案中,生物样品直接从个体获得,例如直接从个体的循环系统中取出样品。在其他的实施方案中,生物样品从实验室获得,其中实验室或前人先前直接从个体获得生物样品。在一些实施方案
中,生物样品是新鲜的,例如,样品没有被冷冻或长时间储存。在其他实施方案中,生物样品已在37℃以下的温度下储存。
[0158]
在一些实施方案中,本发明的监测和识别个体的诊断方法进一步包括向识别为可以给药第二剂量铁碳水化合物复合物和/或具有降低的fgf23介导的副作用风险的个体给药铁碳水化合物复合物,特别是羧基麦芽糖铁。本发明公开的关于给药方案和选定的病人亚组适用于这方面。
[0159]
c.药物组合
[0160]
本发明进一步描述了fcm与一种或多种额外药物的组合,所述组合用于治疗治疗铁缺乏,其中所述额外药物选自:
[0161]
(1)维生素d;
[0162]
(2)磷酸盐;和
[0163]
(3)抗fgf23拮抗抗体。
[0164]
fcm导致活性维生素d、1,25
‑
二羟基维生素d的减少,以及24,25
‑
二羟基维生素d的增加。给药治疗有效量的维生素d有助于减少这种影响。为此,优选给药阿法骨化醇,特别是钙化三醇。或者,可以给药胆钙化醇或麦角钙化醇。
[0165]
如果给药阿法骨化醇或钙化三醇,可在给药第一fcm剂量前3天内给药。或者,可在给药第一fcm剂量的同一天开始给药阿法骨化醇或钙化三醇。还可以进一步选择在给药第一fcm剂量后的第1天、第2天、第3天、第4天、第5天、第6天或第7天,或第14天开始给药阿法骨化醇或钙化三醇。
[0166]
钙化三醇适合以每日0.125μg至2μg的剂量给药,例如0.125μg至1μg,例如0.25μg至0.75μg,例如0.5μg。
[0167]
阿法骨化醇适合以每日0.25μg至5μg的剂量给药,例如0.5μg至2μg,例如1μg。
[0168]
无论是作为fcm给药的前治疗进行给药,或在fcm给药后进行给药,都要继续使用钙化三醇或阿法骨化醇治疗,直到血液参数特别是维生素d水平正常,或直到治疗开始后的3周、4周、5周或6周,以较早发生者为准。
[0169]
优选在使用fcm治疗之前给药胆钙化醇或麦角钙化醇,例如在给药第一fcm剂量之前的14天、7天、6天,或者5天、4天、3天、2天、1天。
[0170]
胆钙化醇适合以每周140μg至2500μg的剂量进行给药,例如优选300μg
‑
600μg,例如优选500μg。
[0171]
麦角钙化醇适合以每日10μg至1250μg剂量进行给药,例如优选500μg。
[0172]
在本发明的一个实施方案中,给药本发明所述的第一fcm剂量之前使用胆钙化醇或麦角钙化醇进行前治疗,然后在给药本发明所述的第一fcm剂量之后使用阿法骨化醇或钙化三醇进行治疗。
[0173]
由于fcm也会导致血清磷酸盐的减少,给药治疗有效量的磷酸盐可以有助于减少这样的影响。例如,可以口服或静脉注射(iv)给药葡萄糖
‑1‑
磷酸或磷酸盐,例如磷酸钙,磷酸钾或磷酸钠。
[0174]
用于iv给药的治疗有效量的磷酸盐包括单次剂量,优选每日单次剂量为10mmol至50mmol,例如30mmol至40mmol,特别地,为15mmol至35mmol的磷酸盐,可重复给药直到血清磷酸盐正常。
[0175]
用于口服给药的治疗有效量的磷酸盐包括单次剂量,优选每日单次剂量为15mmol至85mmol,例如30mmol至65mmol,特别地,为45mmol至50mmol的磷酸盐,可重复给药直到血清磷酸盐正常。
[0176]
根据本发明的一个特别的实施方案,使用额外药物的组合。特别优选地,为维生素d和磷酸盐的组合。
[0177]
抗
‑
fgf23抗体用于治疗非常罕见的疾病,例如x
‑
连锁低磷血症。第一个上市的此类产品是burosumab。优选地,将抗
‑
fgf23抗体用于给药fcm之后出现非常严重的fgf23介导的副作用的病人,例如血清磷酸盐水平低于1mg/dl或ifgf23水平相对于基线提高100pg/ml或更多。
[0178]
根据一个优选的实施方案,额外药物为口服给药。如果额外药物为磷酸盐,例如葡萄糖
‑1‑
磷酸磷酸钙或磷酸钠,或维生素d,例如钙化三醇,是特别有利的。
[0179]
根据一个特定的实施方案,在给药第一剂量的fcm前,给药额外药物。如果额外药物是胆钙化醇或麦角钙化醇,是特别有利的。
[0180]
根据另一个特定的实施方案,在给药第一剂量的fcm之后,但在给药第二剂量之前,给药额外的药物。如果额外药物是钙化三醇或阿法骨化醇,是特别有利的。如果使用磷酸盐作为额外药物,同样优选地,在给药第一剂量的fcm给药之后,给药额外的药物。
[0181]
额外的药物的剂量通常是指成人的药物给药量。给药婴儿的剂量可作相应地调整。
[0182]
示例性实施方案
[0183]
1.一种治疗铁缺乏的方法,其包括给药第一剂量和第二剂量的羧基麦芽糖铁,其中所述第一剂量和所述第二剂量之间的时间为至少10天。
[0184]
2.实施方案1所述的方法,其中所述第一和第二剂量之间的时间为至少14天、18天、21天、28天、35天、42天、49天或56天。
[0185]
3.实施方案1所述的方法,其中所述第一和第二剂量之间的时间为至少3个月或6个月。
[0186]
4.实施方案1
‑
3中任意一项所述的方法,其中所述第一和第二剂量是每日单次剂量。
[0187]
5.实施方案1
‑
4中任意一项所述的方法,其中所述第一剂量是750mg的元素铁以及所述第二剂量是750mg的元素铁。
[0188]
6.一种治疗铁缺乏的方法,其包括给药第一剂量和第二剂量的羧基麦芽糖铁,其中所述第一和所述第二剂量各自的元素铁不超过或为500mg以下。
[0189]
7.一种治疗铁缺乏的方法,其包括给药一个或多个剂量的羧基麦芽糖铁,其中12个月内给药的元素铁的总量不超过5000mg。
[0190]
8.一种治疗铁缺乏的方法,所述方法包括向个体给药羧基麦芽糖铁,其中所述个体具有降低的fgf23介导的副作用风险。
[0191]
9.实施方案8所述的方法,其中具有降低的fgf23介导的副作用风险的个体具有选自如下的血液或尿液参数:
[0192]
(1)正常的血清磷酸盐水平,特别地,>2.5mg/dl;
[0193]
(2)正常的血清维生素d水平,特别地,1,25
‑
二羟基维生素d在以下范围以内:
[0194]
男性:<16岁:24
‑
86pg/ml,≥16岁:18
‑
64pg/ml,
[0195]
女性:<16岁:24
‑
86pg/ml,≥16岁:18
‑
78pg/ml;
[0196]
(3)正常的血清离子钙水平,特别地,1.16
‑
1.32mg/dl;
[0197]
(4)正常的血清pth水平,特别地,15
‑
65pg/ml;
[0198]
(5)正常的尿磷酸盐排泄分数,特别地,10%
‑
20%(0.1
‑
0.2分数)的fepi;以及
[0199]
(6)(1)、(2)、(3)、(4)和(5)的组合。
[0200]
10.实施方案8所述的方法,其中所述具有降低的fgf23介导的副作用风险的个体具有选自如下的血液参数:
[0201]
(1)正常的血清骨特异性碱性磷酸酶水平,特别地,为6.5
‑
22.4u/l;
[0202]
(2)正常的血清碱性磷酸酶水平,特别地,为31
‑
40u/l;
[0203]
(3)正常的血清i型胶原n端前肽水平,特别地,为15.13
‑
85.50ng/ml;
[0204]
(4)正常的血清羧基末端胶原交联(ctx)水平,特别地,为0.03
‑
1.01ng/ml;以及
[0205]
(5)(1)、(2)、(3)和(4)的组合。
[0206]
11.实施方案8所述的方法,其中所述具有降低的fgf23介导的副作用风险的个体的特征在于,不存在以下的一项或多项,特别是所有的淘汰标准:
[0207]
(1)接受过减肥手术;
[0208]
(2)肥胖;
[0209]
(3)心律失常风险增加的心脏病症;
[0210]
(4)原发性或继发性甲状旁腺机能亢进;
[0211]
(5)肺部疾病,例如哮喘或慢性阻塞性肺病(copd)
[0212]
(6)导致低磷血症的遗传性疾病,例如x
‑
连锁低磷血症、常染色体显性低血磷性佝偻病、常染色体隐性低血磷性佝偻病;
[0213]
(7)继发性低磷血症或者肿瘤诱发的低磷血症;
[0214]
(8)骨骼疾病,例如骨质疏松症或骨软化症;以及
[0215]
(9)给药铁1天至2个月以内安排手术。
[0216]
12.实施方案8所述的方法,其中所述具有降低的fgf23介导的副作用风险的个体的特征在于,正常的呼吸容量,其测量为最大呼气压力和/或最大吸气压力,特别地,
[0217]
最大呼气压力为:男性:≥117
‑
(0.83x年龄)cm h2o,女性:≥95
‑
(0.57x年龄)cm h2o;和/或
[0218]
最大吸气压力为:男性:≥62
‑
(0.15x年龄)cm h2o,女性:≥62
‑
(0.50x年龄)cm h2o。
[0219]
13.实施方案1
‑
7中任意一项所述的方法,其用于治疗实施方案8
‑
12所定义的具有降低的fgf23介导的副作用风险的个体。
[0220]
14.一种监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液或尿液参数:(1)血清磷酸盐水平,(2)血清维生素d水平,(3)血清离子钙水平,(4)血清pth水平以及(5)尿磷酸盐排泄分数,其中如果至少一个血液或尿液参数如实施方案9所定义,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
[0221]
15.一种监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包
括从所述个体获得的生物样品中确定至少一个选自如下的血液参数:(1)血清骨特异性碱性磷酸酶水平,(2)血清碱性磷酸酶水平,(3)血清i型胶原n端前肽(pinp)水平以及(4)血清羧基末端胶原交联(ctx)水平,其中如果至少一个血液参数如实施方案10所定义,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
[0222]
16.一种监测个体的方法,其中已向所述个体给药第一剂量的羧基麦芽糖铁,其包括确定所述个体的呼吸容量,其中如果所述呼吸容量是正常的,则可以向所述个体给药第二剂量的羧基麦芽糖铁。
[0223]
17.一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液或尿液参数:(1)血清磷酸盐水平,(2)血清维生素d水平,(3)血清离子钙水平,(4)血清pth水平以及(5)尿磷酸盐排泄分数,其中如果至少一个血液或尿液参数如实施方案9所定义,则所述个体具有降低的fgf23介导的副作用风险。
[0224]
18.一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括从所述个体获得的生物样品中确定至少一个选自如下的血液参数:(1)血清骨特异性碱性磷酸酶水平,(2)血清碱性磷酸酶水平,(3)血清i型胶原n端前肽(pinp)水平以及(4)血清羧基末端胶原交联(ctx)水平,其中如果至少一个血液参数如实施方案10所定义,则所述个体具有降低的fgf23介导的副作用风险。
[0225]
19.一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括确定所述个体的特征是否在于以下的一个或多个,特别地,所有的淘汰标准:
[0226]
(1)接受过减肥手术;
[0227]
(2)肥胖;
[0228]
(3)心律失常风险增加的心脏病症;
[0229]
(4)原发性或继发性甲状旁腺机能亢进;
[0230]
(5)肺部疾病例,如哮喘或慢性阻塞性肺病(copd)
[0231]
(6)导致低磷血症的遗传性疾病,例如x
‑
连锁低磷血症、常染色体显性低血磷性佝偻病、常染色体隐性低血磷性佝偻病;
[0232]
(7)继发性低磷血症或者肿瘤诱发的低磷血症;
[0233]
(8)骨骼疾病,例如骨质疏松症或骨软化症;以及
[0234]
(9)给药铁1天至2个月以内安排手术,其中如果所述个体的特征在于不存在一个或多个,特别地,不存在所有的所述的淘汰标准,则所述个体具有降低的fgf23介导的副作用风险。
[0235]
20.一种识别具有降低的fgf23介导的副作用风险的个体的方法,其包括确定所述个体的呼吸容量,其中如果所述呼吸容量是正常的,则所述个体具有降低的fgf23介导的副作用风险。
[0236]
21.羧基麦芽糖铁与一种或多种额外药物的组合,所述组合用于治疗铁缺乏,其中所述额外药物选自:
[0237]
(1)维生素d;
[0238]
(2)磷酸盐;以及
[0239]
(3)抗fgf23拮抗抗体。
[0240]
22.实施方案21的组合,其中所述维生素d是钙化三醇、阿法骨化醇、胆钙化醇或麦角钙化醇。
[0241]
23.实施方案22的组合,其中在给药第一fcm剂量之前3天内,给药钙化三醇或阿法骨化醇。
[0242]
24.实施方案22的组合,其中在给药第一fcm剂量的同一天,开始给药钙化三醇或阿法骨化醇。
[0243]
25.实施方案22的组合,其中在给药第一fcm剂量后的第1天、第2天、第3天、第4天、第5天、第6天或第7天,或第14天,开始给药钙化三醇或阿法骨化醇。
[0244]
26.实施方案22的组合,其中在给药第一fcm剂量之前的第14天、第7天、第6天,或第5天、第4天、第3天、第2天、第1天,给药胆钙化醇或麦角钙化醇。
[0245]
27.实施方案22的组合,其中在给药第一fcm剂量之前,给药胆钙化醇或麦角钙化醇,然后在给药第一fcm剂量之后,给药钙化三醇或阿法骨化醇。
[0246]
28.实施方案21
‑
27中任意一项的组合,其中所述额外的药物为口服给药。
[0247]
29.实施方案21
‑
28中任意一项的组合,其中在给药第二剂量的羧基麦芽糖铁之前,给药所述额外的药物。
[0248]
30.实施方案21
‑
29的组合,用于实施方案1
‑
13中任意一项的方法。
[0249]
本发明将通过以下实施例进一步说明,而不应被理解为进一步地限制。本技术中引用的所有图和所有参考文献、genbank序列、专利和公开的专利申请的内容通过引用明确地并入本文。
[0250]
实施例
[0251]
进行了两项前瞻性的、随机的、开放标记的对比试验,对比了缺铁性贫血的成年个体使用异麦芽糖苷铁(“iim”,商品名)和羧基麦芽糖铁(“fcm”,商品名injectafer,ferinject)治疗时,与其相关的低磷血症的发病率。
[0252]
试验设计
[0253]
该试验是一项随机的、开放标记的对比试验。具有缺铁性贫血(ida)的个体被1:1随机分配到以下治疗方法中的一个疗程中:
[0254]
·
a组:异麦芽糖苷铁1000(pharmacosmos,denmark,以下称为异麦芽糖苷铁),基线为1000mg
[0255]
·
b组:羧基麦芽糖铁(viforinc,switzerland),基线和第7天为750mg,累积剂量:1500mg
[0256]
根据其美国标签,fcm通过以下方式给药,两次单次剂量为750mg的元素铁,间隔一周。异麦芽糖苷铁1000通过如下方式给药,1000mg单次剂量的元素铁。
[0257]
目标
[0258]
试验的主要目的是为了对比接受异麦芽糖苷铁或羧基麦芽糖铁治疗的ida个体的低磷血症的发病率。
[0259]
试验的次要安全目的是对比接受异麦芽糖苷铁和羧基麦芽糖治疗的ida个体的以下影响:
[0260]
(1)严重低磷血症的发病率
[0261]
(2)患有低磷血症的时间
[0262]
(3)最后一次访视时患有低磷血症的个体的比例
[0263]
(4)s
‑
磷酸盐(绝对[δ]和相对[%]变化)
[0264]
(5)磷酸盐尿液排泄分数
[0265]
(6)完整的成纤维细胞生长因子23(ifgf23),c端fgf23(cfgf23),维生素d(25,1,25,24,25),甲状旁腺激素(pth),和离子钙
[0266]
(7)不良事件(ae)和生化安全参数
[0267]
试验的次要效力目的是比较接受异麦芽糖苷铁和羧基麦芽糖铁治疗的ida个体的血红蛋白(hb)、s
‑
铁蛋白,和转铁蛋白饱和度(tsat)的影响。
[0268]
除了主要和次要目的,还对异麦芽糖苷铁和羧基麦芽糖铁的影响进行了探索性的分析,其包括以下内容
[0269]
(1)生化骨/肌肉标记物
[0270]
(2)肌肉力量
[0271]
终点
[0272]
主要终点为低磷血症(定义为s
‑
磷酸盐<2mg/dl)从基线到第35天的任何时间的发病率。
[0273]
次要安全终点为以下内容:
[0274]
·
从基线至第35天的任何时间,s
‑
磷酸盐低于1.0mg/dl的发病率
[0275]
·
从基线至第35天,出现低磷血症(例如,s
‑
磷酸盐<2.0mg/dl的时间)
[0276]
·
在第35天出现低磷血症的个体的比例
[0277]
·
从基线至1、7、8、14、21和35天,s
‑
磷酸盐的绝对[δ]和相对[%]变化
[0278]
·
在1、7、8、14、21和35天的磷酸盐尿液排泄分数
[0279]
·
从基线至1、7、8、14、21和35天,ifgf23、cfgf23、维生素d(25、1,25、24,25)、pth和离子钙的变化
[0280]
·
ae的类型和发病率。
[0281]
·
在第一剂量的随机治疗之时或之后开始的严重或剧烈的超敏反应(即治疗紧急情况)。所述超敏反应的术语如标准的用于监管活动查询(smq)术语的医学词典所定义的。
[0282]
此外,作为安全评估的一部分,还进行了身体检查和生命体征、身高、体重、心电图(ecg)和安全实验室参数的测定。
[0283]
次要效力终点为如下内容:
[0284]
·
从基线至第1、7、8、14、21和35天,hb、s
‑
铁蛋白和tsat的变化探索性的终点如下:
[0285]
·
从基线至第1、7、8、14、21和35天,生化骨/肌肉标记物(血清i型胶原n端前肽(pinp)、血清羧基末端胶原交联(ctx)、s
‑
碱性磷酸酶(骨特异性及全部)和肌酸激酶)的变化
[0286]
·
通过慢性疾病治疗功能评估(facit)疲劳评分(fatigue scale)测定从基线至第14天和35天的疲劳症状的变化
[0287]
·
通过短表(sf)
‑
36调查表测定从基线至第14天和35天的qol的变化
[0288]
·
用视觉模拟评分(vas)测定从基线至第14天和35天的骨痛变化
[0289]
·
通过握力测定从基线至第14天和35天的肌肉力量的变化
[0290]
·
通过“1kg升臂”测试和“30s椅子站立”测试测定从基线至第14天和35天的上下肢近端肌肉功能变化
[0291]
·
通过最大吸气压力(maximal inspiratory pressure,mip)和最大呼气压力(maximalrespiratory pressure,mep)测定从基线至第14天和35天的呼吸肌肉力量变化
[0292]
安全评估
[0293]
试验包含以下安全评估:
[0294]
·
测定s
‑
磷酸盐(血液和尿液)、ifgf23、cfgf23、维生素d(25、1,25、24,25)、pth和离子钙
[0295]
·
将收集ae并评估其相关性、严重性、严重程度和预期性。根据国际和当地的要求,将这些报告给当局并进行跟进
[0296]
·
身体检查,测定生命体征、ecg、身高、体重和安全实验室参数
[0297]
效力评估
[0298]
试验包括以下效力评估:
[0299]
·
hb、s
‑
铁蛋白、tsat和s
‑
铁
[0300]
探索性评估
[0301]
探索性评估包括以下内容:
[0302]
·
测定血清n端pinp、ctx、s
‑
碱性磷酸酶(骨特异性及全部)和肌酸激酶
[0303]
·
mip和mep
[0304]
试验持续时间和访视次数
[0305]
对单个个体来说,试验持续时间为5周(包括28天的筛选期),每个个体参加8次访视。
[0306]
个体群体
[0307]
满足以下资格标准的个体被纳入。
[0308]
纳入标准:
[0309]
如果个体满足以下标准,则有资格被纳入试验:
[0310]
1.由于不同病因*,例如异常子宫出血、胃肠道疾病、癌症、减肥手术(胃旁路手术)和其他导致大量失血的病症引起的ida的男性或女性(>18岁)。
[0311]
2.hb≤11g/dl
[0312]
3.体重>50kg
[0313]
4.s
‑
铁蛋白≤100ng/ml
[0314]
5.预计的肾小球滤过率(egfr)≥65ml/min/1.73m2[0315]
6.s
‑
磷酸盐>2.5mg/dl
[0316]
7.参与试验前至少一个月***对口服铁剂治疗有不耐受或无反应的历史记录**
[0317]
8.愿意参与并签署知情同意书(informed consent form,icf)
[0318]
*ida的病因(即使不详)记录在病历中,并在源文件中得到验证。
[0319]
**对口服铁治疗的不耐受和无反应,以及体征和症状记录在病史中,并在源文件中得到验证。
[0320]
***根据研究者判断,在过去9个月内,对至少一个月的处方口服铁治疗剂有不耐
受或无反应的记录,并且他们不会再次成为口服铁剂的候选人。
[0321]
淘汰标准:
[0322]
如果个体满足以下任何一项标准,则没有资格纳入本试验:
[0323]
1. 72小时内急性出血>500ml
[0324]
2.根据研究者的判断,主要由ida以外的因素引起贫血。
[0325]
3.血色病或其他铁储存疾病
[0326]
4.对异麦芽糖苷铁(iron isomaltoside)或羧基麦芽糖铁的任何成分的已知的超敏反应
[0327]
5.曾经对任何iv铁化合物产生过严重的超敏反应
[0328]
6.筛查前30天内接受过iv铁治疗
[0329]
7.筛查前30天内接受红细胞生成素或红细胞生成素刺激剂、红细胞输血、放疗和/或化疗的治疗
[0330]
8.筛查前30天接受过研究性药物
[0331]
9.计划在试验期间进行外科手术
[0332]
10.丙氨酸转氨酶(alat)和/或天冬氨酸转氨酶(asat)>正常上限的3倍(例如,失代偿期肝硬化或活动性肝炎)
[0333]
11.筛查前30天内进行了全身麻醉手术
[0334]
12.筛查前30天内任何非病毒性感染
[0335]
13.过去6个月内酗酒或滥用药物
[0336]
14.未经治疗的甲状旁腺机能亢进
[0337]
15.肾脏移植
[0338]
16.预计预期寿命<6个月,或对于癌症病人,东部合作肿瘤学组(ecog)的体力活动状态>1
[0339]
17.影响个体理解试验要求的能力和/或推定为不遵守的情况18.在研究者看来,任何会使个体疾病管理具有风险或可能导致个体无法遵守试验要求的其他实验室异常、医疗状况或精神疾病
[0340]
19.怀孕或哺乳期女性。为了避免怀孕,有生育能力的女性在整个试验时期和最后一次剂量7天内必须采取适当的避孕措施(例如,宫内节育器、激素避孕药或双屏障法)
[0341]
下表提供了包括所述个体群体的总结:
[0342][0343]
试验治疗
[0344]
个体被给予如下所述的一个疗程的异麦芽糖苷铁(a组)或一个疗程的羧基麦芽糖铁(b组)。
[0345]
·
a组:异麦芽糖苷铁1000mg稀释在100ml 0.9%的氯化钠中,在基线,以单次iv输注的方式,在大约20分钟内(50mg铁/分钟,累积剂量:1000mg)完成给药。
[0346]
·
b组:在基线和第7天,以750mg的量输注至少15分钟(累积剂量:1500mg),给药羧基麦芽糖铁。
[0347]
在给药试验药物以前,不允许进行预先给药(例如,抗组胺药物或类固醇)。如果个体正在接受例如过敏和哮喘的日常治疗,则不被视为“预先给药”,并可以继续。
[0348]
统计分析
[0349]
主要终点,即从基线至第35天的任何时间低磷血症(定义为s
‑
磷酸盐<2mg/dl)的发病率被制成表格,并对每个治疗组的精确的95%ci进行评估。
[0350]
通过评估风险差异和相关的95%ci,对比异麦芽糖苷铁和羧基麦芽糖铁,对层(基础疾病类型(因妇科失血导致的ida女性;是/否))进行调整并使用cochran
‑
mantel
‑
haenszel方法筛查s
‑
磷酸盐水平(<或≥3.5mg/dl)。
[0351]
对于敏感性,通过logistic回归模型,以治疗和基础疾病类型为因子,以基线s
‑
磷酸盐为协变量,并通过fisher精确检测来使各治疗组之间进行对比。
[0352]
安全分析组中所有个体都包括在分析中。第一次基线后磷酸盐测定是在第一天进
行的;因此,预计很少有缺失值。如果个体没有基线后磷酸盐测量值,这些个体将会被设定为具有初步分析中的s
‑
磷酸盐<2mg/dl。
[0353]
所有统计分析都将在统计分析计划中描述。
[0354]
基线评估
[0355][0356]
试验评估
[0357]
人口统计和基线评估
[0358]
收集出生日期、性别、种族和吸烟习惯。目前的吸烟者被定义为过去6个月以内吸烟的个体。
[0359]
妊娠试验
[0360]
对所有具备生育能力的女性进行了尿妊娠试验。该试验由现场人员处理和解释。
[0361]
相关病史
[0362]
记录相关病史。在试验期间的后续访视中记录病史的变化(症状或疾病的恶化被记录为ae)。收集以下信息:疾病和开始及停止日期。除了引起ida的基础疾病以外,参与试验前发生的开始日期>12个月被设定为>12个月。
[0363]
伴随药物治疗
[0364]
如果个体正在接受任何伴随药物治疗,则在基线访视时记录。在试验期间的后续访视中,记录伴随药物的变化。收集以下内容:品牌名称、适应症、途径、剂量、频率、单位以及开始和停止日期。参与试验前发生的开始日期>12个月被设定为>12个月。
[0365]
身体检查
[0366]
根据研究者的判断进行身体检查,其可能包括以下内容:
[0367]
·
头
‑
眼
‑
耳
‑
鼻
‑
喉
[0368]
·
心血管系统
[0369]
·
呼吸系统
[0370]
·
神经系统
[0371]
·
胃肠道系统
[0372]
·
肌肉
‑
骨骼系统
[0373]
·
泌尿生殖系统
[0374]
·
皮肤系统
[0375]
·
其他,如有需要
[0376]
身高
[0377]
测量不穿鞋的身高。
[0378]
体重
[0379]
测量体重。
[0380]
生命体征
[0381]
当个体接受试验药物时,在以下时间点测量心率和血压:输注前大约0
‑
10分钟、输注时、输注结束后5
‑
15分钟和20
‑
40分钟。如果在给定时间间隔内测定生命体征超过一次,则在电子病历报告表(ecrf)中记录这段时间内舒张压的最低测量值(包括伴随的收缩压和心率)。
[0382]
心电图
[0383]
记录标准的12导联ecg(包括日期、时间和签名)。在基线和其他治疗访视中,记录了两份ecg;一份是给药试验药物以前,一份是开始给药后大约30分钟。在随后的访视中只记录了一份ecg。
[0384]
ecg不需要由心脏病学专家来评估。
[0385]
呼吸肌肉力量
[0386]
mip和mep的测量为评估呼吸肌肉力量提供了一种无创的临床方法,并且其为评估肌肉压力最广泛使用的测试[ats/ers statement,2002]。mip反映了膈膜和其他吸气肌肉的力量,而mep反映了腹肌和其他呼气肌肉的力量。mip和mep都通过microrpm(carefusion germany 234gmbh,hoechberg,germany)测量。对mip和mep都进行了三次测试,三次测试中的最高值用来作为取得的结果。
[0387]
实验室评估
[0388]
需要在给药试验药物前抽取血液样本,并且如果可以的话,在所有访视时的一天中的同一时间,抽取血液样本以减少昼夜参数的任何波动。
[0389]
实验室评估是在一个中心实验室进行的。向每个站点提供了一份实验手册,其中描述了所有实验室程序。
[0390]
资格实验室评估
[0391]
进行了以下资格实验室评估:
[0392]
·
完整的血液病学组:hb、白细胞/白血细胞(wbc)、红细胞/红血细胞(rbc)、血细胞比容、血小板、中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、平均血红蛋白(mch)、平均血细胞体积(mcv)、平均血红蛋白浓度(mchc)和网织红细胞计数。
[0393]
·
生物化学:
[0394]
оs
‑
铁蛋白
[0395]
оs
‑
磷酸盐
[0396]
о丙氨酸转氨酶(alat)和天冬氨酸转氨酶(asat)
[0397]
оc
‑
反应蛋白(crp)
[0398]
о预计的肾小球滤过率(egfr)
[0399]
оpth
[0400]
维生素e
[0401]
作为人口统计学数据的一部分,在基线访视时测定维生素e。
[0402]
安全实验室评估
[0403]
对以下安全实验室评估进行分析:
[0404]
·
s
‑
磷酸盐:在硫酸的存在下,无机磷与钼酸铵反应形成的具有式(nh4)3[po4](moo3)
12
的磷钼酸复合物。使用roche modular和cobas analyzers,在光谱紫外区(340nm)对该复合物进行光度法测定。
[0405]
·
ifgf23和cfgf23:人完整的fgf23是由immonotropics,inc,sanclemente,ca制造的第二代elisa试剂盒测定。这是一种双位的酶联免疫吸附试验。人c端fgf23由immonotropics,inc,sanclemente,ca制造的elisa试剂盒测定。这是一种双位的酶联免疫吸附试验。
[0406]
·
维生素d(25、1,25、24,25):在蛋白质沉淀后,25
‑
羟基维生素d2、25
‑
羟基维生素d3和及其内标物通过支撑液萃取(sle)进行萃取。在氮气下蒸发后,残留物被重组并使用液相色谱法(lc)与串联质谱检测(ms/ms)进行分析。标准曲线范围为0.5ng/ml至200.00ng/ml,使用的血清体积为0.1ml。
[0407]
·
pth:完整的pth试验是使用advia centaur xp仪器的ipth试剂包进行的。该试验是采用直接化学发光技术的双位夹心免疫试验,在lite试剂中使用恒量的两种抗
‑
人pth抗体。第一种抗体是多克隆山羊抗
‑
人pth(n端1
‑
34)抗体,用吖啶酯标记。第二种抗体是生物素化的多克隆山羊抗
‑
人pth(39
‑
84区)抗体。固相中的链霉亲和素与顺磁乳胶粒子共价偶联。病人样品中存在的pth量与该系统检测到的相对光单位(rlu)的量之间存在直接关系。
[0408]
·
离子钙:由il gem premier 3500pak盒测量。核心部件是传感器卡,其提供一个低容量的气密室,样本在其中呈现给传感器。ph和电解质传感器都是基于离子选择性电极的原理;即,可以在对特定离子具有选择性的渗透性的膜上建立电势。ph和电解质传感器是基于聚氯乙烯(pvc)的离子选择性电极,由内部ag/agcl参比电极和内部盐层组成。相对于卡参比电极测量电势。
[0409]
·
完整的血液学组:白细胞/wbc、红细胞/rbc、血细胞比容、血小板、中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、mch、mcv、mchc和网织红细胞计数。
[0410]
·
生物化学:
[0411]
оs
‑
钠、s
‑
钾、s
‑
钙、s
‑
尿素、s
‑
肌酐、s
‑
白蛋白
[0412]
оs
‑
胆红素,asat,alat
[0413]
оcrp
[0414]
效力实验室评估对以下效力实验室参数进行分析:
[0415]
·
hb
[0416]
·
s
‑
铁蛋白:access铁蛋白试验是一种双位免疫酶法(“夹心”测定)。将样品加入到反应容器中,所述反应容器装有山羊抗
‑
铁蛋白
‑
碱性磷酸酶结合物,以及包被山羊抗
‑
小鼠:小鼠抗
‑
铁蛋白复合物的顺磁性粒子。血清或血浆(肝素)铁蛋白与固相上的固定化单克隆抗
‑
铁蛋白结合,而山羊抗
‑
铁蛋白酶结合物与铁蛋白分子上的不同抗原位点反应。在磁场中的分离和洗涤除去了未与固相结合的物质。在反应容器中加入化学发光底物lumi
‑
phos*530,用发光仪测量反应产生的光。
[0417]
·
tsat(收集s
‑
铁和转铁蛋白来计算tsat)
[0418]
探索性实验室评估对以下探索性实验室评估进行分析:
[0419]
·
血清n端pinp:测量方法为夹心原理、电化学发光免疫分析(eclia)。在第一次孵育过程中,将样品中的pinp和生物素化的单克隆pinp特异性抗体一起孵育。
[0420]
在第二次孵育过程中,加入链霉亲和素包被标记的微粒和使用钌复合物(trs(2,2
‑
双吡啶基)钌(ii)
‑
复合物(ru(bpy)23 ))标记的单克隆pinp特异性抗体,以形成夹心复合物,其通过生物素和链霉亲和素的相互作用与固相结合。反应混合物被吸收进入测量池,其中的微粒被磁力捕获到电极表面。在电极上施加电压,引起化学发光发射,用光电倍增管测量。结果通过校准曲线确定,所述校准曲线由仪器特有的2点校准和通过试剂条形码提供的主曲线生成。该方法在cobas e601analyzer上运行。
[0421]
·
ctx:在第一次孵育过程中,将50μl样品和生物素化的单克隆抗
‑
β
‑
骨胶原交联抗体一起孵育。在第二次孵育过程中,加入链霉亲和素包被标记的微粒和钌复合物标记的单克隆pβ
‑
骨胶原交联特异性抗体,以形成夹心复合物,通过生物素和链霉亲和素的相互作用与固相结合。反应混合物被吸收进入测量池,其中的微粒被磁力捕获到电极表面。然后使用procell去除未结合的物质。在电极上施加电压,引起化学发光发射,用光电倍增管测量。结果通过校准曲线确定,所述校准曲线由仪器特有的2点校准和通过试剂条形码提供的主曲线生成。该方法在cobas e601 analyzer上运行。
[0422]
·
s
‑
碱性磷酸酶(骨特异性及全部):骨特异性磷酸酶(bap)在beckmandxi800上测量。beckman
‑
coulter ostase试验是一种一步免疫酶化学发光试验。对骨特异性碱性磷酸酶(bap)具有特异性的小鼠单克隆抗体加入到反应容器中,反应器中具有包被山羊抗
‑
小鼠多克隆抗体的顺磁性粒子。将校准品、对照品和含有bap的样品加入到包被的粒子,并与抗
‑
bap单克隆抗体结合。将化学发光底物lumi
‑
phos*530加入反应容器中,用发光仪测量反应产生的光。光的产生与样品中bap的量成正比。样品中bap的量是通过存储的多点校准曲线来确定的。血液血清中总的碱性磷酸酶水平是用roche modular analyzer测定的。在镁和锌离子的存在下,对硝基苯磷酸酯被磷酸酶裂解为磷酸根和对硝基苯酚。释放的对硝基苯酚与alp活性成正比,并通过光度法测量。
[0423]
·
肌酸激酶:肌酸激酶(ck)试验是在roche modular和cobas analyzers上进行的。
[0424]
该反应按照以下方式进行:
[0425]
磷酸肌酸 adp ck>肌酸 atp
[0426]
atp 葡萄糖hk>adp g
‑6‑
p
[0427]
g
‑6‑
p nadp >g
‑6‑
pdh6
‑
pg nadph h
[0428]
形成nadph的速率与等摩尔量的肌酸的形成相同。形成nadph的速率与ck的活性成正比,并以光度法测量。
[0429]
尿液评估
[0430]
为了评估s
‑
磷酸盐的排泄分数水平,收集了现场尿液样品。
[0431]
不良事件
[0432]
收集ae,并评估其与试验药物的相关性、严重性、严重程度和预期性。
[0433]
结果
[0434]
主要发现包括fcm的剂量方案对管理磷酸盐、维生素d和钙的内分泌系统有明显的影响。
[0435]
fcm与iim相比,就中度至重度的形式而言,不论是血清磷酸盐低于2mg/dl的中度形式,还是血清磷酸盐在或低于1.0mg/dl的重度形式,低磷血症的发病率都明显更高。参见图1到图5。
[0436]
给药fcm之后,完整的ifgf23(ifgf23)急剧增加,然后在几天内逐渐减少。在第二次给药时,ifgf23再次增加,但这次的水平比最初水平高几倍,即,一种令人惊讶的、前所未知的自我放大效应。对于iim来说,基本上没有观察到ifgf23水平的变化。参见图6和图7。由于潜在的缺铁性贫血,c端fgf23(cfgf23)最初高,在第一次fcm给药时急剧下降,而在第二次fcm给药时上升。参见图8。fcm与iim相比,磷酸盐尿液排泄分数明显增加。参见图10。fcm导致pth的增加、1,25
‑
二羟基维生素d的减少、24,25
‑
二羟基维生素d的增加和离子钙的减少。参见图11至图13。
[0437]
此外,根据以下生化骨/肌肉标记物的测量,fcm导致骨周转和肌肉功能明显变化:
[0438]
与imm相比,fcm诱导了骨特异性碱性磷酸酶的统计学上的明显增加。参见图14。
[0439]
与imm相比,fcm诱导了n端pinp值在统计学上的明显降低。参见图14。
[0440]
与imm相比,fcm诱导了ctx值在统计学上的明显降低。参见图14。
[0441]
与imm相比,fcm诱导了碱性磷酸酶在统计学上的明显增加。参见图14。
[0442]
相对于参照物iv铁治疗,fcm还导致了降低的肌肉功能,其具体通过如下测量,测量为最大呼气压力和/或最大吸气压力的呼吸容量。参见图15。
[0443]
等同
[0444]
本领域技术人员将认识到,或能够通过使用不超过常规的实验来确定本发明所公开的具体实施方案的许多等同物。这样的等同物旨在被以下权利要求所包含。
[0445]
非专利出版物
[0446]
aksan et al.,aliment pharmacol ther 2017,45(10),1303
‑
1318
[0447]
bager et al.,br j clin pharmacol 2017,83,1118
‑
1125
[0448]
bregman et al.,ther adv hematol 2014,5(2),48
‑
60
[0449]
charytan et al.,nephrol dial transplant 2013,28,953
‑
964
[0450]
evstatiev,gastroenterology 2011,141,846
‑
853
[0451]
hussain et al.,anemia 2013,article id 169107,10pages
[0452]
ikuta etal.,int j hematol 2018,https://doi.org/10.1007/s12185
‑
018
‑
2501
‑8[0453]
klein et al.bmj case rep 2018;doi:10.1136/bcr
‑
2017
‑
222851
[0454]
prats et al.,bmc nephrology 2013,14:167
[0455]
qunibi et al.,nephrol dial transplant2011,26,1599
‑
1607
[0456]
sari et al.,neth j med 2017,75(2),65
‑
73
[0457]
schaefer et al.,gastroenterology 2017,152(6),e5
‑
e6
[0458]
seid et al.,am j obstet gynecol 2008,199:435.el
‑
435.e7
[0459]
stein et al.,scand j gastroenterol 2018,https://doi.org/10.1080/
00365521.2018.1498914
[0460]
van wyck et al.,transfusion 2009,49(12),2719
‑
2728
[0461]
wolfet al.,journal of bone and mineral research 2013,28(8),1793
‑
1803
[0462]
zoller et al.,curropin nephrol hypertens 2017,26(4),266
‑
275
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。