一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法
技术领域
1.本发明涉及油气腐蚀防护技术领域,特别是涉及一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法。
背景技术:
2.近年来,全球的油气能源需求不断增加,而油气输送系统是连接生产端和消费端的关键,其中管道输送由于其安全性和经济性被视为远距离油气输送的首选方式。然而在管线运行过程中管线钢会不可避免地发生失效,因此,管道腐蚀速率预测对管道安全运行具有重要意义。
3.建立腐蚀速率预测模型时明确腐蚀介质十分重要,油气生产和传输设施中的腐蚀通常是由共同产生的水相,酸性气体和溶解的酸性化合物引起的。而在天然气的开采过程中,co2几乎总是作为副产物存在,而co2的水合物碳酸也是管道中最常见的腐蚀介质。高强钢的均匀co2腐蚀也是被研究最多,理论最充分的腐蚀系统之一,因此目前的腐蚀速率预测模型大部分都是以co2腐蚀为基础。
4.近年来,相关学者对不同环境下的co2腐蚀进行了大量的研究,并提出了许多腐蚀速率预测模型。然而,随着对co2腐蚀研究的不断深入,有学者发现现有的co2腐蚀理论已经不能解释一些实验现象。特别当介质流动速度较快时,co2腐蚀速率更高。并且,由于环境温差的作用,部分水蒸汽冷凝在管道顶部内璧上,造成线顶腐蚀。这两种常见的腐蚀条件不能直接应用传统的co2腐蚀速率预测模型,因此有必要研究流动和线顶腐蚀条件下的co2腐蚀行为和机理,从而建立co2腐蚀速率预测模型,以保障天然气管线的安全运行。
技术实现要素:
5.为了克服现有技术的不足,本发明的目的是提供一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法。
6.为实现上述目的,本发明提供了如下方案:
7.一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法,包括:
8.获取实际检测的腐蚀环境数据;
9.将所述腐蚀环境数据输入验证好的co2腐蚀速率预测机理模型中,得到预测腐蚀速率;
10.所述co2腐蚀速率预测机理模型的构建方法为:
11.对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据;
12.基于密度泛函理论的第一性原理计算碳酸和h
在铁表面的吸附和电荷转移参数,并分析电荷转移规律,得到co2的腐蚀机理;
13.根据所述腐蚀机理和腐蚀过程构建初始模型;
14.根据所述腐蚀数据对所述初始模型进行精度校准,得到所述co2腐蚀速率预测机
理模型。
15.优选地,所述腐蚀过程包括:
16.化学过程、电化学过程和传质过程。
17.优选地,所述对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据,包括:
18.利用电化学试验和显微表征手段确定所述待测刚体在纯co2饱和溶液中流动和积液条件下的腐蚀行为,得到第一实验结果;
19.根据所述第一实验结果对比分析流动和积液条件下的腐蚀行为规律。
20.优选地,所述对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据,包括:
21.通过电化学试验和显微表征手段确定所述待测刚体在线顶腐蚀条件下的co2腐蚀行为,得到第二实验结果;
22.根据所述第二实验结果分析腐蚀产物的结构与成分。
23.优选地,所述基于密度泛函理论的第一性原理计算碳酸和h
在铁表面的吸附和电荷转移参数,并分析电荷转移规律,得到co2的腐蚀机理,包括:
24.利用第一性原理计算碳酸和h
在fe表面的吸附情况和电荷转移参数;
25.根据所述吸附情况和电荷转移参数确定转移规律;
26.根据所述转移规律进行分析总结,得到所述腐蚀机理。
27.优选地,所述化学过程的建模方法包括:
28.确定co
2-混合盐-h2o体系中的动态相平衡过程;
29.根据热力学概念,获取计算所述动态相平衡过程的平衡常数;
30.根据碳酸解离和水解离的热力学平衡过程的平衡常数、所述动态相平衡过程的平衡常数和所述动态相平衡过程构建所述化学过程。
31.优选地,所述电化学过程的建模方法包括:
32.根据能斯特方程,确定阳极反应、阴极反应和平衡电位;
33.根据所述腐蚀机理确定所述阳极反应为fe的溶解且所述阴极反应为h
和h2o的还原;
34.根据塔菲尔方程确定所述阳极反应和所述阴极反应的电流密度;
35.根据所述电流密度构建所述电化学过程。
36.优选地,所述传质过程的建模方法包括:
37.根据对流作用引起的分子扩散和各种离子的电迁移确定物质的通量表达式和传质公式;
38.对所述通量表达式和所述传质公式进行化简和条件约束,得到金属表面通量公式;
39.根据所述金属表面通量公式构建所述传质过程。
40.优选地,所述待测刚体为x80钢。
41.根据本发明提供的具体实施例,本发明公开了以下技术效果:
42.本发明提供了一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法,首先获取实际检测的腐蚀环境数据;将所述腐蚀环境数据输入验证好的co2腐蚀速率预测机理模
型中,得到预测腐蚀速率;所述co2腐蚀速率预测机理模型的构建方法为:对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据;基于密度泛函理论的第一性原理计算碳酸和h
在铁表面的吸附和电荷转移参数,并分析电荷转移规律,得到co2的腐蚀机理;根据所述腐蚀机理和腐蚀过程构建初始模型;根据所述腐蚀数据对所述初始模型进行精度校准,得到所述co2腐蚀速率预测机理模型。本发明根据co2腐蚀机理建立的内腐蚀速率预测模型预测精度更高,能够为天然气管道的安全运行提供理论依据。
附图说明
43.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
44.图1为本发明实施例提供的方法流程图;
45.图2为本发明实施例提供的腐蚀速率预测模型流程图;
46.图3为本发明实施例提供的动态条件下腐蚀机理示意图;
47.图4本发明实施例提供的薄液层条件下的腐蚀机理示意图
48.图5本发明实施例提供的co2环境下测试得到的腐蚀速率与预测模型计算结果对比示意图。
具体实施方式
49.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
50.在本文中提及“实施例”意味着,结合实施例描述的特定特征、结构或特性可以包含在本技术的至少一个实施例中。在说明书中的各个位置出现该短语并不一定均是指相同的实施例,也不是与其它实施例互斥的独立的或备选的实施例。本领域技术人员显式地和隐式地理解的是,本文所描述的实施例可以与其它实施例相结合。
51.本技术的说明书和权利要求书及所述附图中的术语“第一”、“第二”、“第三”和“第四”等是用于区别不同对象,而不是用于描述特定顺序。此外,术语“包括”和“具有”以及它们任何变形,意图在于覆盖不排他的包含。例如包含了一系列步骤、过程、方法等没有限定于已列出的步骤,而是可选地还包括没有列出的步骤,或可选地还包括对于这些过程、方法、产品或设备固有的其它步骤元。
52.本发明的目的是提供一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法,根据co2腐蚀机理建立的内腐蚀速率预测模型预测精度更高,能够为天然气管道的安全运行提供理论依据。
53.为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合附图和具体实施方式对本发明作进一步详细的说明。
54.图1为本发明实施例提供的方法流程图,如图1所示,本发明提供了一种基于co2腐蚀机理的天然气管道内腐蚀速率预测方法,包括:
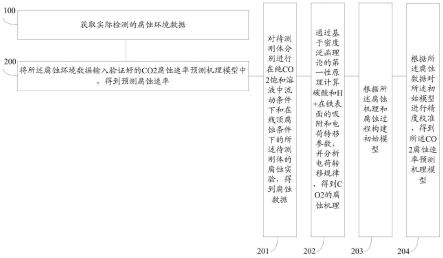
55.步骤100:获取实际检测的腐蚀环境数据;
56.步骤200:将所述腐蚀环境数据输入验证好的co2腐蚀速率预测机理模型中,得到预测腐蚀速率;
57.所述步骤200还包括:
58.步骤201:对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据;
59.步骤202:基于密度泛函理论的第一性原理计算碳酸和h
在铁表面的吸附和电荷转移参数,并分析电荷转移规律,得到co2的腐蚀机理;
60.步骤203:根据所述腐蚀机理和腐蚀过程构建初始模型;
61.步骤204:根据所述腐蚀数据对所述初始模型进行精度校准,得到所述co2腐蚀速率预测机理模型。
62.其中,所述待测刚体可以为x80钢。
63.图2为本发明实施例提供的腐蚀速率预测模型流程图,如图2所示,本实施例首先通过电化学试验和显微表征手段研究x80钢在纯co2饱和溶液中积液和流动条件下的腐蚀行为,对比分析积液和流动条件下的腐蚀行为规律,动态条件下腐蚀机理图如图3所示;同样,通过电化学试验和显微表征手段研究x80钢在线顶腐蚀条件下的co2腐蚀行为,线顶腐蚀环境类似于薄液层,故在薄液层条件下分析腐蚀产物的结构与成分,从而阐明线顶腐蚀条件下的co2腐蚀行为规律,薄液层条件下的腐蚀机理图如图4所示;通过基于密度泛函理论的第一性原理计算碳酸和h
在铁表面的吸附和电荷转移参数,分析电荷转移规律阐明co2腐蚀机理优选地,所述腐蚀过程包括:
64.化学过程、电化学过程和传质过程。
65.优选地,所述对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据,包括:
66.利用电化学试验和显微表征手段确定所述待测刚体在纯co2饱和溶液中流动和积液条件下的腐蚀行为,得到第一实验结果;
67.根据所述第一实验结果对比分析流动和积液条件下的腐蚀行为规律。
68.优选地,所述对待测刚体分别进行在纯co2饱和溶液中流动条件下和在线顶腐蚀条件下的所述待测刚体的腐蚀实验,得到腐蚀数据,包括:
69.通过电化学试验和显微表征手段确定所述待测刚体在线顶腐蚀条件下的co2腐蚀行为,得到第二实验结果;
70.根据所述第二实验结果分析腐蚀产物的结构与成分。
71.具体的,通过实验得到腐蚀动力学参数,为建立co2腐蚀速率预测机理模型提供数据支持。
72.优选地,所述基于密度泛函理论的第一性原理计算碳酸和h
在铁表面的吸附和电荷转移参数,并分析电荷转移规律,得到co2的腐蚀机理,包括:
73.利用第一性原理计算碳酸和h
在fe表面的吸附情况和电荷转移参数;
74.根据所述吸附情况和电荷转移参数确定转移规律;
75.根据所述转移规律进行分析总结,得到所述腐蚀机理。
76.可选地,为了进一步阐明碳酸腐蚀机理,利用第一性原理计算了碳酸和h
在fe表面的吸附和电荷转移能力,并将腐蚀机理的数学关系整合到腐蚀速率预测模型中,为管道的剩余寿命预测工作提供理论依。其中计算结果如表1、表2和表3所示。
77.表1 h2co3在不同位置的吸附能和吸附前后键长键角的变化情况
[0078][0079]
表2 h
在不同位置的吸附能和吸附前后键长键角的变化情况
[0080][0081]
表3电荷布居
[0082][0083]
本实施例确定了碳酸在管道腐蚀中的阴极反应机理,发现h
的还原在碳酸阴极反应中占据主导地位,碳酸的直接还原并不重要,甚至可以忽略不计。主要结论如下:
[0084]
(1)碳酸分子中的两个o原子带负电,mulliken电荷最低,反应活性最强,因此更容易与fe成键。在最稳定的fe(110)面,碳酸的最优吸附位置是th位,h
的吸附能要远小于碳酸,因此h
更容易吸附在fe表面进而发生反应。
[0085]
(2)在管道腐蚀速率预测中,阴极反应物质的确定十分重要,理论计算结果表明,碳酸的直接还原可以忽略,h
的还原速率决定了腐蚀速率的大小。
[0086]
优选地,所述化学过程的建模方法包括:
[0087]
确定co
2-混合盐-h2o体系中的动态相平衡过程;
[0088]
根据热力学概念,获取计算所述动态相平衡过程的平衡常数;
[0089]
根据碳酸解离和水解离的热力学平衡过程的平衡常数、所述动态相平衡过程的平衡常数和所述动态相平衡过程构建所述化学过程。
[0090]
具体的,基于co2腐蚀过程的化学过程步骤如下:
[0091]
(1)在co
2-混合盐-h2o体系中,富co2相中的co2分子和富h2o相中的h2o分子会溶解到对方的相中,在给定的温度和压力条件下,最终达到动态相平衡。在平衡状态下,动态相平衡过程可以写成:
[0092][0093][0094]
(2)在这项工作中,根据基本的热力学概念,平衡常数(k),被用来计算动态相平衡过程:
[0095][0096][0097]
其中fi是气态h2o和co2的逸度,可通过以下表达式计算:
[0098][0099]
其中,pi为组分i的分压,p为压力,为气态组分i的逸度系数。
[0100]
(3)此外,在天然气管道中,输送温度一般不会高于50℃,因此无需考虑h2o的活度模型来表示电解质的非理想性。
[0101]
碳酸解离:
[0102][0103][0104]
水解离:
[0105][0106]
(4)可以计算这些热力学平衡过程的平衡常数(k):
[0107]
[0108][0109][0110][0111]
其中,k为反应平衡常数,ai为离子活度。
[0112]
优选地,所述电化学过程的建模方法包括:
[0113]
根据能斯特方程,确定阳极反应、阴极反应和平衡电位;
[0114]
根据所述腐蚀机理确定所述阳极反应为fe的溶解且所述阴极反应为h
和h2o的还原;
[0115]
根据塔菲尔方程确定所述阳极反应和所述阴极反应的电流密度;
[0116]
根据所述电流密度构建所述电化学过程。
[0117]
具体的,基于co2腐蚀过程的电化学过程步骤如下:
[0118]
(1)在有电解液存在的情况下,金属腐蚀的本质是发生在金属表面的电化学腐蚀反应。碳钢在含co2环境中的腐蚀,其阳极过程是铁的溶解。对于阴极过程,可以忽略碳酸的直接还原作用。而根据能斯特方程,可能的阳极和阴极反应及其平衡电位总结如下:
[0119]
阳极反应:
[0120][0121][0122]
阴极反应:
[0123][0124]
(2)根据co2腐蚀机理研究的结果,该模型考虑的阳极和阴极反应是fe的溶解和h
、h2o的还原。阳极反应的电流密度,即腐蚀速率或腐蚀电流密度,是由电荷转移过程控制的。然而,每个电化学阴极反应的电流密度由这些阴极反应中涉及的活性物种的电荷转移过程和传质过程控制的:
[0125]icorr
=ia=i
c,tot
;
[0126][0127]
其中ir是电荷转移控制的电极反应电流密度,i
l
是传质控制的极限扩散电流密度。对于电荷转移控制的电极反应电流密度,可以用塔菲尔方程计算:
[0128]
[0129][0130]
其中,i
corr
为腐蚀电流密度,i0为交换电流密度,t为温度,tr为参考温度,r为气体常数。
[0131]
优选地,所述传质过程的建模方法包括:
[0132]
根据对流作用引起的分子扩散和各种离子的电迁移确定物质的通量表达式和传质公式;
[0133]
对所述通量表达式和所述传质公式进行化简和条件约束,得到金属表面通量公式;
[0134]
根据所述金属表面通量公式构建所述传质过程。
[0135]
具体的,基于co2腐蚀过程的传质过程步骤如下:
[0136]
(1)电化学反应速率由反应物浓度决定,而反应物浓度由传质过程决定。其中传质过程包括由对流作用引起的分子扩散和各种离子的电迁移。用涵盖化学反应和电化学反应的质量平衡方程描述扩散层中物种的传质过程:
[0137]
物质的通量可由下式描述:
[0138][0139]
由nernst-plank方程:
[0140][0141]
其中,ni为物种通量i,ri为物种i的净反应率。
[0142]
(2)由于预测对象为均匀腐蚀,因此仅在垂直于电极表面方向存在浓度梯度,因此上式可化简为
[0143][0144][0145]
(3)由于式是一个偏微分方程,需要特定的初始条件和边界条件。在初始时间(t=0),假设溶液均匀,金属表面的溶液浓度就是已知值,并且在整个反映过程中,物种总浓度始终不变。因此,对于电活性物种,金属表面与溶液边界的物质通量就是电化学反应速率。金属表面通量如下式:
[0146][0147]
(4)对于非电活性物种,由于不参与电化学反应,因此通量为0:
[0148][0149]
(5)同时,在电化学过程中同样存在“电中性”约束条件:
[0150][0151][0152]
本实施例最后基于co2腐蚀过程的化学过程、电化学过程和传质过程建立co2腐蚀速率预测机理模型,并通过实验数据对模型预测精度进行校准,其中通过假设金属表面为均匀腐蚀,构建了从溶液到金属表面的简单一维结构,这也是典型的腐蚀情况。当温度,压力,溶液性质,co2分压一定时,便可以通过上述公式计算腐蚀速率,将预测模型计算的腐蚀速率与实验数据进行比较,以检验模型的准确性。结果如图5所示,其中图5的虚线表示两倍误差。可以看出,几乎所有的数据都在代表两倍误差极限的范围内,这证明了该模型可以准确地计算出普通条件下的腐蚀速率,并且预测和测试结果的一致性进一步支持了本实施例中提出的腐蚀机制。
[0153]
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。
[0154]
本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其核心思想;同时,对于本领域的一般技术人员,依据本发明的思想,在具体实施方式及应用范围上均会有改变之处。综上所述,本说明书内容不应理解为对本发明的限制。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。