1.本发明涉及一种乳胶微球试剂冻干工艺,具体涉及一种乳胶微球试剂冻干工艺以及在免疫比浊试剂上的应用。
背景技术:
2.胶乳增强免疫比浊法利用粒径均匀的聚合物胶乳颗粒作为固相载体,微球通过吸附或者固定特异性抗体,在检测时与少量的抗原待测物反应,形成的免疫复合物会产品相应的浊度变化。由于聚合物胶乳复合物的粒径要比单纯抗原抗体复合物的粒径大得多,可在反应前后形成更大的浊度变化,既吸光度的变化。
3.免疫反应中使用到的乳胶微球试剂通常保存在水溶液中,而水溶液中的生物活性物质,例如抗体,抗原等极易受稳定性的影响,造成例如受热分解,染菌等问题,致使试剂长期存放后性能的下降,最终影响到试剂检测的准确性。因此保存在水溶液中的试剂溶液,需要保持长期2-8℃的低温保存,以及冷链运输,这不仅仅使得试剂的应用存储中产生很多限制,并且大大增加了试剂的运输储存成本,是如今体外诊断测定中的一个挑战。
4.冻干试剂由于保存条件简单,可实现常温保存和常温运输。并且冻干试剂操作简单,可实现手工操作,无需复杂的仪器设备,成本低廉,可覆盖各种终端应用场景。是诊断试剂的一个新发展方向。对于胶乳增强免疫比浊的项目,对微球试剂做冻干或者烘干处理后,生物活性物质不受水分影响,不会额外产生降解或者生物分解的因素影响,试剂的稳定性会大大延长。但是微球试剂类产品由于自身带有较多的表面电荷,在冷冻或者干燥过程中水分的缺失会破坏体系中微球原有自身电荷平和,导致微球由于电荷不平衡发生凝集。并且微球试剂冷冻过程中,逐步形成的表面锋利的冰结晶结构会破坏微球微观结构,导致微球试剂在复溶应用时产生不可逆的结构破坏或者性能的大幅下降。如免疫层析试剂应用中,微球试剂就通过干燥的形式分布在酥松多孔的玻璃纤维表面,但是层析试剂性在加入样本液体进行复溶后,性能会较大的损失和降低,常常在终端表现不佳,呈现检测cv的波动很大。
5.因此,急需要对微球冻干工艺试剂进行开发改进,需要满足一方面可简化试剂的保存条件,另一方面尽量避免或降低冻干对试剂性能的损失。
技术实现要素:
6.为解决现有微球偶联抗体后的溶液在液态中保存稳定性差的问题,本发明提供一种乳胶微球试剂冻干工艺。
7.本发明提供如下技术方案:一种乳胶微球试剂冻干工艺,包括以下步骤:s1、利用羧基乳胶微球进行抗体的固定,利用羧基基团与抗体上的氨基进行反应,羧基含量在0.15-0.2mmol/mg之间,所得微球试剂保存在ph为7.5
±
0.5的缓冲液中,缓冲液包含离子对、牛血清白蛋白、表面活性剂和防腐剂;
s2、向乳胶微球试剂溶液中添加冻干保护剂,冻干保护剂由糖类物质和两性离子型聚合物组合,冻干保护剂添加比例是乳胶微球试剂溶液质量的20%-50%,优选在30-40%之间,得乳胶微球混合溶液;s3、通过注射泵将乳胶微球混合溶液缓慢滴加到液氮容器中进行速冻,液氮溶液中的保留时间大于15min,以确保冷冻试剂定型,注射泵注射速度在1-10mm/min,获得质量均一的固体球形试剂;s4、液氮容器置于可进行固定速圆周运动的馏分收集器装置上,单位时间通过注射泵滴落到液体容器中的微球试剂可均匀的分散在液体容器底部,固体球形试剂不发生黏连或互相堆积而发生变形;s5、将球形固体试剂通过镊子转移至冻干容器中,放入冻干机进行冷冻干燥。
8.进一步的,冻干保护剂由糖类物质和两性离子型聚合物组合。
9.在上述技术方案中,糖类物质优选单糖类物质,单糖类物质为海藻糖、甘露醇、葡聚糖、果糖、半乳糖、核苷二磷酸糖中的一种或者多种组合,其组分含量占冻干保护剂的10-30%。
10.在上述技术方案中,所述两性离子型聚合物中两性离子基团同时含有碱性阳离子和酸性基阴离子,所述碱性阳离子为胺基盐离子、季铵或吡啶阳离子,所述酸性基阴离子为羧酸基、磺酸基、磷酸基或硫酸酯基,其组分含量占冻干保护剂的5-15%。
11.进一步的,所述两性离子基团为磷酸基类两性离子单体、磺酸基类两性离子单体、羧酸基类两性离子单体中的一种或多种。
12.进一步的,所述两性离子基团为2-甲基丙烯酰氧乙基磷酸胆碱、磷酸胆碱乙二醇丙烯酸酯,甘油磷酰基胆碱(例如n,n-二甲基-n-甲基丙烯酰胺基丙基-n-丙烷磺酸内盐),磺酸基甜菜碱和羧酸基甜菜碱(例如n,n-二甲基-n-甲基丙烯酰氧乙基-n-乙酸内盐)中的一种或多种。
13.本发明通过优化工艺路线,来提高冻干微球制剂的生产效率和自动化程度,主要通过使用注射泵将具有一定粘度的微球混合液按照恒定速度通过针管挤压形成大小均匀的液滴,注射泵的速度为1-10mm/min,平均在5-15s内形成小液滴流下。可同时控制多个注射泵完成多个试剂液滴的形成。其次,通过液氮对形成的小液滴进行速冻处理,装有液氮的容器放置在进行缓慢圆周运动的转盘上,固体小液滴经冷冻后形成后尺寸大小均一,球状完整的固体试剂,球状固体试剂在形成后可形成间隔排布,避免固体球状制剂互相堆叠导致形变和黏连。在大量制备固体微球制剂时,可在转盘旋转一周后,及时倒出多余的液氮溶液,并更换液氮容器,实现连续生产。最后使用镊子在容器底部收集凝固了的微球制剂,转入袋盖试剂管中,称量每个固体微球制剂的重量,对质量偏差较大的部分进行剔除,保证后继产品的性能恒定,并转移到冻干机中进行下一步的处理。
14.一种乳胶微球试剂冻干工艺以及在免疫比浊试剂上的应用,步骤s4中冷冻干燥的工艺,如下:s41、预冻:设定冻干机温度为-5℃;s42、装料:待设定温度到达后,将固体球形试剂装入塑料离心管中,打开管盖,放入冻干机隔板中层,方便后继压盖步骤;s43、冷冻:设置降温时间为20~40min,冻干机隔板温度降至-50℃后,继续冷冻持
续1~5h;s44、抽真空:设置真空度50pa,真空开启后,设置制冷温度为-60℃,降温时间为45~60min;s45、干燥阶段:-60℃持续7h,真空度10~20pa;-40℃持续10h,真空度5~10pa;-20℃持续1h,真空度10~20pa;-0℃持续1h,真空度10~20pa;-20℃持续1h,真空度10~20pa;s46、压盖:通过冻干机隔板进行压盖操作,压盖后恢复压力至常压。
15.一种乳胶微球试剂冻干工艺在免疫比浊试剂上的应用,制备冻干微球试剂,用于干式免疫比浊微球试剂。
16.本发明的冻干微球试剂可保存在单管容器中,试剂装配后可应用在诊断试剂上,试剂检测时加入纯水即可复溶,实现现配现用。这种冻干微球试剂由标记有抗体的微球和冻干保存液混合所得,并通过冻干工艺获得最终的产品形态。
17.与现有技术相比,本发明的有益效果是:(1)本发明使用了两性离子聚合物作为冻干赋形剂和保护剂,从保持微球电荷密度和降低微球试剂周围水含量的角度改善冻干试剂的性能。对比冻干微球试剂和常规液体试剂的检测性能,两者在检测性能下差异<10%,冻干试剂自身性能得到了很好的保存;(2)本发明的冻干制剂,能够显著提高偶联有抗体类蛋白的微球的稳定性,优于常规液态方式储存微球。以微球的稳定性下降<15%为界限,偶联aso抗体蛋白的微球的冻干制剂在常温条件的保存时间可达24个月。而对于液态试剂2~8℃条件下保存的时间仅为9个月;偶联lp(a)单克隆抗体的微球的冻干制剂在常温条件的保存时间可达24个月,而液态试剂在2~8℃条件下保存的时间仅为7个月;(3)本发明的冻干制剂适用于偶联了不同抗原蛋白或抗体蛋白的微球,通用性较好;(4)本发明中通过注射泵恒定流速生成液体和转盘收集固体微球制剂,设计了微球冻干工艺的连续性生产流程,可实现扩大规模的制备,可提高生产效率;(5)本发明采用冻干方式保存偶联有蛋白的微球,比冷冻低温储存运输微球,更加经济便捷,有效降低了偶联有蛋白的微球产品的运输与储存成本。
18.本发明可以很好解决目前诊断试剂中普遍存在的试剂稳定性问题和运输成本问题,具有非常广阔的免疫检验应用价值。
附图说明
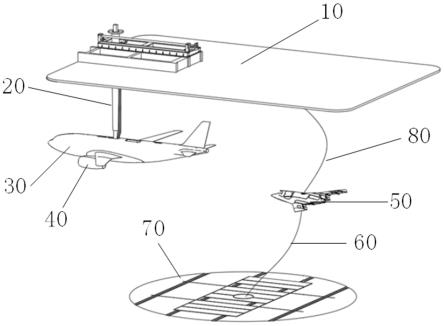
19.图1为本发明注射泵挤压液体速冻成型示意图。
20.图2为本发明单管收集冷冻固体制剂过程示意图。
21.图3为本发明冻干试剂和液体试剂性能对比图。
具体实施方式
[0022] 下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他
实施例,都属于本发明保护的范围。
[0023]
实施例1冻干保护剂的制备配制方法:称取30g的海藻糖、40g甘露醇、5g葡聚糖、加入800ml的纯化水中并搅拌溶解,称取25g的聚甲基丙烯酰氧基磷酸胆碱(分子量mw3000-5000),量取300μl的proclin300,加入溶液中并混匀,使用纯化水,将配制的溶液体积定容至1l,最后,使用0.22μm的滤膜,对溶液进行过滤。
[0024]
实施例2aso抗体的微球标记标记方法:量取2mg的130nm羧基微球,加入0.1mnah2po4缓冲液进行稀释,ph6.2。稀释后的微球浓度为1mg/ml。将装有微球溶液的离心管,放置于涡旋震荡及超声约20s,使微球充分混匀重悬。依次向微球中依次加入10μlnhs及10μledc,涡旋震荡混匀后,将离心管避光在旋转混合仪上300rpm室温孵育30分钟。将活化后的微球通过离心15000rpm,离心30min,去除上清液,加入0.1mnah2po4缓冲液进行复溶,并加入aso抗体溶液到活化好的微球中,涡旋震荡及超声后,将离心管避光在旋转混合仪上300rpm室温孵育2h。反应结束后加入等体积的封闭缓冲液(100mmpbs,5%bsa,0.03%proclin300),涡旋震荡及超声重悬微球。将离心管在旋转混合仪上300rpm室温孵育30min。反应结束后,离心清洗微球,并使用封闭液对微球进行复溶,配置微球终浓度为2mg/ml。
[0025]
实施例3冻干微球制剂的配置将上述方法制备的偶联有抗体的微球与冻干保护剂的混合,其中微球偶联物与冻干保护剂的混合比例为7:3,混合后的微球溶液使用涡旋混匀仪进行混匀。
[0026]
混匀后的微球溶液,通过注射泵,按照5mm/min的速度,缓慢挤压液体滴入装有液氮的容器中,液氮容器通过自动馏分收集器进行圆周旋转,实现微球混合溶液的小液滴周期性的分布在容器底部,避免固体微球制剂的互相堆叠与积压变形。在收集完毕后,使用镊子对固体微球制剂进行分装,分装在带盖离心管后,对每个固体制剂的重量进行测定,去除偏移平均重量的固体制剂。
[0027]
实施例4固体微球制剂冻干冻干机预冻,设定温度为-55℃,预冻3h。待预冻结束后将装配好的固体微球制剂放入冻干机中,并抽真空进行升华,真空度10pa,在-40℃升华25h。升华结束后设定进行解析干燥阶段,维持冻干机真空度压力为15pa,缓慢升温至20℃,再维持温度3h结束。待冻干流程结束后,使用自动压盖将单支试剂管进行封口。回复真空度至常压,去除冻干微球试剂,放置于常温条件下保存。
[0028]
实施例5乳胶微球冻干试剂在aso项目上的应用在胶乳增强免疫比浊项目对aso项目进行性能对比分析,在日立7170-a全自动生化分析仪上进行检测,检测参数为:主波505,副幅波0,样本进样量2ul,r1进样量240,r2进样量60ul。其中r1试剂为含有2.0%peg6000的100mmpbs(ph7.4),r2试剂为常规液体胶乳微球试剂(包含致敏胶乳溶液)和胶乳微球冻干试剂。其中冻干试剂在测试前溶解,现配现用。标准品和质控品分别为aso重组蛋白,辅料为小牛白蛋白,控品由bio-rad公司提供。
[0029]
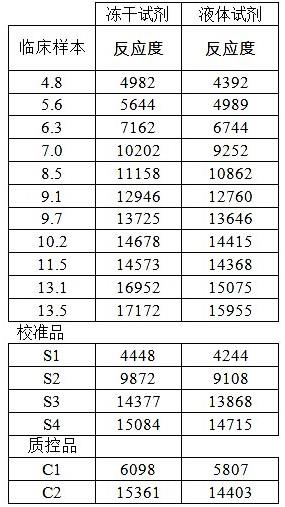
表1冻干试剂和液体是在aso项目上的对比
通过直线拟合计算得到结果为:血清aso线性回归方程为y=0.96x-161,相关系数r=0.994,r2=0.989。可认为冻干试剂在测定范围内与液体试剂匹配度较高,检测系统的线性较好,两者偏差较小。
[0030]
实施例6乳胶微球冻干试剂在aso项目上稳定性的验证加速稳定性考察,在37℃高温条件下,通过热破坏试验考察实施例5中冻干保护剂所制备的微球冻干制剂的稳定性情况,并与常规液体试剂做对比。每个点测试重复2次,取均值。分别在37℃高温保存的第0、3、4、5、6、7天进行取样测试,结果反馈液体试剂在加速至第7天时,出现了降幅超标了情况,而冻干微球试剂的稳定性持续保持良好,最大波动不超过7%。
[0031]
表237℃加速稳定性能考察表
在常温0-25℃保存条件下,跟踪了微球冻干试剂长达2年的试剂稳定性,并与在2-8℃保存下的液体试剂做对比。分别验证了1、3、5、7、9、12、18和24个月的测试数据情况,结果反馈在持续跟进2年的常温保存条件下,冻干微球试剂的性能保持恒定,试剂测值的波动情况在15%以内,冻干试剂可保持长期的稳定。
[0032]
表3 冻干试剂长期稳定考察表
跟踪了液体试剂在2-8℃下长期保存的稳定性测试情况,试剂在第7个月后开始明显的稳定性下降情况,在第9个月的试剂性能降幅超过15%,在为期24个月的稳定性考察中,试剂性能最大降幅达到30%。液体试剂的稳定性效果不及冻干试剂稳定性。
[0033]
表4 液体试剂长期稳定考察
微球冻干工艺试剂的开发改进,需要满足一方面可简化试剂的保存条件,另一方面尽量避免或降低冻干对试剂性能的损失。
[0034]
本发明在前人的基础上一方面使用糖类物质,使得试剂在冻干过程中避免形成较多的冰结晶对纳米微球造成破坏,另一方面创新性的引入两性离子聚合物,这一组分一方面改善液体的粘度,使得微球试剂较容易在冻干中赋形,另一方面增加整体溶液中的电荷密度,对微球表面的电荷进行稳定荷保护。另外两性离子聚合物是带有等量正负电荷的聚合物,它通过离子溶剂化作用,与水分子具有很强的结合能力,来降低微球试剂在溶液中周围水的密度,从而降低冷冻对微球试剂的破坏影响。常见的两性离子聚合物单体有2-甲基丙烯酰氧基磷酸胆碱(mpc)、磺酸基甜菜碱和羧酸基甜菜碱等,使用这类物质作为冻干保护剂,这类物质可以与微球形成一层类似膜结构的表面,避免冰冻对微球试剂的影响,降低微球试剂复溶后性能的损失。将两性离子聚合物引入冻干配方中的文献或者专利尚未见到。
[0035]
本发明还设计了一套自动化制备冻干制剂的方法,可轻松实现大规模生产。微球冻干配方通过注射泵缓慢定量的滴加进入液氮中,并维持15min以上进行定型。这种速冻方法一方面可避免液体试剂在逐渐结冰过程中浓度差异和冰结晶对微球结构的破坏,同时小体积冷冻制剂方便控制成品试剂的用量,也易于装配。冻干配方液的溶液粘度较高,可精确控制每个小液滴质量,并形成成品质量均一的冷冻物。此外通过自动馏分收集器可均匀收集冷冻的试剂液滴,避免冷冻液滴相互黏连和挤压变形。此套设备无需人工操作可简化工艺路线,并避免人工操作产生的误差。微球冻干试剂未在文献或专利中见到明确表述具体的冻干工艺路线和操作方法。
[0036]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。