n-(3-甲基-5-异噻唑基)-2-氧代-3-(2h)-苯并噁唑乙酰胺的药物应用
技术领域
1.本发明属于医药技术领域,具体涉n-(3-甲基-5-异噻唑基)-2-氧代-3-(2h)-苯并噁唑乙酰胺在制备阿尔茨海默病防治药物中的应用。
背景技术:
2.阿尔茨海默症(alzheimer’s disease,ad)又名老年痴呆,是一种进行性、破坏认知与记忆功能的持续性神经退行性疾病。它的主要病理特征是以β淀粉样蛋白(β-amyloid protein,aβ)沉积和tau蛋白过度磷酸化形成的神经原纤维缠结(neurofibrillary tangle,nft)为主。ad患者的表现为自主行为能力下降,认知能力丧失,如记忆和语言障碍、行为紊乱和情绪障碍。据世界卫生组织报告,每年约有990万新的痴呆症病例被诊断出来。据预测,到2032年,痴呆症患者的总数将接近7500万。在过去的20年里,ad的治疗一直是药物发现和临床研究领域的热门话题。
3.目前,治疗ad的药物是胆碱酯酶抑制剂5和(n-甲基-d-天门冬氨酸)nmda受体拮抗剂。不幸的是,这些药物只能缓解ad的症状,但不能逆转ad的病理过程。ad患者脑组织出现明显的萎缩,在这些部位可见明显的由β淀粉样蛋白(aβ)沉积形成的老年斑,是ad发展的关键因素。近年来,许多研究表明ad的神经化学和神经病理学改变均与aβ有着密切联系,当aβ产生过多或者清除减少时,aβ蛋白聚集成为具有高度神经毒性的多聚体并引起机体产生氧化应激、炎症及tau蛋白高度磷酸化等诱导神经元死亡的因素。因此,aβ是ad发病中最重要的病理因素,基于淀粉样蛋白级联假说的药物治疗策略可以降低aβ的水平,这可能与ad的治疗有关。因此,寻找新药的工作正在兴起。
4.foxo1是foxo家族中最重要的转录因子,在调节细胞增殖、氧化应激、脑缺血、自噬、神经退行性疾病等方面起着重要作用。foxo1可能是一个潜在的治疗ad的目标。但到目前为止,还没有用于治疗ad的foxo1激动剂。
技术实现要素:
5.本发明的目的在于提供n-(3-甲基-5-异噻唑基)-2-氧代-3-(2h)-苯并噁唑乙酰胺在制备阿尔茨海默病防治药物中的应用。将该化合物简称化合物d,其结构式如下所示:
6.通过一系列的下游生物学实验验证了该化合物对于foxo1的调节能力。发现该化合物d是一个foxo1激动剂,可以上调foxo1下游基因转录活性。同时发现在体外的细胞实验
体系中,化合物d可以抑制bace1的活性,并且可以减少sh-sy5y细胞中aβ的生成。因此,化合物d可用于制备阿尔茨海默病防治药物。本发明优点:通过计算机辅助药物设计技术发现了foxo1的天然化合物d,通过体外生物学实验,证明了该分子是foxo1的天然激动剂;在人源细胞系中,证明了化合物d可以作为foxo1激动剂,抑制bace1活性并且减少aβ的生成。具有开发防治阿尔茨海默病药物价值。
附图说明
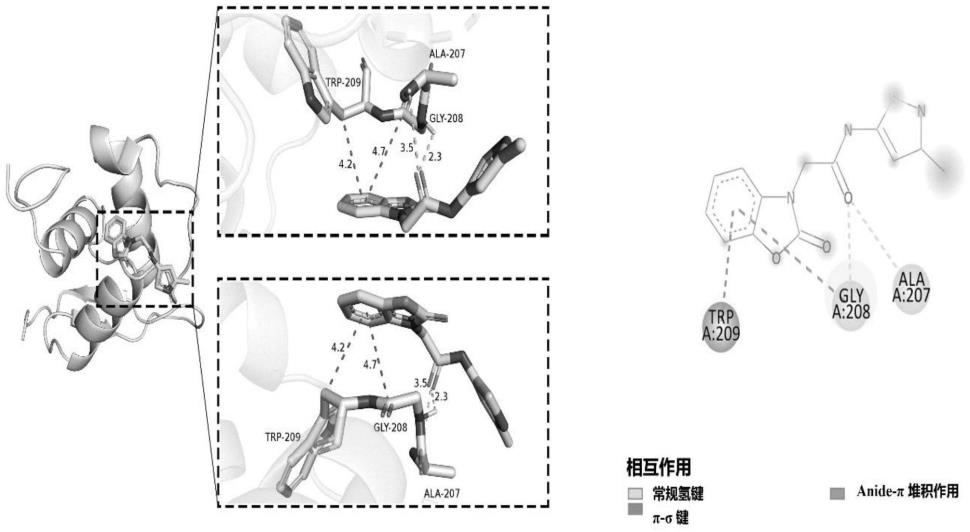
7.图1为本发明化合物d与foxo1的分子对接结果。
8.图2为本发明化合物d与foxo1复合物的分子动力学模拟结果。
9.图3为本发明不同剂量的化合物d对sh-sy5y细胞活力影响结果。
10.图4为本发明化合物d能提高foxo1下游相关基因的转录活性。
11.图5为本发明化合物d降低sh-sy5y细胞中aβ的产生结果。
12.图6为本发明化合物d通过抑制bace1的活性减少aβ的产生。
具体实施方式
13.在既往的研究中,发明人发现了转录因子foxo1可能在ad的发病过程中起到了调控作用。相对于目前正在开发的药物来说,foxo1作为药物靶点的优势在于其是foxo家族中最重要的转录因子,在调节细胞增殖、氧化应激、脑缺血、自噬、神经退行性疾病等方面起着重要作用。foxo1在不同的脑区都有表达,尤其是在海马和皮层区。发明人发现foxo1在6月龄app/ps1转基因小鼠的皮层组织的表达量明显低于野生小鼠。在ad细胞模型中过表达foxo1可以有效地降低aβ和tau蛋白过度磷酸化水平。这些结果表明,foxo1可能是一个潜在的治疗ad的药物靶标。
14.本发明化合物d对于ad治疗的药理作用属于“first in class”范畴,而不属于“me too”或者“me better”范畴。
15.以下实施例进一步说明本发明的内容,但不应理解为对本发明的限制。在不背离本发明精神和实质的情况下,对本发明方法、步骤或条件所作的修改和替换,均属于本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。实施例1
16.1、使用autodock vina软件进行foxo1蛋白准备。从附图1的分子对接结果显示,化合物d能够与foxo1具有较好的结合,主要结合力为氢键,对接的能量为:-7.9kcal/mol,提示该小分子具有较好的结合。
17.2、使用gromacs进行分子动力学模拟试验。从附图2的rmsd、rmsf和rg图结果可以看出化合物d和foxo1复合物在50ns模拟过程保持稳定,说明化合物d稳定可靠,可以有效靶向foxo1,整个复合物系统结构稳定。
18.3、将sh-sy5y细胞以每孔1.5
×
104的数目种在96孔板里,培养24h后换上含有不同浓度化合物d的培养液,继续培养细胞。24h后进行cck-8细胞毒性试验。
19.如图3的结果可知,在显微镜下观察经化合物d处理后的细胞密度,结果与cck-8检测结果一致。80μμ、100μm药物作用24小时后,sh-sy5y细胞出现明显的核聚集、碎裂等明显
的细胞凋亡症状,20、40、60、80、100μm药物作用24小时后sh-sy5y细胞数依次减少,表明在化合物d作用24小时后,sh-sy5y细胞活性降低具有浓度依赖性。用cck-8检测不同浓度的化合物d对sh-sy5y细胞活力的影响。与对照组相比,化合物d处理的sh-sy5y细胞的细胞活力随着浓度的增加而逐渐降低。
20.4、进一步验证了化合物d对foxo1活性的影响。western blot和rt-qpcr结果显示,发现化合物d增强foxo1下游靶蛋白的转录活性。随着化合物d浓度的增加,foxo1下游基因p21、bim和pparγ的蛋白表达水平和核酸转录水平均显著升高,但并未引起foxo1蛋白表达水平的增加。如图4所示,随着化合物d浓度的增加,p21和bim的蛋白表达水平逐渐升高,而pparγ的表达水平随着化合物d浓度的增加而逐渐降低。这些结果表明,化合物d是一种能显著激活foxo1转录水平的foxo1激动剂。
21.5、将sh-sy5y细胞以每孔1.5
×
104的数目种在96孔板里,培养24h后加入含有不同浓度化合物d的培养液,24h后收集细胞蛋白和上清液,使用humanβ-amyloid(1-40)和β-amyloid(1-42)elisa试剂盒,如图5所示,发现化合物d可以降低aβ1-40和aβ1-42的产生。
22.6、为了研究化合物d的作用机制,检测了aβ代谢过程中相关蛋白app、adam10、ps1和bace1的水平。如图6所示,发现bace1的表达水平随着化合物d的浓度的增加而显著下降。在化合物d处理下,app、adam10和ps1的表达无明显差异。总体而言,化合物d在高浓度时下调sh-sy5y细胞bace1的表达,从而显著下调sh-sy5y细胞内和培养基上清液中aβ1-40、aβ1-42的水平,化合物d作为foxo1激动剂对ad有潜在的治疗作用。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。