1.本发明属于图像处理领域,具体涉及用于医学图像分类的证据推理方法及可视化证据标记方法。
背景技术:
2.随着经济技术的发展和人们生活水平的提高,人们对于健康的关注也越来越高。近年来,随着深度学习在医疗技术领域的创新和不断应用,智慧医疗领域也得到了快速发展。计算机辅助分类方法在医学图像分类任务上的应用,极大方便了医护人员,并且也节约了大量的人力和物力。
3.但是现有的计算机辅助分类方法仍然存在缺陷:一是模型的分类过程如同黑箱一样,对用户并没有提供可信的分类依据;如输入一张医学图像(比如眼底图像),现有的模型只能给出正常或异常的分类结果,但并没有提供支撑判断分类的证据;而没有证据支撑的辅助分类过程在医学领域是不可接受。二是现有的计算机辅助分类方法不具备推理能力;现有的方法通过低语义的信息与医学图像分类概率建立关联,容易造成伪相关,导致分类结果的可靠性不高,准确性也不好。
技术实现要素:
4.本发明的目的之一在于提供一种用于医学图像分类的证据推理方法,其中包含特征聚合投票和动态图网络推理结构能够使得分类过程更加可信和透明,而且具有较好的可解释性,可靠性高、准确性好。
5.本发明的目的之二在于提供一种包括了用于医学图像分类的证据推理方法的可视化证据标记方法。
6.本发明提供的这种用于医学图像分类的证据推理方法,包括如下步骤:
7.s1.获取已有的医学图像,并与各个医学图像的真实标签进行一一对应标记,得到训练数据集,再提取医学图像的特征图;
8.s2.构建用于医学图像分类的证据推理原始模型:
9.构建证据推理模型:
10.s2.1.采用特征聚合投票的方式将医学图像所对应的特征图转化为符号结点;一个符号结点表示一类医学图像属性;
11.s2.2.以步骤s2.1得到的符号结点作为图网络的结点,以结点与结点之间的相关性为图网络的边,构建图网络;
12.s2.3.对全局属性的相关性进行建模,并采用步骤s2.2得到的图网络进行证据推理,得到支撑医学图像分类的证据信息,并将证据信息量化为数值参数;
13.利用构建的证据推理模型,进行医学图像的分类:
14.s2.4.设定医学图像的原始概率分布,并采用步骤s2.3得到的量化后的证据信息对医学图像的原始概率分布进行优化;
15.s2.5.对分类结果进行数值化评估;
16.s3.采用步骤s1得到的训练数据集,对步骤s2构建的用于医学图像分类的证据推理原始模型进行训练,得到用于医学图像分类的证据推理模型;
17.s4.采用步骤s3得到的用于医学图像分类的证据推理模型,对实际的待分类的医学图像进行分类,并给出对应的分类证据。
18.步骤s1所述的获取已有的医学图像,并与各个医学图像的真实标签进行一一对应标记,得到训练数据集,再提取医学图像的特征图,具体为将已有的医学图像分为正常和异常,并将分类结果作为真实标签,与医学图像进行一一对应,从而构建训练数据集,然后采用resnet50骨架网络提取医学图像的特征图。
19.步骤s2.1所述的采用特征聚合投票的方式将医学图像所对应的特征图转化为符号结点;一个符号结点表示一类医学图像属性,具体包括如下步骤:
20.聚合投票利用特征图f的每个像素值对每个节点以不同的投票权重进行投票,然后每个节点把所有像素值的投票信息进行聚合,结果代表每一种医学图像属性;具体为采用如下算式进行计算:
[0021][0022]
式中pn为每一类的医学图像属性;h为特征图f的长;w为特征图f的高;fi为局部特征;wg为维度转化矩阵;为局部特征fi对每个节点nn投票的权重,且vn为可训练的投票权重,n为医学图像属性的个数。
[0023]
步骤s2.2所述的以步骤s2.1得到的符号结点作为图网络的结点,以结点与结点之间的相关性为图网络的边,构建图网络,具体包括如下步骤:
[0024]
构造图网络g={n,ε},其中医学图像属性作为节点sm,且sm∈n,n为医学图像属性的个数;两个医学图像属性的关联边为(sm,sn),且(sm,sn)∈ε,ε为关联边的集合;a为m类属性之间的邻接矩阵,且为长为m、高为m的矩阵。
[0025]
步骤s2.3所述的对全局属性的相关性进行建模,并采用步骤s2.2得到的图网络进行证据推理,得到支撑医学图像分类的证据信息,并将证据信息量化为数值参数,具体包括如下步骤:
[0026]
a.采用如下规则,使得图网络在所有符号节点sm∈n上进行置信传播:
[0027][0028]
式中h
t
为t时刻特征结点信息;σ(.)为relu激活函数;为归一化度矩阵;h
t-1
为t-1时刻特征结点信息;w
t-1
为可训练的权重矩阵;为t-1时刻归一化的邻接矩阵,且a
t-1
为t-1时刻的邻接矩阵,im为单位矩阵;
[0029]
b.学习医学图像属性之间的关系,推理得到局部属性与结构的关系,从而得到用于支撑医学图像分类的证据;通过如下损失函数约束邻接矩阵的内在关系:
[0030][0031][0032]
式中a
t
为t时刻的邻接矩阵,为t时刻归一化后邻接矩阵的第i行;lr为学习率;l为损失函数;为t时刻邻接矩阵的第i行;为t时刻邻接矩阵第i行的最小值;为t时刻邻接矩阵第i行的最大值;
[0033]
c.采用如下算式计算得到证据向量:
[0034]
e-,e
=mlp(σ(conv(concat(f,f'))))
[0035]
式中e
为支撑医学图像分类为异常的证据,e-为支撑医学图像分类为正常的证据;mlp(.)为多层感知机;conv(.)为采用1*1的卷积核进行处理的操作;为原始特征图;f'为推理后的特征图,且由h
t
拉伸得到h为特征图f'的长,w为特征图f'的高,c1为f'的通道数;concat(.)为f和f'在通道上相加的操作函数,且
[0036]
步骤s2.4所述的设定医学图像的原始概率分布,并采用步骤s2.3得到的量化后的证据信息对医学图像的原始概率分布进行优化,具体包括如下步骤:
[0037]
设定医学图像的原始概率密度为beta分布b(pi|αi,βi),其中pi为分类预测概率,αi为证据化参数,βi为证据化参数;采用如下公式对概率密度分布进行优化:
[0038][0039][0040]
式中ld为损失函数;n为医学图像的总数;yi为医学图像的真实标签,且yi∈{0,1};pi为分类预测概率;|| ||为求均方差;γ()为gamma函数;αi为证据化参数,且αi=e
1;βi为证据化参数,且βi=e- 1;l为损失函数;λ为超参数,且λ∈[0,1];kl(x||y)为kullback-leibler散度;为beta分布,为优化的证据化参数,为优化的证据化参数;b(pi|《1,1》)为参数为1的beta分布。
[0041]
步骤s2.5所述的对分类结果进行数值化评估,包括计算分类结果的预测概率、置信度和不确定性;具体如下步骤:
[0042]
采用如下算式计算医学图像分类的预测概率:
[0043][0044]
[0045]
式中p
为异常的概率;p-为正常的概率;α,β为证据化参数;e为证据总和,且e=α β;
[0046]
采用如下算式计算预测结果为p
和p-的置信度:
[0047][0048][0049]
式中c
为预测结果为异常的概率的置信度;c-为预测结果为正常的概率的置信度;
[0050]
最后,计算得到预测结果为不确定的概率的置信度u为u=1-c
-c-。
[0051]
本发明还提供了一种包括了上述用于医学图像分类的证据推理方法的可视化证据标记方法,还包括如下步骤:
[0052]
s5.根据步骤s4得到的分类结果,将分类结果所对应的证据进行可视化,并对证据进行可视化标记和输出,从而得到具有证据可视化标记的医学图像。
[0053]
本发明提供的这种用于医学图像分类的证据推理方法及可视化证据标记方法,首次将证据推理集成到深度学习框架中,可用于提高医学图像分类的可解释性和泛化性;同时提出了一种新的显式证据推理范式来计算医学图像的分类结果;因此本发明证据推理方法具有较好的可解释性,而且可靠性高,准确性好。
附图说明
[0054]
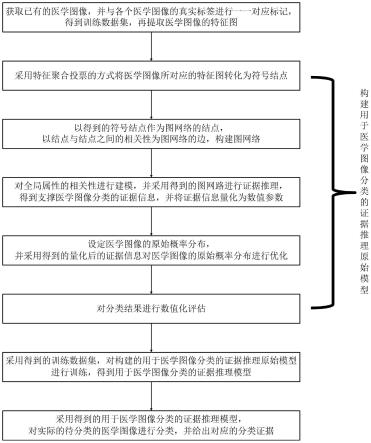
图1为本发明的证据推理方法的方法流程示意图。
[0055]
图2为本发明的可视化证据标记方法的方法流程示意图。
[0056]
图3为本发明的可视化证据标记方法的标记结果示意图。
具体实施方式
[0057]
如图1所示为本发明的证据推理方法的方法流程示意图:本发明提供的这种用于医学图像分类的证据推理方法,包括如下步骤:
[0058]
s1.获取已有的医学图像,并与各个医学图像的真实标签进行一一对应标记,得到训练数据集,再提取医学图像的特征图;具体为将已有的医学图像分为正常和异常,并将分类结果作为真实标签,与医学图像进行一一对应,从而构建训练数据集,然后采用resnet50骨架网络提取医学图像的特征图;
[0059]
s2.构建用于医学图像分类的证据推理原始模型:
[0060]
构建证据推理模型:
[0061]
s2.1.采用特征聚合投票的方式将医学图像所对应的特征图转化为符号结点;一个符号结点表示一类医学图像属性;具体包括如下步骤:
[0062]
聚合投票利用特征图f的每个像素值对每个节点以不同的投票权重进行投票,然后每个节点把所有像素值的投票信息进行聚合,结果代表每一种医学图像属性;具体为采用如下算式进行计算:
[0063][0064]
式中pn为每一类的医学图像属性;h为特征图f的长;w为特征图f的高;fi为局部特征;wg为维度转化矩阵;为局部特征fi对每个节点nn投票的权重,且vn为可训练的投票权重,n为医学图像属性的个数;
[0065]
与现有技术不同之处在于设计了一个聚合投票部分;现有技术就直接利用特征图的零散像素级别的低语义信息作为诊断依据,此做法缺乏可解释性,也不能作为诊断的证据;本发明提出的聚合投票利用特征图f的每个像素值对每个节点以不同的投票权重进行投票,然后每个节点把所有像素值的投票信息进行聚合,结果代表每一种眼底图像属性;特征提取的输入为医学图像,标签为图像级别;采用resnet50网络进行特征提取,得到特征图f;本发明的本步骤所提取的医学图像的属性语义信息分布在整个特征图中,准确性和可靠性更高;
[0066]
s2.2.以步骤s2.1得到的符号结点作为图网络的结点,以结点与结点之间的相关性为图网络的边,构建图网络;具体包括如下步骤:
[0067]
构造图网络g={n,ε},其中医学图像属性作为节点sm,且sm∈n,n为医学图像属性的个数;两个医学图像属性的关联边为(sm,sn),且(sm,sn)∈ε,ε为关联边的集合;a为m类属性之间的邻接矩阵,且为长为m、高为m的矩阵;在初始化阶段利用全连接的方式构造它们之间的关系;
[0068]
s2.3.现有技术是利用得到的特征图f进行拉伸,然后经过全连接层和softmax得到医学图像的预测分类概率;但是,现有技术是对零散的像素级别的语义信息与医学图像之间的相关性进行建模,是一种数据拟合的方式,容易导致伪相关关系,从而使得分类出现误差或错误,分类过程的可解释性不强;因此本发明提出动态图推理的方式,利用得到的医学图像属性的全局相关性进行推理,从而得到局部的医学图像属性以及属性之间的关系作为证据,来支撑医学图像分类的结果;不同的医学图像属性经过动态图网络推理,可以得到局部的医学图像属性的关系,并对这局部医学图像属性与医学图像分类概率进行建模,量化成证据的形式来支撑医学图像分类的结果;
[0069]
因此,本发明对全局属性的相关性进行建模,并采用步骤s2.2得到的图网络进行证据推理,得到支撑医学图像分类的证据信息,并将证据信息量化为数值参数;具体包括如下步骤:
[0070]
a.采用如下规则,使得图网络在所有符号节点sm∈n上进行置信传播:
[0071][0072]
式中h
t
为t时刻特征结点信息;σ(.)为relu激活函数;为归一化度矩阵;h
t-1
为t-1时刻特征结点信息;w
t-1
为可训练的权重矩阵;为t-1时刻归一化的邻接矩阵,且a
t-1
为t-1时刻的邻接矩阵,im为单位矩阵;
[0073]
b.学习医学图像属性之间的关系,推理得到局部属性与结构的关系,从而得到用于支撑医学图像分类的证据;通过如下损失函数约束邻接矩阵的内在关系:
[0074][0075][0076]
式中a
t
为t时刻的邻接矩阵,为t时刻归一化后邻接矩阵的第i行;lr为学习率;l为损失函数;为t时刻邻接矩阵的第i行;为t时刻邻接矩阵第i行的最小值;为t时刻邻接矩阵第i行的最大值;
[0077]
c.采用如下算式计算得到证据向量:
[0078]
e-,e
=mlp(σ(conv(concat(f,f'))))
[0079]
式中e
为支撑医学图像分类为异常的证据,e-为支撑医学图像分类为正常的证据;mlp(.)为多层感知机;conv(.)为采用1*1的卷积核进行处理的操作;为原始特征图;f'为推理后的特征图,且由h
t
拉伸得到h为特征图f'的长,w为特征图f'的高,c1为f'的通道数;concat(.)为f和f'在通道上相加的操作函数,且
[0080]
利用构建的证据推理模型,进行医学图像的分类:
[0081]
s2.4.设定医学图像的原始概率分布,并采用步骤s2.3得到的量化后的证据信息对医学图像的原始概率分布进行优化;具体包括如下步骤:
[0082]
设定医学图像的原始概率密度为beta分布b(pi|αi,βi),其中pi为分类预测概率,αi为证据化参数,βi为证据化参数;采用如下公式对概率密度分布进行优化:
[0083][0084][0085]
式中ld为损失函数;n为医学图像的总数;yi为医学图像的真实标签,且yi∈{0,1};pi为分类预测概率;|| ||为求均方差;γ()为gamma函数;αi为证据化参数,且αi=e
1;βi为证据化参数,且βi=e- 1;l为损失函数;λ为超参数,且λ∈[0,1];kl(x||y)为kullback-leibler散度;为beta分布,为优化的证据化参数,为优化的证据化参数;b(pi|《1,1》)为参数为1的beta分布;
[0086]
s2.5.对分类结果进行数值化评估;具体如下步骤:
[0087]
采用如下算式计算医学图像分类的预测概率:
[0088]
[0089][0090]
式中p
为异常的概率;p-为正常的概率;α,β为证据化参数;e为证据总和,且e=α β;
[0091]
采用如下算式计算预测结果为p
和p-的置信度:
[0092][0093][0094]
式中c
为预测结果为异常的概率的置信度;c-为预测结果为正常的概率的置信度;
[0095]
最后,计算得到预测结果为不确定的概率的置信度u为u=1-c
-c-;
[0096]
s3.采用步骤s1得到的训练数据集,对步骤s2构建的用于医学图像分类的证据推理原始模型进行训练,得到用于医学图像分类的证据推理模型;
[0097]
s4.采用步骤s3得到的用于医学图像分类的证据推理模型,对实际的待分类的医学图像进行分类,并给出对应的分类证据。
[0098]
以下以眼底图像为实施对象,对本发明的证据推理方法进行进一步说明:
[0099]
本发明提供的这种用于眼底图像分类的证据推理方法,包括如下步骤:
[0100]
s1.获取已有的眼底图像,并与各个眼底图像的真实标签进行一一对应标记,得到训练数据集,再提取眼底图像的特征图;具体为将已有的眼底图像分为正常和异常,并将分类结果作为真实标签,与眼底图像进行一一对应,从而构建训练数据集,然后采用resnet50骨架网络提取眼底图像的特征图;
[0101]
s2.构建用于眼底图像分类的证据推理原始模型:
[0102]
构建证据推理模型:
[0103]
s2.1.采用特征聚合投票的方式将眼底图像所对应的特征图转化为符号结点;一个符号结点表示一类眼底图像属性;具体包括如下步骤:
[0104]
聚合投票利用特征图f的每个像素值对每个节点以不同的投票权重进行投票,然后每个节点把所有像素值的投票信息进行聚合,结果代表每一种眼底图像属性(包括视杯、视盘、静脉、动脉等);具体为采用如下算式进行计算:
[0105][0106]
式中pn为每一类的眼底图像属性;h为特征图f的长;w为特征图f的高;fi为局部特征;wg为维度转化矩阵;为局部特征fi对每个节点nn投票的权重,且vn为可训练的投票权重,n为眼底图像属性的个数;
[0107]
s2.2.以步骤s2.1得到的符号结点作为图网络的结点,以结点与结点之间的相关性为图网络的边,构建图网络;具体包括如下步骤:
[0108]
构造图网络g={n,ε},其中眼底图像属性作为节点sm,且sm∈n,n为眼底图像属性的个数;两个眼底图像属性的关联边为(sm,sn),且(sm,sn)∈ε,ε为关联边的集合;a为m类属性之间的邻接矩阵,且为长为m、高为m的矩阵;在初始化阶段利用全连接的方式构造它们之间的关系;
[0109]
s2.3.对全局属性的相关性进行建模,并采用步骤s2.2得到的图网络进行证据推理,得到支撑眼底图像分类的证据信息,并将证据信息量化为数值参数;不同的眼底属性(静脉、动脉、视杯、视盘等)经过动态图网络推理,可以得到局部的眼底属性(视杯、视盘等)的关系,并对这局部眼底属性与眼底图像分类概率进行建模,量化成证据的形式来支撑眼底图像分类的结果;具体包括如下步骤:
[0110]
a.采用如下规则,使得图网络在所有符号节点sm∈n上进行置信传播:
[0111][0112]
式中h
t
为t时刻特征结点信息;σ(.)为relu激活函数;为归一化度矩阵;h
t-1
为t-1时刻特征结点信息;w
t-1
为可训练的权重矩阵;为t-1时刻归一化的邻接矩阵,且a
t-1
为t-1时刻的邻接矩阵,im为单位矩阵;
[0113]
b.学习眼底图像属性之间的关系,推理得到局部属性与结构的关系,从而得到用于支撑眼底图像分类的证据;通过如下损失函数约束邻接矩阵的内在关系:
[0114][0115][0116]
式中a
t
为t时刻的邻接矩阵,为t时刻归一化后邻接矩阵的第i行;lr为学习率;l为损失函数;为t时刻邻接矩阵的第i行;为t时刻邻接矩阵第i行的最小值;为t时刻邻接矩阵第i行的最大值;
[0117]
c.采用如下算式计算得到证据向量:
[0118]
e-,e
=mlp(σ(conv(concat(f,f'))))
[0119]
式中e
为支撑眼底图像分类为异常的证据,e-为支撑眼底图像分类为正常的证据;mlp(.)为多层感知机;conv(.)为采用1*1的卷积核进行处理的操作;为原始特征图;f'为推理后的特征图,且由h
t
拉伸得到h为特征图f'的长,w为特征图f'的高,c1为f'的通道数;concat(.)为f和f'在通道上相加的操作函数,且
[0120]
利用构建的证据推理模型,进行眼底图像的分类:
[0121]
s2.4.设定眼底图像的原始概率分布,并采用步骤s2.3得到的量化后的证据信息对眼底图像的原始概率分布进行优化;具体包括如下步骤:
[0122]
设定眼底图像的原始概率密度为beta分布b(pi|αi,βi),其中pi为分类预测概率,αi为证据化参数,βi为证据化参数;采用如下公式对概率密度分布进行优化:
[0123][0124][0125]
式中ld为损失函数;n为眼底图像的总数;yi为眼底图像的真实标签,且yi∈{0,1};pi为分类预测概率;|| ||为求均方差;γ()为gamma函数;αi为证据化参数,且αi=e
1;βi为证据化参数,且βi=e- 1;l为损失函数;λ为超参数,且λ∈[0,1];kl(x||y)为kullback-leibler散度;为beta分布,为优化的证据化参数,为优化的证据化参数;b(pi|《1,1》)为参数为1的beta分布;
[0126]
s2.5.对分类结果进行数值化评估;具体如下步骤:
[0127]
采用如下算式计算眼底图像分类的预测概率:
[0128][0129][0130]
式中p
为异常的概率;p-为正常的概率;α,β为证据化参数;e为证据总和,且e=α β;
[0131]
采用如下算式计算预测结果为p
和p-的置信度:
[0132][0133][0134]
式中c
为预测结果为异常的概率的置信度;c-为预测结果为正常的概率的置信度;
[0135]
最后,计算得到预测结果为不确定的概率的置信度u为u=1-c
-c-;
[0136]
s3.采用步骤s1得到的训练数据集,对步骤s2构建的用于眼底图像分类的证据推理原始模型进行训练,得到用于眼底图像分类的证据推理模型;
[0137]
s4.采用步骤s3得到的用于眼底图像分类的证据推理模型,对实际的待分类的眼底图像进行分类,并给出对应的分类证据。
[0138]
如图2所示为本发明的可视化证据标记方法的方法流程示意图:本发明提供的这种包括了上述用于医学图像分类的证据推理方法的可视化证据标记方法,包括如下步骤:
[0139]
s1.获取已有的医学图像,并与各个医学图像的真实标签进行一一对应标记,得到训练数据集,再提取医学图像的特征图;具体为将已有的医学图像分为正常和异常,并将分类结果作为真实标签,与医学图像进行一一对应,从而构建训练数据集,然后采用resnet50骨架网络提取医学图像的特征图;
[0140]
s2.构建用于医学图像分类的证据推理原始模型:
[0141]
构建证据推理模型:
[0142]
s2.1.采用特征聚合投票的方式将医学图像所对应的特征图转化为符号结点;一个符号结点表示一类医学图像属性;具体包括如下步骤:
[0143]
聚合投票利用特征图f的每个像素值对每个节点以不同的投票权重进行投票,然后每个节点把所有像素值的投票信息进行聚合,结果代表每一种医学图像属性;具体为采用如下算式进行计算:
[0144][0145]
式中pn为每一类的医学图像属性;h为特征图f的长;w为特征图f的高;fi为局部特征;wg为维度转化矩阵;为局部特征fi对每个节点nn投票的权重,且vn为可训练的投票权重,n为医学图像属性的个数;
[0146]
s2.2.以步骤s2.1得到的符号结点作为图网络的结点,以结点与结点之间的相关性为图网络的边,构建图网络;具体包括如下步骤:
[0147]
构造图网络g={n,ε},其中医学图像属性作为节点sm,且sm∈n,n为医学图像属性的个数;两个医学图像属性的关联边为(sm,sn),且(sm,sn)∈ε,ε为关联边的集合;a为m类属性之间的邻接矩阵,且为长为m、高为m的矩阵;在初始化阶段利用全连接的方式构造它们之间的关系;
[0148]
s2.3.对全局属性的相关性进行建模,并采用步骤s2.2得到的图网络进行证据推理,得到支撑医学图像分类的证据信息,并将证据信息量化为数值参数;具体包括如下步骤:
[0149]
a.采用如下规则,使得图网络在所有符号节点sm∈n上进行置信传播:
[0150][0151]
式中h
t
为t时刻特征结点信息;σ(.)为relu激活函数;为归一化度矩阵;h
t-1
为t-1时刻特征结点信息;w
t-1
为可训练的权重矩阵;为t-1时刻归一化的邻接矩阵,且a
t-1
为t-1时刻的邻接矩阵,im为单位矩阵;
[0152]
b.学习医学图像属性之间的关系,推理得到局部属性与结构的关系,从而得到用于支撑医学图像分类的证据;通过如下损失函数约束邻接矩阵的内在关系:
[0153][0154][0155]
式中a
t
为t时刻的邻接矩阵,为t时刻归一化后邻接矩阵的第i行;lr为学习率;l
为损失函数;为t时刻邻接矩阵的第i行;为t时刻邻接矩阵第i行的最小值;为t时刻邻接矩阵第i行的最大值;
[0156]
c.采用如下算式计算得到证据向量:
[0157]
e-,e
=mlp(σ(conv(concat(f,f'))))
[0158]
式中e
为支撑医学图像分类为异常的证据,e-为支撑医学图像分类为正常的证据;mlp(.)为多层感知机;conv(.)为采用1*1的卷积核进行处理的操作;为原始特征图;f'为推理后的特征图,且由h
t
拉伸得到h为特征图f'的长,w为特征图f'的高,c1为f'的通道数;concat(.)为f和f'在通道上相加的操作函数,且
[0159]
利用构建的证据推理模型,进行医学图像的分类:
[0160]
s2.4.设定医学图像的原始概率分布,并采用步骤s2.3得到的量化后的证据信息对医学图像的原始概率分布进行优化;具体包括如下步骤:
[0161]
设定医学图像的原始概率密度为beta分布b(pi|αi,βi),其中pi为分类预测概率,αi为证据化参数,βi为证据化参数;采用如下公式对概率密度分布进行优化:
[0162][0163][0164]
式中ld为损失函数;n为医学图像的总数;yi为医学图像的真实标签,且yi∈{0,1};pi为分类预测概率;|| ||为求均方差;γ()为gamma函数;αi为证据化参数,且αi=e
1;βi为证据化参数,且βi=e- 1;l为损失函数;λ为超参数,且λ∈[0,1];kl(x||y)为kullback-leibler散度;为beta分布,为优化的证据化参数,为优化的证据化参数;b(pi|《1,1》)为参数为1的beta分布;
[0165]
s2.5.对分类结果进行数值化评估;具体如下步骤:
[0166]
采用如下算式计算医学图像分类的预测概率:
[0167][0168][0169]
式中p
为异常的概率;p-为正常的概率;α,β为证据化参数;e为证据总和,且e=α β;
[0170]
采用如下算式计算预测结果为p
和p-的置信度:
[0171]
[0172][0173]
式中c
为预测结果为异常的概率的置信度;c-为预测结果为正常的概率的置信度;
[0174]
最后,计算得到预测结果为不确定的概率的置信度u为u=1-c
-c-;
[0175]
s3.采用步骤s1得到的训练数据集,对步骤s2构建的用于医学图像分类的证据推理原始模型进行训练,得到用于医学图像分类的证据推理模型;
[0176]
s4.采用步骤s3得到的用于医学图像分类的证据推理模型,对实际的待分类的医学图像进行分类,并给出对应的分类证据;
[0177]
s5.根据步骤s4得到的分类结果,将分类结果所对应的证据进行可视化,并对证据进行可视化标记和输出,从而得到具有证据可视化标记的医学图像。
[0178]
采用本发明提供的这种可视化证据标记方法,在眼底图像上进行可视化证据标记,标记结果如图3所示:图3(a)为获取的原始的眼底图像,图3(b)中标记的高亮部分为视盘部分;图3(c)中标记的高亮部分为视杯部分;图3(d)中标记的高亮部分为动脉部分;图3(e)中标记的高亮部分为静脉部分。从图3中可以看到,本发明的可视化证据标记方法,能够在医学图像(以眼底图像为例)上进行较好的证据标记。
[0179]
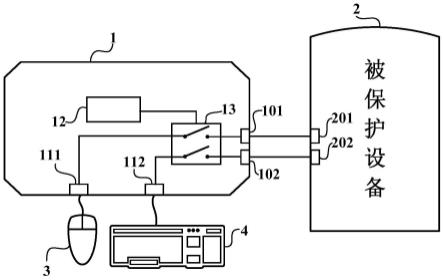
本发明提出的这种可视化证据标记方法,可以用于现有的医疗设备中的医学图像(以眼底图像为例)成像设备;在具体实施时,医学图像(以眼底图像为例)成像设备正常获取人员的医学图像(以眼底图像为例);然后采用本发明提供的可视化证据标记方法对获取的医学图像(以眼底图像为例)进行分类,以及证据可视化标记(比如采用高亮的形式、矩形框标记的形式等);接下来将得到的分类结果和标记结果在医学图像(以眼底图像为例)上进行二次成像,就得到了包含分类结果和证据标记结果的医学图像(以眼底图像为例);最后将带有分类结果和标记结果的医学图像(以眼底图像为例)输出;此时医学图像(以眼底图像为例)成像设备就成为了一台具有更多功能的医学图像(以眼底图像为例)设备。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。