1.本发明涉及煤炭热解领域,具体涉及一种煤炭热力学参数构建方法。
背景技术:
2.而煤炭的常规利用带来的环境污染和温室气体效应日趋严重。而将煤的热转化过程解耦成煤热解、气化和半焦的热转化的煤炭分级转化技术也被视为煤炭清洁高效利用的关键技术。煤和煤炭产品的热力学性质的估算在发展和分析与煤有关的热转化过程如热解、气化、液化中是十分重要的,对煤炭热力学参数的估算,在对煤炭热转化进行热力学第一定律和第二定律分析时尤为必要。虽然目前对煤和煤炭产品的比热等方面进行了许多研究,但涉及煤的标准摩尔生成熵等热力学参数的构建较少。
技术实现要素:
3.针对现有技术中缺乏煤炭标准摩尔生成熵等热力学参数构建方法的问题,本发明提出一种煤炭热力学参数构建方法。
4.为实现上上述目的,本发明技术方案如下:
5.一种煤炭热力学参数构建方法,包括如下步骤:
6.对于煤炭进行元素分析,确定煤炭中各元素与c元素的摩尔比;
7.基于所述摩尔比,构建煤炭完全燃烧反应,根据所述煤炭完全燃烧反应的化学计量数,计算煤炭的标准摩尔生成焓;
8.基于所述摩尔比,构建煤炭生成反应,根据所述煤炭生成反应的化学计量数,分段计算得到煤炭的标准摩尔生成熵;
9.根据所述标准摩尔生成焓和标准摩尔生成熵,计算煤炭的标准摩尔生成吉布斯自由能。
10.进一步的,所述摩尔比包括煤炭中h、o、n和s元素与c元素的摩尔比,分别为α1、α2、α3和α4,得到煤炭分子式为ch
α1oα2nα3sα4
。
11.进一步的,所述煤炭完全燃烧反应为:进一步的,所述煤炭完全燃烧反应为:
12.进一步的,所述煤炭的标准摩尔生成焓δhf通过燃烧热的公式计算,燃烧热的公式如下:
[0013][0014]
其中,vi为煤炭完全燃烧反应中四种产物的化学计量数,
△hf,i
为每种反应产物的标准摩尔生成焓,q为煤燃烧反应热。
[0015]
进一步的,所述煤炭生成反应为:
[0016][0017]
得到石墨型碳c、固体硫s以及氢气、氮气、氧气的化学计量数,依次为1、α4、α2,分别记为vc、vs、
[0018]
进一步的,所述分段计算煤炭的标准摩尔生成熵中,第一阶段标准摩尔生成熵δs1计算方式如下:
[0019][0020]
其中,c(c)
p,
、c(s)
p,
、c(h2)
p,
、c(n2)
p,
、c(o2)
p,
分别为石墨型c、固体硫s以及氢气、氮气、氧气的定压热容;δhsx为固体硫的相变热,ta为第一阶段升温温度,tsx为固体硫的相变温度。
[0021]
进一步的,所述分段计算煤炭的标准摩尔生成熵中,第二阶段标准摩尔生成熵δs2计算方式如下:
[0022][0023]
其中:tcx为石墨型c单质的相变温度,δhcx为石墨型碳c单质的相变热,δho、δhh、δhn分别为氧气、氢气、氮气的化学键键能;tb为第二阶段升温温度,dk为气体最高解离温度。
[0024]
进一步的,所述分段计算煤炭的标准摩尔生成熵中,第三阶段标准摩尔生成熵δs3计算方式如下:
[0025][0026]
其中:r为摩尔气体常数,ni为c、h、o、n、s几种原子的物质的量,xi为c、h、o、n、s几种原子物质的量分数,xi为煤炭单质中主要的化学键比例,δdhi为各个化学键的化学键键能,ti为各个化学键的解离温度。
[0027]
进一步的,所述分段计算煤炭的标准摩尔生成熵中,第四阶段标准摩尔生成熵δs4计算方式如下:
[0028][0029]
其中,c(coal)
p,m
为煤的定压热容,tc为降温温度。
[0030]
进一步的,所述煤炭的标准摩尔生成熵为分段计算的所有标准摩尔生成熵之和。
[0031]
与现有技术相比,本发明有益效果有:
[0032]
通过煤炭热力学参数的构建,有利于运用热力学方法对煤热转化涉及的关键产物如焦油各组分的生成反应进行研究,有助于明确反应氛围、总压及温度等关键参数对煤热
转化关键反应的吉布斯自由能和平衡常数的影响规律,总体有助于明确适宜的反应条件并为产物调控提供理论指导。
附图说明
[0033]
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
[0034]
在附图中:
[0035]
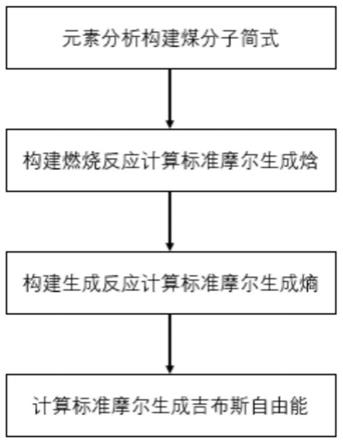
图1为本发明一种煤炭热力学参数构建方法总体流程示意图;
[0036]
图2为本发明一种煤炭热力学参数构建方法中标准摩尔生成熵的计算示意图。
具体实施方式
[0037]
下面将参考附图并结合实施例来详细说明本发明。需要说明的是,在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
[0038]
以下详细说明均是示例性的说明,旨在对本发明提供进一步的详细说明。除非另有指明,本发明所采用的所有技术术语与本发明所属领域的一般技术人员的通常理解的含义相同。本发明所使用的术语仅是为了描述具体实施方式,而并非意图限制根据本发明的示例性实施方式。
[0039]
实施例1
[0040]
一种煤炭热力学参数构建方法,包括:标准摩尔生成焓的计算以及标准摩尔生成熵的计算和标准摩尔生成吉布斯自由能的计算。
[0041]
首先对于煤炭进行元素分析,确定煤炭中h、o、n和s元素与c元素的摩尔比,分别为α1、α2、α3和α4,设定煤炭分子式为ch
α1oα2nα3sα4
。再分别计算标准摩尔生成焓、标准摩尔生成熵以及标准摩尔生成吉布斯自由能。
[0042]
标准摩尔生成焓的计算包括:
[0043]
首先构建煤炭完全燃烧反应:
[0044][0045]
得到煤炭完全燃烧反应中四种产物的化学计量数vi,查询得到每种反应产物的标准摩尔生成焓为
△hf,i
,通过经验公式计算煤燃烧反应热记为q,通过燃烧热的公式计算煤炭的标准摩尔生成焓:
[0046][0047]
其中,δhf为煤炭的标准摩尔生成焓。
[0048]
煤炭的标准摩尔生成焓可以用于判断煤热解生成焦油组分在不同温度和压力条件下的反应是吸热反应还是放热反应,并估算反应能耗,焦油组分包括苯酚、甲酚、环烷烃、芳香族烃等。
[0049]
标准摩尔生成熵的计算包括:
[0050]
构建煤炭生成反应:
[0051][0052]
得到石墨型碳c、固体硫s以及氢气、氮气、氧气的化学计量数,,依次为1、α4、α2,分别记为vc、vs、
[0053]
将煤炭由相关单质生成划分为四个步骤:
[0054]
第一阶段、石墨型碳c和固体硫s先可逆等压升温到石墨的升华温度3970.15k,而固态硫在717.28k时升华为气态硫,氢气、氮气以及氧气分别可逆等压升温到气体可以解离的最高温度6900k,本步骤主要涉及可逆等压升温和等温可逆相变两个过程,计算如下:
[0055][0056]
其中,c(c)
p,
、c(s)
p,
、c(h2)
p,
、c(n2)
p,
、c(o2)
p,
分别为石墨型c、固体硫s以及氢气、氮气、氧气的定压热容;δhsx为固体硫的相变热,ta为第一阶段升温温度,tsx为固体硫的相变温度;
[0057]
第二阶段、石墨在5103.15k时先等温可逆相变为气态石墨,然后与气态硫一起升温到整个体系的最高解离温度,气态的各个物质中化学键断裂转变为原子态,假设认为由气态到原子态也可视为一种相变过程,用相变过程的熵计算公式对其过程的熵变进行计算。整个步骤主要涉及可逆等压升温和可逆相变两个过程,计算如下:
[0058][0059]
其中,δhcx为石墨型c单质的相变温度,δhcx为石墨型碳c单质的相变热,δho、δhh、δhn分别为氧气、氢气、氮气的化学键键能;tb为第二阶段升温温度,tdk为气体最高解离温度,本实施例中取6900k;
[0060]
第三阶段、几种原子态物质等温等压可逆混合,根据煤炭生成过程中主要化学键比例,生成煤炭单质。假设在整个体系最高温下生成相关化学键且原子生成化学键的过程也视为一种相变过程,整个步骤主要涉及等温等压可逆和可逆相变两个过程,计算如下:
[0061][0062]
其中,r为摩尔气体常数,ni、xi分别为c、h、o、n、s几种原子的物质的量和物质的量分数,xi为煤炭单质中主要的化学键比例,δdhi为各个化学键的化学键键能,ti为各个化学键的解离温度;
[0063]
第四阶段、煤炭作为一种混合物,主要部分为有规则结构的石墨型碳,因此假设用
石墨的升华温度以及升华热代替煤炭的相关数据。煤炭先从体系的最高温度降到升华温度,在进行等温可逆相变,然后在降到标准状况下的温度。计算公式如下:
[0064][0065]
其中,c(coal)
p,m
为煤的定压热容,tc为降温温度。
[0066]
第五、将前四个阶段计算得到的熵进行加和,得到煤炭的标准摩尔生成熵δs。
[0067]
标准摩尔生成吉布斯自由能的计算包括:
[0068]
根据计算得到的煤炭的标准摩尔生成焓和熵可求得热力学温度下的煤炭标准摩尔生成吉布斯自由能δg:
[0069]
δg=δh
f-tδs
[0070]
式中:t为热力学温度,本实施例中取298.15k;
[0071]
煤炭的标准摩尔生成吉布斯自由能用于判断煤热解生成的焦油组分在哪些反应温度和反应压力下发生哪些反应,焦油组分包括苯酚、甲酚、环烷烃、芳香族烃等。
[0072]
实施例2
[0073]
本实施例针对实施例1进行实际计算说明,具体如下。
[0074]
选取一种神府煤进行元素分析,其中,α1、α2、α3和α4是根据煤元素分析的结果确定的神府煤中h、o、n、s元素与c元素的摩尔比。确定煤的分子简式为ch
0.761o0.273n0.01s0.005
,其次构建煤炭生成反应:
[0075]
c(s) 0.3805h2(g) 0.1365o2(g) 0.005n2(g) 0.005s(s)
[0076]
=ch
0.761o0.273n0.01s0.005
[0077]
神府煤元素分析(wt.%daf)
[0078]
chons68.864.4025.040.820.88 α1α2α3α
4 0.7610.2730.0100.005
[0079]
标准摩尔生成焓的计算:
[0080]
对于神府煤的完全燃烧反应,产物就包括h2o、co2、so2和n2,其各自的标准摩尔生成焓可以通过查找标准数据可得,其标准摩尔生成焓如表所示,神府煤的燃烧反应热可以通过经验公式进行计算,由此进行神府煤的标准摩尔生成焓的计算。
[0081] o2co2h2on2so2δfhm0(kj/mol)0-393.509-241.8180-296.830
[0082][0083]
根据q经验公式进行计算,得到反应产物的生成焓之和为-486.988kj/mol,煤燃烧反应热q为-415.718kj/mol,则神府煤的标准摩尔生成焓为-71.271kj/mol。
[0084]
标准摩尔生成熵的计算:
[0085]
1)考虑到固态硫的升华热为278.81kj/mol,升华温度为717.75k,计算得到的生成熵为δs1=109.66 1.942=111.602j/mol/k。
[0086][0087]
2)查表可得c-c原子标况下对应的键解离能为595.63kj/mol,s-s原子标况下对应的解离能为425.30kj/mol,计算得到:
[0088]
δs2=16.162 180.522 34.580=231.263j/mol/k。
[0089][0090]
3)参照shin煤模型中的化学键比例确定煤生成过程中的主要共价键,并对主要共价键的熵变进行计算,化学键生成过程的能变可以取相应化学键的解离能负值,考虑相应化学键在煤炭中的比例。计算得到
[0091]
δs3=17.50-217.637=-200.137j/mol/k。
[0092][0093]
4)采用石墨的升华温度以及升华热代替煤的相关数据,计算得到
[0094]
δs4=-180.526j/mol/k。
[0095][0096]
5)将上述四步的生成熵加和得到神府煤的标准摩尔生成熵
[0097][0098]
神府煤的标准摩尔生成吉布斯自由能计算如下:
[0099][0100]
由技术常识可知,本发明可以通过其它的不脱离其精神实质或必要特征的实施方案来实现。因此,上述公开的实施方案,就各方面而言,都只是举例说明,并不是仅有的。所有在本发明范围内或在等同于本发明的范围内的改变均被本发明包含。
[0101]
最后应当说明的是:以上实施例仅用以说明本发明的技术方案而非对其限制,尽管参照上述实施例对本发明进行了详细的说明,所属领域的普通技术人员应当理解:依然可以对本发明的具体实施方式进行修改或者等同替换,而未脱离本发明精神和范围的任何修改或者等同替换,其均应涵盖在本发明的权利要求保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。