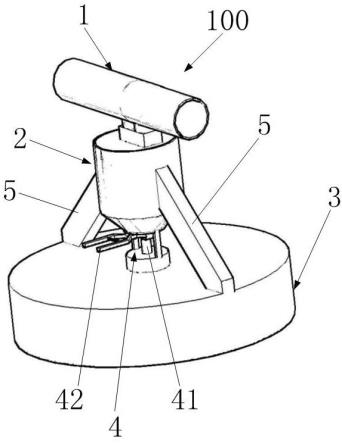
1.本发明涉及一种制备左乙拉西坦的方法,属于医药化工领域。
背景技术:
2.左乙拉西坦(levetiracetam,商品名为keppra)是由比利时公司ucb研制的一种新型抗癫痫药物,是一种乙酰吡咯烷类化合物,其化学名称为(s)-α-乙基-2-氧合-1-乙酰胺吡咯烷,结构如下所示:
[0003][0004]
ucb公司在专利us7122682中报道了一种通过(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯(ii)在氨水条件下氨解得到左乙拉西坦的方法,合成路线如下所示:
[0005][0006]
反应完成后,直接在真空条件下蒸馏除去氨水,然后甲苯拖带得到待精制固体,收率仅为92%,收率偏低;另外,由于左乙拉西坦在氨水条件下并不稳定,该工艺需要蒸馏除去大量的溶剂水,在蒸馏后期物料温度会有所升高,可能会造成左乙拉西坦的水解和消旋,生成异构体(ⅲ)和水解物(ⅳ),从而影响最终成品质量,具体数据见对比实施例一,因此该后处理方式不利于工业化大生产。
[0007][0008]
另有专利us7214803报道了一种用氨水氨解得到左乙拉西坦的方法,该专利中报道的后处理方式是在反应完成后,用15倍体积的二氯甲烷萃取反应液中的产品,浓缩二氯甲烷,仅得到73%的待精制固体,因此该后处理方式由于收率太低,也不利于工业化大生产。
技术实现要素:
[0009]
本发明的目的是提供一种获得高质量、高收率的由氨水氨解得到左乙拉西坦的方
法,包括以下步骤:
[0010]
(a)-5~5℃下,(s)-α-乙基-2-氧代-1-吡咯烷乙酸甲酯或(s)-α-乙基-2-氧代-1-吡咯烷乙酯与氨气在水中反应至完全;
[0011]
(b)除去体系中部分氨气,至体系ph小于12;
[0012]
(c)控制温度45℃以下蒸馏除去部分水;
[0013]
(d)料液中加入无机盐;
[0014]
(e)料液用有机溶剂萃取,有机溶剂萃取层蒸馏至干,得到左乙拉西坦。
[0015]
步骤(a)所述水用量为(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯质量的0.6~4倍;
[0016]
步骤(a)反应是否完全,可以使用tlc监控有无(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯残留确认反应是否完全。
[0017]
步骤(b)除去氨气的方法;优选在控制温度20~30℃、真空度≥0.09mpa除去氨气,也可以采用例如通入氮气等方法置换体系内氨气;优选除去氨气至体系ph=10~12;
[0018]
步骤(c)蒸馏除去的水量为初始水质量的0.2~0.7倍,优选0.5倍;蒸馏温度优选控制在40-45℃;
[0019]
步骤(d)中所述无机盐选自氯化钠、硫酸钠、氯化钙、硫酸镁、硫酸铵,优选氯化钠,用量为(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯质量的0.1~1倍;
[0020]
步骤(e)中所述萃取溶剂优选为二氯甲烷,二氯甲烷用量为(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯质量的1~5倍。优选用二氯甲烷萃取三遍。
[0021]
本发明的创新点在于:通过步骤(b)除去反应体系中过量的氨气,降低产品的在蒸馏溶剂过程中的水解和消旋;通过步骤(c)蒸馏除去部分溶剂,提高后续的萃取效率;通过步骤(d)加入无机盐降低左乙拉西坦在水体系中的溶解度,进一步提高萃取效率。通过以上操作可以在提高收率的同时不影响产品的质量,具有非常高的实用价值。
具体实施方式
[0022]
实施例一:
[0023]
反应釜中加入100g水和50g(s)-α-乙基-2-氧代-1-吡咯烷乙酸甲酯(异构体:0.2%),搅拌降温至-5℃,通氨气至饱和,停止通氨气,-5℃密闭保温搅拌反应9小时,tlc无(s)-α-乙基-2-氧代-1-吡咯烷乙酸甲酯残留,停止反应。反应溶液在30℃、真空0.095mpa抽氨气2小时,检测溶液ph=11.5,控制温度45℃真空除去50g溶剂,加入15g氯化钠,搅拌溶解,用200g二氯甲烷萃取3遍,合并二氯甲烷层,控制温度45℃以下浓缩至干,得到44.5g左乙拉西坦(收率97%,纯度:99.95%,异构体:0.3%)。
[0024]
实施例二:
[0025]
反应釜中加入150g水和50g(s)-α-乙基-2-氧代-1-吡咯烷乙酸乙酯(异构体:0.2%),搅拌降温至5℃,通氨气至饱和,停止通氨气,5℃密闭保温反应12小时,tlc无(s)-α-乙基-2-氧代-1-吡咯烷乙酸乙酯残留,停止反应。反应溶液在20℃、真空0.095mpa抽氨气2小时,检测溶液ph=11.6,控制温度40℃真空除去50g溶剂,加入25g硫酸钠,搅拌溶解,用100g二氯甲烷萃取3遍,合并二氯甲烷层,控制温度45℃以下浓缩至干,得到41.8g左乙拉西坦(收率96%,纯度:99.93%,异构体:0.4%)。
[0026]
对比实施例一:
[0027]
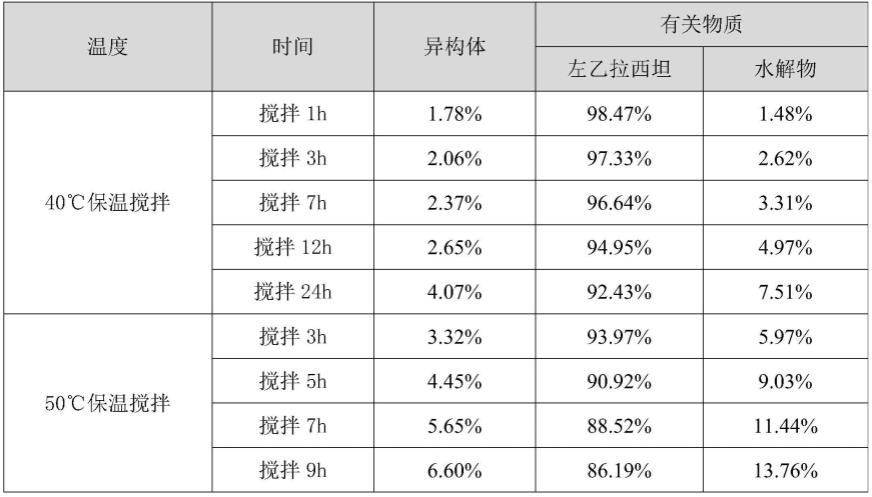
取左乙拉西坦50g(纯度:100.0%;异构体:n.d)溶解于100g浓氨水中,分别控制温度40℃,50℃,60℃搅拌1小时、3小时、7小时、12小时、24小时,取样检测纯度及异构体,数据如下:
[0028][0029][0030]
上述数据表明左乙拉西坦在40℃的氨水体系中稳定性差。
[0031]
对比实施例二:
[0032]
对比实施例二所有操作同实施例一,不同之处在于没有加入氯化钠,最终得到34.4g左乙拉西坦(收率:75%,纯度:99.96%,异构体:0.3%)。
[0033]
该实施例说明没有加入氯化钠会严重影响后续的萃取收率。
[0034]
对比实施例三:
[0035]
对比实施例二所有操作同实施例一,不同之处在于没有抽氨气的操作,最终得到36.7g左乙拉西坦(收率:80%,纯度:98.11%,异构体:0.4%)。
[0036]
该实施例说明没有抽氨气会严重影响后续的萃取收率及最终产品的质量。
[0037]
对比实施例四:
[0038]
对比实施例二所有操作同实施例一,不同之处在于抽氨气操作后没有蒸馏溶剂的操作,最终得到38.1g左乙拉西坦(收率:83%,纯度:99.31%,异构体:0.4%)。
[0039]
该实施例说明抽氨气操作后没有蒸馏溶剂会严重影响后续的萃取收率。
技术特征:
1.一种制备左乙拉西坦的方法,包括以下步骤:(a)-5~5℃下,(s)-α-乙基-2-氧代-1-吡咯烷乙酸甲酯或(s)-α-乙基-2-氧代-1-吡咯烷乙酯与氨气在水中反应至完全;(b)除去体系中部分氨气,至体系ph小于12;(c)控制温度45℃以下蒸馏除去部分水;(d)料液中加入无机盐;(e)料液用有机溶剂萃取,有机溶剂萃取层蒸馏至干,得到左乙拉西坦。2.根据权利要求1所述的方法,步骤(a)所述水用量为(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯质量的0.6~4倍。3.根据权利要求1所述的方法,步骤(b)除去氨气的方法选自:在控制温度20~30℃、真空度≥0.09mpa抽去氨气;优选除氨气至体系ph=10~12。4.根据权利要求1所述的方法,步骤(c)蒸馏除去的水量为初始水质量的0.2~0.7倍。5.根据权利要求4所述的方法,步骤(c)蒸馏除去的水量为初始水质量的0.5倍。6.根据权利要求1所述的方法,步骤(c)蒸馏的温度为40-45℃。7.根据权利要求1所述的方法,步骤(d)中所述无机盐选自氯化钠、硫酸钠、氯化钙、硫酸镁、硫酸铵,优选氯化钠。8.根据权利要求1所述的方法,步骤(d)无机盐的用量为(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯质量的0.1~1倍。9.根据权利要求1所述的方法,步骤(e)中所述萃取溶剂优选为二氯甲烷。10.根据权利要求1所述的方法,二氯甲烷用量为(s)-α-乙基-2-氧代-1-吡咯烷乙酸酯质量的1~5倍;优选用二氯甲烷萃取三遍。
技术总结
本发明公开了一种左乙拉西坦的制备方法,包括(S)-α-乙基-2-氧代-1-吡咯烷乙酸酯在水中氨化完成后,除去反应体系中过量的氨气,蒸馏除去部分水,并在萃取前加入无机盐,从而提高左乙拉西坦的收率和质量。高左乙拉西坦的收率和质量。
技术研发人员:颜峰峰 孟艳华 陈辉 龚玉龙 李敏勇 朱元勋
受保护的技术使用者:浙江华海药业股份有限公司
技术研发日:2021.03.30
技术公布日:2022/10/31
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。