1.本发明涉及食品安全检测技术领域,尤其涉及一种检测食品中芬太尼类新精神活性物质的方法。
背景技术:
2.芬太尼(fentanyl)是一种合成阿片类药物,于1960年由比利时科学家paul janseen首次合成,作为镇痛药出售,药理作用与吗啡类似,其镇痛效果为吗啡的80倍。芬太尼类药物为临床主要的麻醉用药,但药物剂量一旦过量,会导致呼吸抑制甚至死亡的危险。由于芬太尼具有强大的镇痛效果,能与中枢特异性受体相互作用,缓解疼痛,产生欣快(幸福)感的物质,这些特殊的管制药品物质若遵照药品管理的相关规定,合理的开具和使用这类药物,按照医嘱推荐的用法、用量来使用可治病就医,一旦滥用也就成为了我们熟知的毒品。芬太尼类新精神活性物质药效强、致死率高、滥用严重,芬太尼类物质被广泛使用,芬太尼非药用以及滥用的现象也随之出现。常见的有芬太尼、瑞芬太尼、舒芬太尼和卡芬太尼等6种,且新型芬太尼类似物不断出现(目前已有60余种报道)。目前,在全球范围内芬太尼类物质制造、走私和滥用问题越来越突出,由于芬太尼类新精神活性物质具有毒性强、变化快、品种多、缉查难等特点,对检测稽查工作提出了巨大的挑战。为保障正常公共秩序及国家安全,各国纷纷制定了相应的法律法规进行管控。
3.芬太尼(及其衍生物)同阿片μ受体结合并具有高亲和力、高脂溶性和强内在活性。这些既是芬太尼的重要药理药效作用特点,但也是导致其致命的不良反应或毒性的主要原因,表现为同时具有强效镇痛效应和高滥用潜力,可快速透过细胞膜通过血脑屏障进入大脑,短时间形成血药高峰,极易形成耐受和药物依赖。芬太尼可通过皮肤、粘膜吸收,因此,此类物质中毒不但发生在滥用者中,而且可发生在无防护措施情况下芬太尼类药物处置或接触的工作人员中。但是,目前防范芬太尼类新精神活性物质滥用,打击吸毒、贩毒及毒品走私方面均只局限于生物基质(如血液、尿液、毛发等)检测其含量,均为事后监测验证。
4.适用于对生物样品中芬太尼及其衍生药物进行初步筛选的分析方法多样,例如:免疫分析法、气相色谱-质谱、液相色谱-质谱(hplc-ms/ms)方法等。免疫分析是利用抗原(靶标)和抗体的特异性结合来进行测定的一种方法,但不同的免疫分析法对芬太尼类似物的交叉反应具有局限性,且某些交叉反应是未知的;气相色谱-质谱方法不能直接测定非挥发性、极性或热不稳定性的物质,需要对目标物进行衍生化反应,与未来分析化学快速、高效的发展趋势不符。液相色谱-质谱方法作为最常用的检测手段,相比较于气相色谱-质谱方法来说,该技术灵敏度更高,更加稳定,而且适用范围更广,但目前食品中芬太尼类物质的液相色谱-质谱检测方法报道较少,导致芬太尼类药物渗入食品的不法现象出现。目前食品中芬太尼类精神活性物质尚无国家权威检测标准,现有可查见的检测方法中仅有生物基体中芬太尼类的检测方法研究,是防范芬太尼类精神活性物质滥用的事后监测、验证。但是生物样品成分复杂,干扰物众多,对芬太尼的定性和定量分析带来一定难度,生物基质样品中芬太尼类物质检测前处理过程繁琐费时,需用大量有机溶剂,存在安全隐患且污染环境;
生物基质中芬太尼类药物浓度含量普遍较低,因此对芬太尼检测灵敏度要求较高,单一检测方法难以满足要求,一般需采用多种仪器综合分析和各种联用技术分析,生物基质样品检测芬太尼的相关检测方法不适用于食品基质。开展识别食品中芬太尼类精神活性物质的研究,将防范芬太尼类精神活性物质滥用从事后监测、验证,提前到前端的防范和源头控制,建立一种预处理方便快捷、检测灵敏、定量准确的方法来测定食品中芬太尼类精神活性物质成分的残留量,以便精准识别食品中是否含有芬太尼类精神活性物质。不仅对维护广大人民的身体健康和保障舌尖上的食品安全十分必要,而且为此类案件执法提供有力技术支撑,同时还可为公安机关对重点嫌疑人群、特殊行业从业人群开展对此类物质的监测,监控芬太尼类物质的滥用情况和流行趋势,防止危害社会事件的发生,以实现对芬太尼类精神活性物质准确、快速、实时监测。因此,亟需一种可靠、快速、准确的识别食品中芬太尼类物质的分析检测方法,并将其应用于解决实际问题。将防范芬太尼滥用、打击吸毒贩毒及毒品走私方面由事后监测验证转移到事前(前端)防范和源头控制。
技术实现要素:
5.本发明的目的在于提供一种检测食品中芬太尼类新精神活性物质的方法,本发明的检测方法能够准确、高效地识别食品中是否存在芬太尼类精神活性物质,可特异性区别各种芬太尼类似物及其异构体。
6.为了实现上述发明目的,本发明提供以下技术方案:
7.本发明提供了一种检测食品中芬太尼类新精神活性物质的方法,包括以下步骤:
8.(1)将待检测样品、水和乙腈混合后,再依次与无水醋酸钠粉末、无水硫酸镁混合,离心后取上清液,旋蒸、洗脱后过滤,得到待上机样品溶液;
9.(2)配制一系列浓度递增的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼的标准溶液,对标准溶液依次进行hplc-ms/ms检测,绘制上述7种成分的标准曲线;
10.(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度。
11.进一步地,步骤(1)中待检测样品、水、乙腈、无水醋酸钠粉末、无水硫酸镁的用量比例为待检测样品∶水∶乙腈∶无水醋酸钠粉末∶无水硫酸镁=1.80~2.20g∶2~5ml∶12~18ml∶1.4~1.6g∶5~8g。
12.进一步地,步骤(1)中离心的转速为3500~4500r/min,离心的时间为3~8min。
13.进一步地,步骤(1)中旋蒸的温度为40~50℃,旋蒸至样品中没有液体结束。
14.进一步地,步骤(1)中洗脱的洗脱液包括含有乙酸铵的甲酸水溶液和乙腈;所述含有乙酸铵的甲酸水溶液∶乙腈=8~12∶1,所述含有乙酸铵的甲酸水溶液中乙酸铵的浓度为3~8mmol/l,所述含有乙酸铵的甲酸水溶液中甲酸的含量为0.08%~0.12%。
15.进一步地,步骤(1)中采用0.22μm的尼龙66有机系滤膜进行过滤。
16.进一步地,步骤(1)中的待检测样品为固体食品或液体食品。
17.进一步地,步骤(3)中hplc-ms/ms检测的色谱条件为:采用waters acquity uplclm bhe c18色谱柱,进样量为4~6μl,色谱柱温度为34~36℃,流动相流量为0.2~0.4ml/min;
18.液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
19.梯度洗脱程序为:0~1.0min,10%流动相b;1.1~3.0min,65%流动相b;3.1~4.0min,65%流动相b;4.1~6.0min,10%流动相b。
20.进一步地,步骤(3)中hplc-ms/ms检测的色谱条件为:采用acquity uplc@hsst3色谱柱,进样量为4~6μl,色谱柱温度为34~36℃,流动相流量为0.2~0.4ml/min;
21.液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
22.梯度洗脱程序为:0~0.5min,10%流动相b;0.5~1.0min,35%流动相b;1.0~2.5min,35%流动相b;2.5~3.5min,35~10%流动相b;3.5~6.0min,10%流动相b。
23.进一步地,步骤(3)中hplc-ms/ms检测的质谱条件为:
24.可加热的电喷雾离子源;
25.正离子扫描模式;
26.离子源电压:5000~6000v;
27.离子源温度:500~600℃;
28.气帘气压:24~26psi;
29.碰撞气压:8~12psi;
30.喷雾气压:54~56psi;
31.加热气压:54~56psi;
32.采集模式:多反应监测模式mrm。
33.相比于现有技术,本发明的有益效果为:
34.本发明通过系列试验攻克复杂食品基体样品处理、高准确度识别与定量等关键技术,建立快速、准确、高效的食品中多种芬太尼的检测方法,从而识别食品中是否存在芬太尼类精神活性物质,将防范芬太尼类精神活性物质滥用从事后监测、验证,提前到前端的防范和源头控制。本发明不仅对维护广大人民的身体健康和保障舌尖上的食品安全十分必要,而且为此类案件执法提供有力技术支撑,同时还可为公安机关对重点嫌疑人群、特殊行业从业人群开展对此类物质的监测,监控芬太尼类物质的滥用情况和流行趋势,防止危害社会事件的发生,以实现对芬太尼类精神活性物质准确、快速、实时监测。芬太尼类因“芬太尼家族”的不断更新,出现了许多结构相似的类似物或结构异构体,本发明检测方法具有高分辨率和高特异性以区别各种芬太尼类似物及其异构体。相比于传统方法,操作简单快速,回收率高,检出限低,降低操作人员的要求。
附图说明
35.图1为实施例5以可乐为检测样品的检测图谱;
36.图2为7种芬太尼标准品的检测图谱。
具体实施方式
37.本发明提供了一种检测食品中芬太尼类新精神活性物质的方法,包括以下步骤:
38.(1)将待检测样品、水和乙腈混合后,再依次与无水醋酸钠粉末、无水硫酸镁混合,
离心后取上清液,旋蒸、洗脱后过滤,得到待上机样品溶液;
39.(2)配制一系列浓度递增的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼的标准溶液,对标准溶液依次进行hplc-ms/ms检测,绘制上述7种成分的标准曲线;
40.(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度。
41.在本发明中,将待检测样品、水和乙腈混合后,再依次与无水醋酸钠粉末、无水硫酸镁混合,离心后取上清液,旋蒸、洗脱后过滤,得到待上机样品溶液;所述待检测样品、水、乙腈、无水醋酸钠粉末、无水硫酸镁的用量比例为待检测样品∶水∶乙腈∶无水醋酸钠粉末∶无水硫酸镁=1.80~2.20g∶2~5ml∶12~18ml∶1.4~1.6g∶5~8g,优选为待检测样品∶水∶乙腈∶无水醋酸钠粉末∶无水硫酸镁=1.90~2.10g∶3~4ml∶14~16ml∶1.45~1.55g∶6~7g,进一步优选为待检测样品∶水∶乙腈∶无水醋酸钠粉末∶无水硫酸镁=1.95~2.05g∶3.3~3.7ml∶14.5~15.5ml∶1.48~1.52g∶6.2~6.8g。
42.在本发明中,所述离心的转速为3500~4500r/min,优选为3600~4300r/min,进一步优选为3800~4200r/min;所述离心的时间为3~8min,优选为4~7min,进一步优选为5~6min;所述离心使用allegra 64r冷冻台式高速离心机(美国beckman coulter公司)。
43.在本发明中,所述旋蒸的温度为40~50℃,优选为42~48℃,进一步优选为44~46℃;所述旋蒸的时间优选为旋蒸至样品中没有液体结束。
44.在本发明中,所述洗脱的洗脱液包括含有乙酸铵的甲酸水溶液和乙腈;所述含有乙酸铵的甲酸水溶液∶乙腈=8~12∶1,优选为9~11∶1,进一步优选为9.5~10.5∶1;所述含有乙酸铵的甲酸水溶液中乙酸铵的浓度为3~8mmol/l,优选为4~7mmol/l,进一步优选为5~6mmol/l;所述含有乙酸铵的甲酸水溶液中甲酸的含量为0.08%~0.12%,优选为0.09~0.11%,进一步优选为0.10%。
45.在本发明中,所述过滤优选为采用0.22μm的尼龙66有机系滤膜进行过滤。
46.在本发明中,所述待检测样品优选为固体食品或液体食品。
47.在本发明中,配制一系列浓度递增的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼的标准溶液,对标准溶液依次进行hplc-ms/ms检测,绘制上述7种成分的标准曲线。
48.在本发明中,将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度。
49.在本发明中,所述hplc-ms/ms检测的色谱条件为:采用waters acquityuplclm bhe c18色谱柱;进样量为4~6μl,优选为4.5~5.5μl,进一步优选为4.8~5.2μl;色谱柱温度为34~36℃,优选为34.5~35.5℃,进一步优选为34.8~35.2℃;流动相流量为0.2~0.4ml/min,优选为0.25~0.35ml/min,进一步优选为0.28~0.32ml/min;
50.液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
51.梯度洗脱程序为:0~1.0min,10%流动相b;1.1~3.0min,65%流动相b;3.1~4.0min,65%流动相b;4.1~6.0min,10%流动相b。
52.在本发明中,所述hplc-ms/ms检测的色谱条件为:采用acquity uplc@hsst3色谱
柱,进样量为4~6μl,优选为4.5~5.5μl,进一步优选为4.8~5.2μl;色谱柱温度为34~36℃,优选为34.5~35.5℃,进一步优选为34.8~35.2℃;流动相流量为0.2~0.4ml/min,优选为0.25~0.35ml/min,进一步优选为0.28~0.32ml/min;
53.液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
54.梯度洗脱程序为:0~0.5min,10%流动相b;0.5~1.0min,35%流动相b;1.0~2.5min,35%流动相b;2.5~3.5min,35~10%流动相b;3.5~6.0min,10%流动相b。
55.在本发明中,所述hplc-ms/ms检测的质谱条件为:
56.可加热的电喷雾离子源;
57.正离子扫描模式;
58.离子源电压:5000~6000v,优选为5200~5800v,进一步优选为5400~5600v;
59.离子源温度:500~600℃,优选为520~580℃,进一步优选为540~560℃;
60.气帘气压:24~26psi,优选为25psi;
61.碰撞气压:8~12psi,优选为9~11psi,进一步优选为10psi;
62.喷雾气压:54~56psi,优选为55psi;
63.加热气压:54~56psi,优选为55psi;
64.采集模式:多反应监测模式mrm。
65.在本发明中,所述hplc-ms/ms检测中质谱仪为ab3500三重四极杆质谱仪(美国absciex公司),色谱仪为岛津超高效液相色谱仪。
66.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
67.实施例1
68.本实施例提供了一种检测面包中芬太尼类新精神活性物质的方法,包括以下步骤:
69.(1)称取2.00g面包(其中添加浓度为400ng/ml的芬太尼、舒芬太尼、瑞芬太尼、奥芬太尼、乙酰芬太尼、卡芬太尼和浓度为80ng/ml的阿芬太尼各0.100ml),加入3.5ml水和15ml乙腈(分析纯),漩涡混合1min后,先加1.5g无水醋酸钠的混合粉末,迅速振摇,漩涡混合1min,再加入6g无水硫酸镁,迅速振摇,连续漩涡(2300r/min)混合5min,然后用4000r/min离心5min,移取全部上清液至鸡心瓶中,45℃旋蒸至干,用2ml洗脱液(组成为内含5mmol/l乙酸铵的0.1%甲酸水溶液:乙腈(色谱级)=9:1)洗脱,过0.22μm的尼龙66有机系滤膜,得到待上机样品溶液;
70.(2)标准储备液配制:分别精密称取芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼标准品各10mg(精确至0.01mg)至小烧杯中,加0.1%甲酸甲醇溶液溶解,溶液定量移入10ml容量瓶中,用0.1%甲酸甲醇溶液稀释至刻度,摇匀,配制成浓度均为1.0mg/ml的标准储备液;
71.混合标准中间溶液1配制:准确吸取浓度为1.0mg/ml的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼混合标准储备液各100μl于同一个100ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0μg/ml的混合标准中间溶液1;
72.混合标准中间溶液2配制:准确吸取混合标准中间溶液1.0ml于10ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为0.10μg/ml的混合标准中间溶液2;
73.标准工作溶液的配制:分别准确吸取混合标准中间溶液2和混合标准中间溶液1各200μl、400μl、1000μl于20ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,得芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0ng/ml、2.0ng/ml、5.0ng/ml、10.0ng/ml、20.0ng/ml、50.0ng/ml的系列标准工作溶液;
74.对上述得到的系列标准工作溶液依次进行hplc-ms/ms检测,以各溶液浓度为横坐标,测定得到的响应值为纵坐标,绘制各溶液标准曲线;
75.(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度;
76.所述hplc-ms/ms检测的色谱条件为:采用waters acquity uplclm bhe c18色谱柱,进样量为5μl,色谱柱温度为35℃,流动相流量为0.3ml/min;
77.液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
78.梯度洗脱程序为:0~1.0min,10%流动相b;1.1~3.0min,65%流动相b;3.1~4.0min,65%流动相b;4.1~6.0min,10%流动相b;
79.所述hplc-ms/ms检测的质谱条件为:
80.可加热的电喷雾离子源;
81.正离子扫描模式;
82.离子源电压:5500v;
83.离子源温度:550℃;
84.气帘气压:25psi;
85.碰撞气压:9psi;
86.喷雾气压:55psi;
87.加热气压:55psi;
88.采集模式:多反应监测模式mrm;
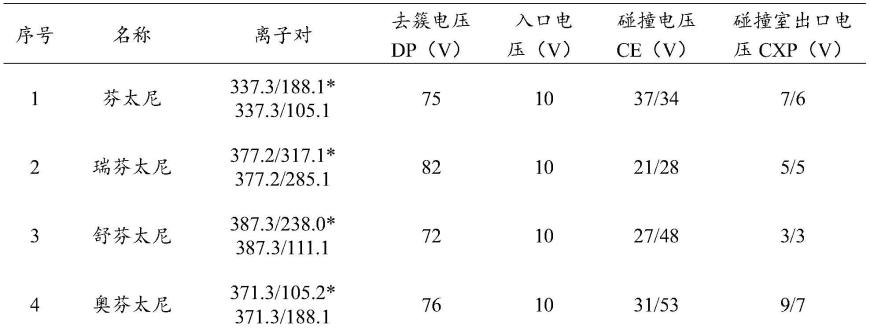
89.各化合物的质谱参数见表1:
90.表1:各化合物质谱参数
91.[0092][0093]
注:标注*为定量离子对
[0094]
实施例2
[0095]
本实施例提供了一种检测糕点中芬太尼类新精神活性物质的方法,包括以下步骤:
[0096]
(1)称取2.00g糕点(其中添加浓度为400ng/ml的芬太尼、舒芬太尼、瑞芬太尼、奥芬太尼、乙酰芬太尼、卡芬太尼和浓度为80ng/ml的阿芬太尼各0.100ml),加入3.0ml水和14ml乙腈(分析纯),漩涡混合1min后,先加1.55g无水醋酸钠的混合粉末,迅速振摇,漩涡混合1min,再加入7g无水硫酸镁,迅速振摇,连续漩涡(2300r/min)混合5min,然后用3500r/min离心6min,移取全部上清液至鸡心瓶中,50℃旋蒸至干,用2ml洗脱液(组成为内含5mmol/l乙酸铵的0.1%甲酸水溶液:乙腈(色谱级)=8:1)洗脱,过0.22μm的尼龙66有机系滤膜,得到待上机样品溶液;
[0097]
(2)标准储备液配制:分别精密称取芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼标准品各10mg(精确至0.01mg)至小烧杯中,加0.1%甲酸甲醇溶液溶解,溶液定量移入10ml容量瓶中,用0.1%甲酸甲醇溶液稀释至刻度,摇匀,配制成浓度均为1.0mg/ml的标准储备液;
[0098]
混合标准中间溶液1配制:准确吸取浓度为1.0mg/ml的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼混合标准储备液各100μl于同一个100ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0μg/ml的混合标准中间溶液1;
[0099]
混合标准中间溶液2配制:准确吸取混合标准中间溶液1.0ml于10ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为0.10μg/ml的混合标准中间溶液2;
[0100]
标准工作溶液的配制:分别准确吸取混合标准中间溶液2和混合标准中间溶液1各200μl、400μl、1000μl于20ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,得芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0ng/ml、2.0ng/ml、5.0ng/ml、10.0ng/ml、20.0ng/ml、50.0ng/ml的系列标准工作溶液;
[0101]
对上述得到的系列标准工作溶液依次进行hplc-ms/ms检测,以各溶液浓度为横坐标,测定得到的响应值为纵坐标,绘制各溶液标准曲线;
[0102]
(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度;
[0103]
所述hplc-ms/ms检测的色谱条件为:采用waters acquity uplclm bhe c18色谱柱,进样量为5μl,色谱柱温度为36℃,流动相流量为0.4ml/min;
[0104]
液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈
为流动相;
[0105]
梯度洗脱程序为:0~1.0min,10%流动相b;1.1~3.0min,65%流动相b;3.1~4.0min,65%流动相b;4.1~6.0min,10%流动相b;
[0106]
所述hplc-ms/ms检测的质谱条件为:
[0107]
可加热的电喷雾离子源;
[0108]
正离子扫描模式;
[0109]
离子源电压:5600v;
[0110]
离子源温度:540℃;
[0111]
气帘气压:25psi;
[0112]
碰撞气压:10psi;
[0113]
喷雾气压:55psi;
[0114]
加热气压:55psi;
[0115]
采集模式:多反应监测模式mrm;
[0116]
各化合物的质谱参数见表1。
[0117]
实施例3
[0118]
本实施例提供了一种检测奶粉中芬太尼类新精神活性物质的方法,包括以下步骤:
[0119]
(1)称取2.10g奶粉(其中添加浓度为400ng/ml的芬太尼、舒芬太尼、瑞芬太尼、奥芬太尼、乙酰芬太尼、卡芬太尼和浓度为80ng/ml的阿芬太尼各0.100ml),加入4.0ml水和16ml乙腈(分析纯),漩涡混合1min后,先加1.45g无水醋酸钠的混合粉末,迅速振摇,漩涡混合1min,再加入6.5g无水硫酸镁,迅速振摇,连续漩涡(2300r/min)混合5min,然后用4500r/min离心4min,移取全部上清液至鸡心瓶中,40℃旋蒸至干,用2ml洗脱液(组成为内含5mmol/l乙酸铵的0.1%甲酸水溶液:乙腈(色谱级)=10:1)洗脱,过0.22μm的尼龙66有机系滤膜,得到待上机样品溶液;
[0120]
(2)标准储备液配制:分别精密称取芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼标准品各10mg(精确至0.01mg)至小烧杯中,加0.1%甲酸甲醇溶液溶解,溶液定量移入10ml容量瓶中,用0.1%甲酸甲醇溶液稀释至刻度,摇匀,配制成浓度均为1.0mg/ml的标准储备液;
[0121]
混合标准中间溶液1配制:准确吸取浓度为1.0mg/ml的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼混合标准储备液各100μl于同一个100ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0μg/ml的混合标准中间溶液1;
[0122]
混合标准中间溶液2配制:准确吸取混合标准中间溶液1.0ml于10ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为0.10μg/ml的混合标准中间溶液2;
[0123]
标准工作溶液的配制:分别准确吸取混合标准中间溶液2和混合标准中间溶液1各200μl、400μl、1000μl于20ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,得芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0ng/ml、2.0ng/ml、5.0ng/ml、10.0ng/ml、20.0ng/ml、50.0ng/ml的系列标准工作溶液;
[0124]
对上述得到的系列标准工作溶液依次进行hplc-ms/ms检测,以各溶液浓度为横坐标,测定得到的响应值为纵坐标,绘制各溶液标准曲线;
[0125]
(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度;
[0126]
所述hplc-ms/ms检测的色谱条件为:采用acquity uplc@hsst3色谱柱,进样量为5μl,色谱柱温度为34℃,流动相流量为0.3ml/min;
[0127]
液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
[0128]
梯度洗脱程序为:0~0.5min,10%b;0.5~1.0min,35%b;1.0~2.5min,35%b;2.5~3.5min,35~10%b;3.5~6.0min,10%b;
[0129]
所述hplc-ms/ms检测的质谱条件为:
[0130]
可加热的电喷雾离子源;
[0131]
正离子扫描模式;
[0132]
离子源电压:5400v;
[0133]
离子源温度:560℃;
[0134]
气帘气压:25psi;
[0135]
碰撞气压:10psi;
[0136]
喷雾气压:55psi;
[0137]
加热气压:55psi;
[0138]
采集模式:多反应监测模式mrm;
[0139]
各化合物的质谱参数见表1。
[0140]
实施例4
[0141]
本实施例提供了一种检测牛奶中芬太尼类新精神活性物质的方法,包括以下步骤:
[0142]
(1)称取2.00g牛奶(其中添加浓度为400ng/ml的芬太尼、舒芬太尼、瑞芬太尼、奥芬太尼、乙酰芬太尼、卡芬太尼和浓度为80ng/ml的阿芬太尼各0.100ml),加入2.5ml水和16ml乙腈(分析纯),漩涡混合1min后,先加1.4g无水醋酸钠的混合粉末,迅速振摇,漩涡混合1min,再加入7g无水硫酸镁,迅速振摇,连续漩涡(2300r/min)混合5min,然后用4000r/min离心5min,移取全部上清液至鸡心瓶中,48℃旋蒸至干,用2ml洗脱液(组成为内含5mmol/l乙酸铵的0.1%甲酸水溶液:乙腈(色谱级)=9:1)洗脱,过0.22μm的尼龙66有机系滤膜,得到待上机样品溶液;
[0143]
(2)标准储备液配制:分别精密称取芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼标准品各10mg(精确至0.01mg)至小烧杯中,加0.1%甲酸甲醇溶液溶解,溶液定量移入10ml容量瓶中,用0.1%甲酸甲醇溶液稀释至刻度,摇匀,配制成浓度均为1.0mg/ml的标准储备液;
[0144]
混合标准中间溶液1配制:准确吸取浓度为1.0mg/ml的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼混合标准储备液各100μl于同一个100ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0μg/ml的混合标准中间溶液1;
[0145]
混合标准中间溶液2配制:准确吸取混合标准中间溶液1.0ml于10ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为0.10μg/ml的混合标准中间溶液2;
[0146]
标准工作溶液的配制:分别准确吸取混合标准中间溶液2和混合标准中间溶液1各200μl、400μl、1000μl于20ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,得芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0ng/ml、2.0ng/ml、5.0ng/ml、10.0ng/ml、20.0ng/ml、50.0ng/ml的系列标准工作溶液;
[0147]
对上述得到的系列标准工作溶液依次进行hplc-ms/ms检测,以各溶液浓度为横坐标,测定得到的响应值为纵坐标,绘制各溶液标准曲线;
[0148]
(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度;
[0149]
所述hplc-ms/ms检测的色谱条件为:采用waters acquity uplclm bhe c18色谱柱,进样量为5μl,色谱柱温度为36℃,流动相流量为0.3ml/min;
[0150]
液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
[0151]
梯度洗脱程序为:0~1.0min,10%流动相b;1.1~3.0min,65%流动相b;3.1~4.0min,65%流动相b;4.1~6.0min,10%流动相b;
[0152]
所述hplc-ms/ms检测的质谱条件为:
[0153]
可加热的电喷雾离子源;
[0154]
正离子扫描模式;
[0155]
离子源电压:5500v;
[0156]
离子源温度:550℃;
[0157]
气帘气压:25psi;
[0158]
碰撞气压:9psi;
[0159]
喷雾气压:55psi;
[0160]
加热气压:55psi;
[0161]
采集模式:多反应监测模式mrm;
[0162]
各化合物的质谱参数见表1。
[0163]
实施例5
[0164]
本实施例提供了一种检测可乐中芬太尼类新精神活性物质的方法,包括以下步骤:
[0165]
(1)称取2.10g可乐阴性样品2份(其中1份添加浓度为400ng/ml的芬太尼、舒芬太尼、瑞芬太尼、奥芬太尼、乙酰芬太尼、卡芬太尼和浓度为80ng/ml的阿芬太尼各0.100ml),各加入2ml水和15ml乙腈(分析纯),漩涡混合1min后,先加1.5g无水醋酸钠的混合粉末,迅速振摇,漩涡混合1min,再加入6g无水硫酸镁,迅速振摇,连续漩涡(2300r/min)混合5min,然后用4500r/min离心4min,移取全部上清液至鸡心瓶中,40℃旋蒸至干,用2.00ml洗脱液(组成为内含5mmol/l乙酸铵的0.1%甲酸水溶液:乙腈(色谱级)=9:1)洗脱,过0.22μm的尼龙66有机系滤膜,得到阴性样品基质空白(后续配基质标准曲线用)和待上机样品(含有标准品)溶液;
[0166]
(2)标准储备液配制:分别精密称取芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼标准品各10mg(精确至0.01mg)至小烧杯中,加0.1%甲酸甲醇溶液溶解,溶液定量移入10ml容量瓶中,用0.1%甲酸甲醇溶液稀释至刻度,摇匀,配制成浓度均为1.0mg/ml的标准储备液;
[0167]
混合标准中间溶液1配制:准确吸取浓度为1.0mg/ml的芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼混合标准储备液各100μl于同一个100ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0μg/ml的混合标准中间溶液1;
[0168]
混合标准中间溶液2配制:准确吸取混合标准中间溶液1.0ml于10ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,即得含芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为0.10μg/ml的混合标准中间溶液2;
[0169]
标准工作溶液的配制:分别准确吸取混合标准中间溶液2和混合标准中间溶液1各200μl、400μl、1000μl于20ml容量瓶中,用乙腈(色谱级)定容至刻度,摇匀,得芬太尼、瑞芬太尼、舒芬太尼、奥芬太尼、卡芬太尼、阿芬太尼、乙酰芬太尼浓度为1.0ng/ml、2.0ng/ml、5.0ng/ml、10.0ng/ml、20.0ng/ml、50.0ng/ml的系列标准工作溶液;同理,用前面制得的阴性样品基质空白代替乙腈配制基质系列标准工作溶液。
[0170]
对上述得到的系列标准工作溶液依次进行hplc-ms/ms检测,以各溶液浓度为横坐标,测定得到的响应值为纵坐标,绘制各溶液标准曲线;
[0171]
(3)将待上机样品溶液进行hplc-ms/ms检测,将各成分响应值代入步骤(2)得到的标准曲线中获得待检测样品中上述7种成分的浓度;
[0172]
所述hplc-ms/ms检测的色谱条件为:采用acquity uplc@hsst3色谱柱,进样量为5μl,色谱柱温度为35℃,流动相流量为0.3ml/min;
[0173]
液相色谱采用流动相a:内含5mmol/l乙酸铵的0.1%甲酸-水溶液和流动相b:乙腈为流动相;
[0174]
梯度洗脱程序为:0~0.5min,10%流动相b;0.5~1.0min,35%流动相b;1.0~2.5min,35%流动相b;2.5~3.5min,35~10%流动相b;3.5~6.0min,10%流动相b;
[0175]
所述hplc-ms/ms检测的质谱条件为:
[0176]
可加热的电喷雾离子源;
[0177]
正离子扫描模式;
[0178]
离子源电压:5500v;
[0179]
离子源温度:550℃;
[0180]
气帘气压:25psi;
[0181]
碰撞气压:9psi;
[0182]
喷雾气压:55psi;
[0183]
加热气压:55psi;
[0184]
采集模式:多反应监测模式mrm;
[0185]
各化合物的质谱参数见表1。
[0186]
实验例
[0187]
采用实施例1~5的检测方法检测分析结果见表2,其中实施例5的检测图谱见图1,
7种芬太尼标准品图谱见图2。
[0188]
表2:实施例1~5的检测分析结果表
[0189][0190]
采用实施例5的测定方法对线性方程、基质标准曲线配制及基质效应、检出限、回收率、精密度和准确度进行考察。
[0191]
基质效应:每个化合物的线性方程由以上6个点计算得到,最低浓度为loq(s/n≥10),并确保实际样品的浓度落在线性范围内,计算相关系数(r);将阴性空白同类样品按前述预处理方法处理后,将最后洗脱液收集,配制浓度范围1~50ng/ml标准曲线,同时对基质效应进行考察,通过进样分析后计算基质匹配标准曲线与标准溶液曲线斜率,并取两者比值即为基质效应,结果见表3。
[0192]
表3:基质效应考察结果
[0193][0194]
本试验通过比较相同浓度的同类芬太尼分别用试剂洗脱液和阴性空白样品洗脱液配制,发现7种芬太尼在可乐饮料食品基质中基质效应不显著,基质效应均处于77.3%-94.6%之间,普遍呈现基质抑制效应。但为了提高定量准确性仍建议使用基质匹配曲线外标法定量。因标准溶液曲线配置使用上机用初始流动相洗脱液,可以抵消部分基质效应(见表4)。不同的食品基质其基质效应各不相同,有的抑制或有的增强。
[0195]
表4:不同浓度芬太尼物质在不同食品基质中基质效应(%)比较
[0196][0197][0198]
检出限:取空白样品加入不同浓度的7种混合标准品溶液,按照前述样品预处理后上机检测,以信噪比s/n≥3时的质量浓度为检测限,s/n≥10时的质量浓度为定量限,且将定量限作为线性范围的最小浓度。7种芬太尼中除奥芬太尼检测限1.0ng/ml(或1.0ng/mg),其余6种可达0.5ng/ml(mg),定量限5ng/ml(或5.0ng/mg),根据信噪比阿芬太尼检测限可达0.05ng/ml(mg),定量限0.1ng/ml(或0.1ng/mg),结果见表5。
[0199]
表5:7种芬太尼信噪比
[0200][0201]
回收率、精密度和准确度试验:取待上机样品加入5.0,10,50ng/mg三种浓度的7种混合标准品溶液,按照前述样品预处理后上机检测,计算回收率(准确度),精密度,结果见表6。
[0202]
表6:各芬太尼回归方程、线性范围、相关系数、精密度和准确度
[0203][0204]
由以上实施例可知,本发明提供了一种检测食品中芬太尼类新精神活性物质的方法,本发明的检测方法能够准确、高效地识别食品中是否存在芬太尼类精神活性物质,可特异性区别各种芬太尼类似物及其异构体。
[0205]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。